Entalpia em unidades intensivas – Entalpia específica
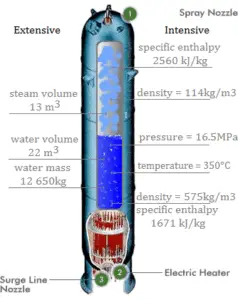
A entalpia pode ser transformada em uma variável intensiva ou específica dividindo-se pela massa . Os engenheiros usam mais a entalpia específica na análise termodinâmica do que a própria entalpia. A entalpia específica (h) de uma substância é a sua entalpia por unidade de massa. É igual à entalpia total (H) dividida pela massa total (m).
h = H / m
Onde:
h = entalpia específica (J / kg)
H = entalpia (J)
m = massa (kg)
Observe que a entalpia é a quantidade termodinâmica equivalente ao conteúdo total de calor de um sistema. A entalpia específica é igual à energia interna específica do sistema mais o produto da pressão e volume específico .
h = u + pv
Em geral, a entalpia é uma propriedade de uma substância , como pressão, temperatura e volume, mas não pode ser medida diretamente. Normalmente, a entalpia de uma substância é dada com relação a algum valor de referência. Por exemplo, a entalpia específica da água ou vapor é dada usando a referência de que a entalpia específica da água é zero a 0,01 ° C e pressão atmosférica normal , onde h L = 0,00 kJ / kg . O fato de o valor absoluto da entalpia específica ser desconhecido não é um problema, no entanto, porque é a alteração na entalpia específica (∆h) e não o valor absoluto que é importante nos problemas práticos.
Entalpia específica do vapor úmido
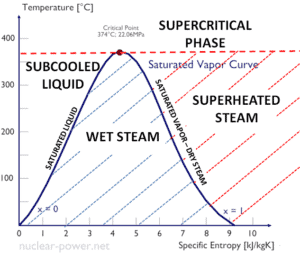 A entalpia específica da água líquida saturada (x = 0) e do vapor seco (x = 1) pode ser selecionada nas tabelas de vapor. No caso do vapor molhado , a entalpia real pode ser calculado com a qualidade de vapor, x , e as entalpias específicas de água no estado líquido saturado e vapor seco:
A entalpia específica da água líquida saturada (x = 0) e do vapor seco (x = 1) pode ser selecionada nas tabelas de vapor. No caso do vapor molhado , a entalpia real pode ser calculado com a qualidade de vapor, x , e as entalpias específicas de água no estado líquido saturado e vapor seco:
h molhado = h s x + (1 – x) h l
Onde
h úmido = entalpia do vapor úmido (J / kg)
h s = entalpia do vapor “seco” (J / kg)
h l = entalpia de água líquida saturada (J / kg)
Como pode ser visto, o vapor úmido sempre terá entalpia menor do que o vapor seco.
Exemplo:
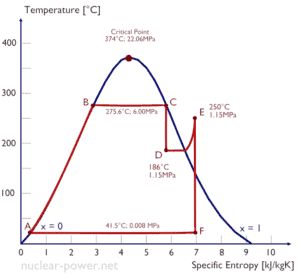
Um estágio de alta pressão da turbina a vapor opera em estado estacionário com condições de entrada de 6 MPa, t = 275,6 ° C, x = 1 (ponto C). O vapor sai deste estágio da turbina a uma pressão de 1,15 MPa, 186 ° C ex = 0,87 (ponto D). Calcule a diferença de entalpia entre esses dois estados.
A entalpia para o estado C pode ser coletada diretamente das tabelas de vapor, enquanto a entalpia para o estado D deve ser calculada usando a qualidade do vapor:
h 1, molhado = 2785 kJ / kg
h 2, molhado = h 2, s x + (1 – x) h 2, l = 2782. 0,87 + (1 – 0,87). 790 = 2420 + 103 = 2523 kJ / kg
Δh = 262 kJ / kg
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.