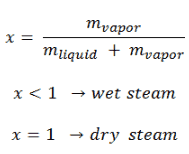Líquido saturado y subenfriado
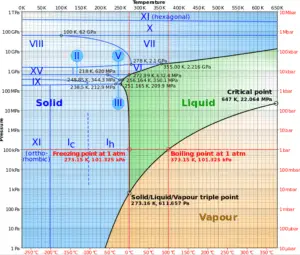
Fuente: wikipedia.org CC BY-SA
Como se puede ver en el diagrama de fase del agua, en las regiones de dos fases (p. Ej., En el borde de las fases vapor / líquido), la temperatura específica solo establecerá la presión y la presión específica establecerá la temperatura.
- La curva de vapor de saturación es la curva que separa el estado de dos fases y el estado de vapor sobrecalentado en el diagrama Ts.
- La curva de líquido saturado es la curva que separa el estado líquido subenfriado y el estado de dos fases en el diagrama Ts.
Si un agua existe como líquido a la temperatura y presión de saturación con una calidad de x = 0 , se denomina estado líquido saturado (monofásico). Si la temperatura del líquido es inferior a la temperatura de saturación para la presión existente, se llama líquido subenfriado o líquido comprimido . El término subenfriamiento se refiere a un líquido que existe a una temperatura por debajo de su punto de ebullición normal. Por ejemplo, el agua normalmente hierve a 100 ° C (a presión atmosférica); a temperatura ambiente 20 ° C el agua se denomina “subenfriado”. Analógicamente, el subenfriamiento se define también en ingeniería nuclear pero para otro propósito.
Por ejemplo, la temperatura en el presurizador se puede mantener a 350 ° C (662 ° F), lo que proporciona un margen de subenfriamiento (la diferencia entre la temperatura del presurizador y la temperatura más alta en el núcleo del reactor) de 30 ° C. El margen de subenfriamiento es un parámetro de seguridad muy importante de los PWR, ya que se debe excluir la ebullición en el núcleo del reactor.
Calidad de vapor – Fracción de sequedad
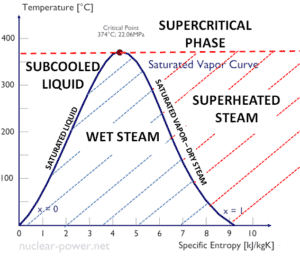 Como se puede ver en el diagrama de fases del agua , en las regiones de dos fases (p. Ej., En el borde de las fases vapor / líquido), solo la temperatura establecida establecerá la presión y la presión específica establecerá la temperatura. Pero estos parámetros no definirán el volumen y la entalpía porque necesitaremos conocer la proporción relativa de las dos fases presentes.
Como se puede ver en el diagrama de fases del agua , en las regiones de dos fases (p. Ej., En el borde de las fases vapor / líquido), solo la temperatura establecida establecerá la presión y la presión específica establecerá la temperatura. Pero estos parámetros no definirán el volumen y la entalpía porque necesitaremos conocer la proporción relativa de las dos fases presentes.
La fracción de masa del vapor en una región de vapor líquido de dos fases se denomina calidad del vapor (o fracción de sequedad), x , y se obtiene mediante la siguiente fórmula:
El valor de la calidad varía de cero a la unidad . Aunque se define como una relación, la calidad se da con frecuencia como un porcentaje. Desde este punto de vista, distinguimos entre tres tipos básicos de vapor. Debe agregarse, en x = 0, estamos hablando del estado líquido saturado (monofásico).
- Vapor húmedo
- Vapor seco
- Vapor supercalentado
Esta clasificación del vapor tiene su limitación. Considere el comportamiento del sistema que se calienta a la presión, que es más alta que la presión crítica . En este caso, no habría cambio de fase de líquido a vapor. En todos los estados solo habría una fase. La vaporización y la condensación pueden ocurrir solo cuando la presión es menor que la presión crítica. Los términos líquido y vapor tienden a perder su significado.
Ver también: saturación
Propiedades de Steam – Tablas de Steam
El agua y el vapor son un fluido común utilizado para el intercambio de calor en el circuito primario (desde la superficie de las barras de combustible hasta el flujo de refrigerante) y en el circuito secundario. Se utiliza debido a su disponibilidad y alta capacidad calorífica, tanto para enfriamiento como para calefacción. Es especialmente efectivo para transportar calor a través de la vaporización y la condensación de agua debido a su gran calor latente de vaporización .
Una desventaja es que los reactores moderados por agua tienen que usar un circuito primario de alta presión para mantener el agua en estado líquido y para lograr una eficiencia termodinámica suficiente. El agua y el vapor también reaccionan con metales que se encuentran comúnmente en industrias como el acero y el cobre, que se oxidan más rápido por el agua y el vapor no tratados. En casi todas las centrales térmicas (carbón, gas, nuclear), el agua se utiliza como fluido de trabajo (utilizado en un circuito cerrado entre la caldera, la turbina de vapor y el condensador) y el refrigerante (utilizado para intercambiar el calor residual a un cuerpo de agua). o llévelo por evaporación en una torre de enfriamiento).
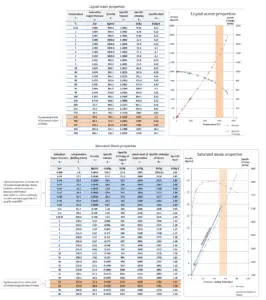
El agua y el vapor son un medio común porque sus propiedades son muy conocidas . Sus propiedades están tabuladas en las llamadas ” Tablas de Steam “. En estas tablas, las propiedades básicas y clave, como la presión, la temperatura, la entalpía, la densidad y el calor específico, se tabulan a lo largo de la curva de saturación vapor-líquido en función de la temperatura y la presión. Las propiedades también están tabuladas para estados monofásicos ( agua comprimida o vapor sobrecalentado ) en una red de temperaturas y presiones que se extienden a 2000 ºC y 1000 MPa.
Se pueden encontrar más datos completos y autorizados en la página del NIST Webbook sobre las propiedades termofísicas de los fluidos.
Ver también: Tablas de vapor
Referencia especial: Allan H. Harvey. Propiedades termodinámicas del agua, NISTIR 5078. Recuperado de https://www.nist.gov/sites/default/files/documents/srd/NISTIR5078.htm