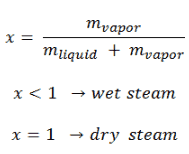Líquido saturado e sub-resfriado
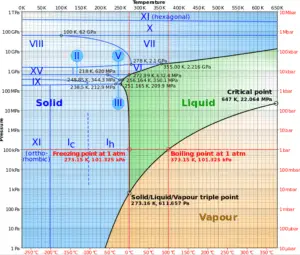
Fonte: wikipedia.org CC BY-SA
Como pode ser visto no diagrama de fases da água, nas regiões bifásicas (por exemplo, na fronteira das fases vapor / líquido), a especificação da temperatura sozinha definirá a pressão e a pressão especificada definirá a temperatura.
- A curva de vapor de saturação é a curva que separa o estado de duas fases e o estado de vapor superaquecido no diagrama Ts.
- A curva líquida saturada é a curva que separa o estado líquido sub – resfriado e o estado de duas fases no diagrama Ts.
Se uma água existe como líquido na temperatura e pressão de saturação com qualidade de x = 0 , isso é chamado de estado líquido saturado (monofásico). Se a temperatura do líquido for mais baixa que a temperatura de saturação da pressão existente, isso será chamado de líquido sub – resfriado ou líquido comprimido . O termo sub-resfriamento refere-se a um líquido existente a uma temperatura abaixo do seu ponto de ebulição normal. Por exemplo, a água normalmente ferve a 100 ° C (à pressão atmosférica); à temperatura ambiente de 20 ° C, a água é denominada “sub-resfriada”. Analogamente, o sub-resfriamento é definido também na engenharia nuclear, mas para outro propósito.
Por exemplo, a temperatura no pressurizador pode ser mantida em 350 ° C (662 ° F), o que fornece uma margem de sub-resfriamento (a diferença entre a temperatura do pressurizador e a temperatura mais alta no núcleo do reator) de 30 ° C. A margem de sub-resfriamento é um parâmetro de segurança muito importante dos PWRs, pois a ebulição no núcleo do reator deve ser excluída.
Qualidade de Vapor – Fração de Secura
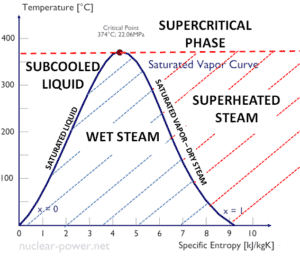 Como pode ser visto no diagrama de fases da água , nas regiões bifásicas (por exemplo, na fronteira das fases vapor / líquido), a especificação da temperatura por si só definirá a pressão e a especificação da pressão definirá a temperatura. Mas esses parâmetros não definirão o volume e a entalpia, pois precisaremos conhecer a proporção relativa das duas fases presentes.
Como pode ser visto no diagrama de fases da água , nas regiões bifásicas (por exemplo, na fronteira das fases vapor / líquido), a especificação da temperatura por si só definirá a pressão e a especificação da pressão definirá a temperatura. Mas esses parâmetros não definirão o volume e a entalpia, pois precisaremos conhecer a proporção relativa das duas fases presentes.
A fração de massa do vapor em uma região de vapor líquido de duas fases é chamada qualidade do vapor (ou fração de secura), x , e é dada pela seguinte fórmula:
O valor da qualidade varia de zero a unidade . Embora definida como uma proporção, a qualidade é frequentemente fornecida como uma porcentagem. Deste ponto de vista, distinguimos entre três tipos básicos de vapor. Deve ser adicionado, em x = 0, estamos falando de estado líquido saturado (monofásico).
- Vapor Molhado
- Vapor seco
- Vapor superaquecido
Esta classificação de vapor tem sua limitação. Considere o comportamento do sistema que é aquecido à pressão, que é maior que a pressão crítica . Nesse caso, não haveria alteração na fase do líquido para o vapor. Em todos os estados, haveria apenas uma fase. A vaporização e a condensação podem ocorrer apenas quando a pressão é menor que a pressão crítica. Os termos líquido e vapor tendem a perder seu significado.
Veja também: Saturação
Propriedades do Steam – Tabelas Steam
Água e vapor são um fluido comum usado para a troca de calor no circuito primário (da superfície das barras de combustível ao fluxo do líquido de refrigeração) e no circuito secundário. É utilizado devido à sua disponibilidade e alta capacidade de aquecimento, tanto para refrigeração quanto para aquecimento. É especialmente eficaz para transportar calor através da vaporização e condensação da água devido ao seu calor latente muito grande de vaporização .
Uma desvantagem é que os reatores moderados a água precisam usar o circuito primário de alta pressão para manter a água no estado líquido e para obter eficiência termodinâmica suficiente. Água e vapor também reagem com metais comumente encontrados em indústrias como aço e cobre, que são oxidados mais rapidamente por água e vapor não tratados. Em quase todas as centrais térmicas (carvão, gás, nuclear), a água é usada como fluido de trabalho (usado em um circuito fechado entre caldeira, turbina a vapor e condensador) e o líquido de arrefecimento (usado para trocar o calor residual por um corpo de água) ou carregue-o por evaporação em uma torre de resfriamento).
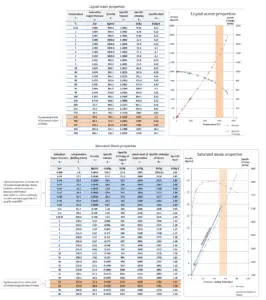
Água e vapor são um meio comum, porque suas propriedades são muito conhecidas . Suas propriedades estão tabuladas nas chamadas ” Tabelas Steam “. Nessas tabelas, as propriedades básicas e principais, como pressão, temperatura, entalpia, densidade e calor específico, são tabuladas ao longo da curva de saturação vapor-líquido em função da temperatura e da pressão. As propriedades também são tabuladas para estados monofásicos ( água compactada ou vapor superaquecido ) em uma grade de temperaturas e pressões que se estendem a 2000 ºC e 1000 MPa.
Outros dados oficiais abrangentes podem ser encontrados na página do NIST Webbook sobre propriedades termofísicas de fluidos.
Veja também: Tabelas Steam
Referência especial: Allan H. Harvey. Propriedades termodinâmicas da água, NISTIR 5078. Recuperado em https://www.nist.gov/sites/default/files/documents/srd/NISTIR5078.htm