Spezifische Entropie
Die Entropie kann durch Teilen durch die Masse in eine intensive oder spezifische Variable umgewandelt werden. Ingenieure verwenden die spezifische Entropie in der thermodynamischen Analyse mehr als die Entropie selbst. Die spezifische Entropie (n) einer Substanz ist ihre Entropie pro Masseneinheit. Sie entspricht der Gesamtentropie (S) geteilt durch die Gesamtmasse (m).
s = S / m
wo:
s = spezifische Entropie (J / kg)
S = Entropie (J)
m = Masse (kg)
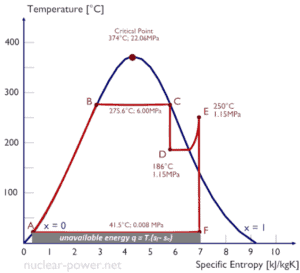
Die Entropie quantifiziert die Energie eines Stoffes, der für nützliche Arbeiten nicht mehr zur Verfügung steht. Da die Entropie so viel über die Nützlichkeit einer bei der Durchführung von Arbeiten übertragenen Wärmemenge aussagt, enthalten die Dampftabellen Werte der spezifischen Entropie (s = S / m) als Teil der in der Tabelle aufgeführten Informationen.
Im Allgemeinen ist die spezifische Entropie eine Eigenschaft einer Substanz wie Druck, Temperatur und Volumen, kann jedoch nicht direkt gemessen werden. Normalerweise wird die Entropie eines Stoffes in Bezug auf einen Referenzwert angegeben. Zum Beispiel wird die spezifische Entropie von Wasser oder Dampf unter Verwendung der Referenz angegeben, dass die spezifische Entropie von Wasser bei 0,01 ° C und normalem atmosphärischem Druck Null ist , wobei s = 0,00 kJ / kg. Die Tatsache, dass der absolute Wert der spezifischen Entropie unbekannt ist, ist jedoch kein Problem, da es die Änderung der spezifischen Entropie ((s) und nicht der absolute Wert ist, der für praktische Probleme wichtig ist.
Temperatur-Entropie-Diagramme – Ts-Diagramme
Im Allgemeinen werden die Phasen eines Stoffes und die Beziehungen zwischen seinen Eigenschaften am häufigsten in Eigenschaftsdiagrammen dargestellt . Es wurde eine große Anzahl verschiedener Eigenschaften definiert, und es gibt einige Abhängigkeiten zwischen den Eigenschaften.
Ein Temperatur-Entropie-Diagramm ( Ts-Diagramm ) ist der Diagrammtyp, der am häufigsten zur Analyse von Energieübertragungssystemzyklen verwendet wird. Es wird in der Thermodynamik verwendet, um Änderungen der Temperatur und der spezifischen Entropie während eines thermodynamischen Prozesses oder Zyklus zu visualisieren.
Dies liegt daran , die Arbeit von oder auf dem System und die getan Wärme hinzugefügt oder entfernt aus dem System kann auf dem visualisiert wird Ts Diagramm . Nach der Definition der Entropie entspricht die Wärme, die zu oder von einem System übertragen wird, der Fläche unter der Ts-Kurve des Prozesses.
dQ = TdS
Ein isentropischer Prozess wird in einem Ts-Diagramm als vertikale Linie dargestellt, während ein isothermer Prozess eine horizontale Linie ist. In einem idealisierten Zustand ist die Kompression eine Pumpe, die Kompression in einem Kompressor und die Expansion in einer Turbine sind isentrope Prozesse. Daher ist es in der Energietechnik sehr nützlich, da diese Geräte in thermodynamischen Kreisläufen von Kraftwerken eingesetzt werden.
Beachten Sie, dass die isentropischen Annahmen nur für ideale Kreisprozessen gelten. Reale thermodynamische Kreisprozessen haben inhärente Energieverluste aufgrund der Ineffizienz von Kompressoren und Turbinen.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.