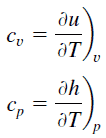Wärmekapazität
 Verschiedene Substanzen sind betroffen unterschiedliche Größen durch die Zugabe von Wärme . Wenn verschiedenen Substanzen eine bestimmte Wärmemenge zugesetzt wird, steigen ihre Temperaturen um unterschiedliche Mengen. Diese Proportionalitätskonstante zwischen der Wärme Q , die das Objekt absorbiert oder verliert, und der resultierenden Temperaturänderung T des Objekts ist als Wärmekapazität C eines Objekts bekannt.
Verschiedene Substanzen sind betroffen unterschiedliche Größen durch die Zugabe von Wärme . Wenn verschiedenen Substanzen eine bestimmte Wärmemenge zugesetzt wird, steigen ihre Temperaturen um unterschiedliche Mengen. Diese Proportionalitätskonstante zwischen der Wärme Q , die das Objekt absorbiert oder verliert, und der resultierenden Temperaturänderung T des Objekts ist als Wärmekapazität C eines Objekts bekannt.
C = Q / ΔT
Die Wärmekapazität ist eine umfangreiche Eigenschaft der Materie, dh sie ist proportional zur Größe des Systems. Die Wärmekapazität C hat die Energieeinheit pro Grad oder Energie pro Kelvin. Wenn das gleiche Phänomen wie eine intensive Eigenschaft ausgedrückt wird , wird die Wärmekapazität durch die Menge an Substanz, Masse oder Volumen geteilt, sodass die Menge unabhängig von der Größe oder dem Ausmaß der Probe ist.
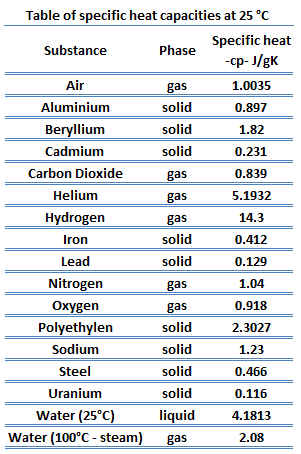
Spezifische Wärmekapazität
Die Wärmekapazität eines Stoffes pro Masseneinheit wird als spezifische Wärmekapazität (c p ) des Stoffes bezeichnet. Der Index p gibt an, dass die Wärmekapazität und die spezifische Wärmekapazität gelten, wenn die Wärme bei konstantem Druck hinzugefügt oder abgeführt wird .
c p = Q / m & Dgr; T.
Spezifische Wärmekapazität des idealen Gases
Im Idealgasmodell werden die intensiven Eigenschaften c v und c p für reine, einfache kompressible Substanzen als partielle Ableitungen der inneren Energie u (T, v) bzw. der Enthalpie h (T, p) definiert :
wobei die Indizes v und p die Variablen bezeichnen, die während der Differenzierung festgehalten werden. Die Eigenschaften c v und c p werden als spezifische Wärme (oder Wärmekapazität ) bezeichnet, da sie unter bestimmten besonderen Bedingungen die Temperaturänderung eines Systems mit der durch Wärmeübertragung hinzugefügten Energiemenge in Beziehung setzen. Ihre SI – Einheiten sind J / kg K oder J / mol K . Für Gase sind zwei spezifische Wärmemengen definiert, eine für konstantes Volumen (c v ) und eine für konstanten Druck (c p ) .
 Nach dem ersten Hauptsatz der Thermodynamik beträgt für einen Prozess mit konstantem Volumen mit einem einatomigen idealen Gas die molare spezifische Wärme:
Nach dem ersten Hauptsatz der Thermodynamik beträgt für einen Prozess mit konstantem Volumen mit einem einatomigen idealen Gas die molare spezifische Wärme:
C v = 3 / 2R = 12,5 J / mol K.
da
U = 3 / 2nRT
Es kann abgeleitet werden, dass die molare spezifische Wärme bei konstantem Druck ist:
C p = C v + R = 5 / 2R = 20,8 J / mol K.
Dieses C p ist größer als die molare spezifische Wärme bei konstantem Volumen C v , da nun nicht nur Energie zugeführt werden muss , um die Temperatur des Gases zu erhöhen, sondern auch, damit das Gas funktioniert, da sich in diesem Fall das Volumen ändert.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.