Volume d’un atome et d’un noyau
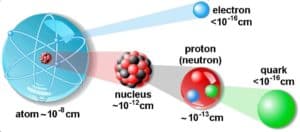
L’atome est constitué d’un noyau petit mais massif entouré d’un nuage d’ électrons se déplaçant rapidement . Le noyau est composé de protons et de neutrons . Les rayons nucléaires typiques sont de l’ordre de 10 -14 m. En supposant une forme sphérique, les rayons nucléaires peuvent être calculés selon la formule suivante:
r = r 0 . Un 1/3
où r 0 = 1,2 x 10 -15 m = 1,2 fm
Si nous utilisons cette approximation, nous nous attendons donc à ce que le volume du noyau soit de l’ordre de 4 / 3πr 3 ou 7,23 × 10 -45 m 3 pour les noyaux d’hydrogène ou 1721 × 10 -45 m 3 pour 238 U noyaux. Ce sont des volumes de noyaux et des noyaux atomiques (protons et neutrons) contiennent environ 99,95% de la masse de l’atome.
Un atome est-il un espace vide?
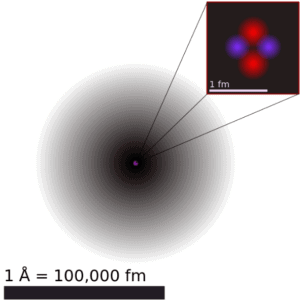
Le volume d’un atome est environ 15 ordres de grandeur plus grand que le volume d’un noyau. Pour l’atome d’uranium , le rayon de Van der Waals est d’environ 186 pm = 1,86 × 10 -10 m . Le rayon de Van der Waals, rw , d’un atome est le rayon d’une sphère dure imaginaire représentant la distance d’approche la plus proche pour un autre atome. En prenant la forme sphérique, l’ atome d’ uranium a un volume d’environ 26,9 × 10 −30 m 3 . Mais cet «immense» espace est principalement occupé par les électrons, car le noyau n’occupe qu’environ 1721 × 10 -45 m3 de l’espace. Ensemble, ces électrons ne pèsent qu’une fraction (disons 0,05%) de l’atome entier.
Il peut sembler que l’espace et la matière sont vides , mais ce n’est pas le cas . En raison de la nature quantique des électrons , les électrons ne sont pas des particules ponctuelles, ils sont étalés sur tout l’atome. La description classique ne peut pas être utilisée pour décrire des choses à l’échelle atomique. À l’échelle atomique, les physiciens ont découvert que la mécanique quantique décrivait très bien les choses à cette échelle. Les emplacements des particules en mécanique quantique ne sont pas à une position exacte, ils sont décrits par une fonction de densité de probabilité . Par conséquent, l’espace dans un atome (entre les électrons et un noyau atomique) n’est pas vide, mais il est rempli par une fonction de densité de probabilité d’électrons (généralement appelée « nuage d’électrons »).
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci