Energia interna específica
A energia interna específica (u) de uma substância é sua energia interna por unidade de massa. É uma propriedade intensiva . É igual à energia interna total (U) dividida pela massa total (m).
u = U / m
Onde:
u = energia interna específica (J / kg)
U = energia interna (J)
m = massa (kg)
Energia Interna – Energia Térmica
Energia potencial e energia cinética , discutidas nos capítulos anteriores, são formas macroscópicas de energia . Eles dependem de variáveis macroscópicas, como a posição e a velocidade dos objetos.
Na termodinâmica, energia interna (também chamada de energia térmica ) é definida como a energia associada a formas microscópicas de energia . É uma quantidade extensa , depende do tamanho do sistema ou da quantidade de substância que ele contém. A unidade SI de energia interna é o joule (J) . É a energia contida no sistema, excluindo a energia cinética do movimento do sistema como um todo e a energia potencial do sistema. As formas microscópicas de energia incluem aquelas devidas à rotação , vibração, translação e interaçõesentre as moléculas de uma substância. Nenhuma dessas formas de energia pode ser medida ou avaliada diretamente, mas técnicas foram desenvolvidas para avaliar a mudança na soma total de todas essas formas microscópicas de energia.
Além disso, a energia é armazenada nas ligações químicas entre os átomos que compõem as moléculas. Esse armazenamento de energia no nível atômico inclui energia associada a estados orbitais de elétrons, rotação nuclear e forças de ligação no núcleo.
A energia interna é representada pelo símbolo U , e a mudança na energia interna em um processo é U 2 – U 1 .
Energia microscópica
A energia interna envolve energia na escala microscópica . Pode ser dividido em energia microscópica potencial, pote U e energia cinética microscópica, U kin , componentes:
U = U pote + U parentes
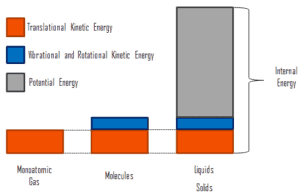 onde a energia cinética microscópica, U kin , envolve os movimentos de todas as partículas do sistema em relação à estrutura do centro de massa. Para um gás monatômico ideal , essa é apenas a energia cinética translacional do movimento linear dos átomos. Partículas monoatômicas não giram ou vibram. O comportamento do sistema é bem descrito pela teoria cinética dos gases. A teoria cinética baseia-se no fato de que durante uma colisão elástica entre uma molécula com alta energia cinética e outra com baixa energia cinética, parte da energia será transferida para a molécula de energia cinética inferior. No entanto, para gases poliatômicos, existem rotações eenergia cinética vibracional também.
onde a energia cinética microscópica, U kin , envolve os movimentos de todas as partículas do sistema em relação à estrutura do centro de massa. Para um gás monatômico ideal , essa é apenas a energia cinética translacional do movimento linear dos átomos. Partículas monoatômicas não giram ou vibram. O comportamento do sistema é bem descrito pela teoria cinética dos gases. A teoria cinética baseia-se no fato de que durante uma colisão elástica entre uma molécula com alta energia cinética e outra com baixa energia cinética, parte da energia será transferida para a molécula de energia cinética inferior. No entanto, para gases poliatômicos, existem rotações eenergia cinética vibracional também.
A energia potencial microscópica, U pot , envolve as ligações químicas entre os átomos que compõem as moléculas, as forças de ligação no núcleo e também os campos de força física no sistema (por exemplo, campos elétricos ou magnéticos).
Em líquidos e sólidos, há um componente significativo da energia potencial associada às forças de atração intermoleculares .
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.