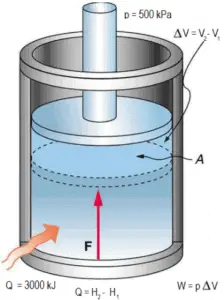
Modelo de gás ideal
O modelo de gás ideal é usado para prever o comportamento dos gases e é um dos modelos de substâncias mais úteis e mais usados já desenvolvidos. Descobri que, se confinarmos amostras de 1 mol de vários gases em volume idêntico e mantivermos os gases na mesma temperatura , suas pressões medidas serão quase as mesmas . Além disso, quando confinamos gases em densidades mais baixas, as diferenças tendem a desaparecer. Verificou-se que esses gases tendem a obedecer à seguinte relação, conhecida como lei dos gases ideais :
pV = nRT
Onde:
p é a pressão absoluta do gás
n é a quantidade de substância
T é a temperatura absoluta
Vé o volume
R é a constante de gás ideal, ou universal,igual ao produto da constante de Boltzmann e da constante de Avogadro. O poder da lei do gás ideal está em sua simplicidade. Quando quaisquer duas das variáveis termodinâmicas , p, ve T são dadas, a terceira pode ser facilmente encontrada.
O modelo de gás ideal é baseado nas seguintes suposições:
- A pressão, o volume e a temperatura de um gás ideal obedecem à lei do gás ideal .
- A energia interna específica é apenas uma função da temperatura: u = u (T)
- A massa molar de um gás ideal é idêntica à massa molar da substância real
- Os aquecimentos específicos – c p e c v – são independentes da temperatura, o que significa que são constantes.
Do ponto de vista microscópico, é baseado nas seguintes premissas:
- As moléculas do gás são pequenas esferas duras .
- As únicas forças entre as moléculas de gás são aquelas que determinam as colisões pontuais .
- Todas as colisões são elásticas e todo movimento é sem atrito .
- A distância média entre as moléculas é muito maior que o tamanho das moléculas.
- As moléculas estão se movendo em direções aleatórias.
- Não há outra força atraente ou repulsiva entre essas moléculas.
Validade da lei do gás ideal
Como o gás ideal é definido como aquele em que todas as colisões entre átomos ou moléculas são perfeitamente elásticas e nas quais não existem forças atraentes intermoleculares, não existe na natureza algo como um gás verdadeiramente ideal. Por outro lado, todos os gases reais se aproximam do estado ideal a baixas pressões (densidades) . A baixas pressões, as moléculas estão suficientemente afastadas para que não interajam.
Em outras palavras, a Lei do Gás Ideal é precisa apenas em pressões relativamente baixas (em relação à pressão crítica p cr ) e em altas temperaturas (em relação à temperatura crítica T cr ). Nesses parâmetros, o fator de compressibilidade, Z = pv / RT , é de aproximadamente 1 . O fator de compressibilidade é usado para explicar o desvio da situação ideal. Esse fator de correção depende da pressão e temperatura para cada gás considerado.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.