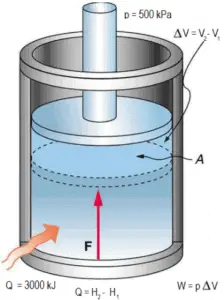
Ideales Gasmodell
Das ideale Gasmodell dient zur Vorhersage des Verhaltens von Gasen und ist eines der nützlichsten und am häufigsten verwendeten Stoffmodelle, die jemals entwickelt wurden. Ich habe festgestellt, dass , wenn wir darauf beschränken , 1 mol Proben von verschiedenen Gasen in gleichem Volumen und halten die Gase an der gleichen Temperatur , dann ihre gemessenen Drücke sind fast die gleichen . Darüber hinaus verschwinden die Unterschiede, wenn wir Gase mit niedrigeren Dichten einschließen. Es wurde festgestellt, dass solche Gase in der Regel die folgende Beziehung einhalten, die als ideales Gasgesetz bekannt ist :
pV = nRT
wo:
p ist der absolute Druck des Gases
n ist die Menge der Substanz
T ist die absolute Temperatur
Vist das Volumen
R ist die ideale oder universelle Gaskonstante , die dem Produkt der Boltzmann-Konstante und der Avogadro-Konstante entspricht. Die Kraft des idealen Gasgesetzes liegt in seiner Einfachheit. Wenn zwei der thermodynamischen Variablen p, v und T gegeben sind, kann die dritte leicht gefunden werden.
Das ideale Gasmodell basiert auf folgenden Annahmen:
- Der Druck, das Volumen und die Temperatur eines idealen Gases entsprechen dem idealen Gasgesetz .
- Die spezifische innere Energie ist nur eine Funktion der Temperatur: u = u (T)
- Die Molmasse eines idealen Gases ist identisch mit der Molmasse der realen Substanz
- Die spezifischen Erhitzungen – c p und c v – sind unabhängig von der Temperatur, was bedeutet, dass sie Konstanten sind.
Aus mikroskopischer Sicht basiert es auf folgenden Annahmen:
- Die Moleküle des Gases sind kleine, harte Kugeln .
- Die einzigen Kräfte zwischen den Gasmolekülen sind diejenigen, die die punktförmigen Kollisionen bestimmen .
- Alle Kollisionen sind elastisch und jede Bewegung ist reibungslos .
- Der durchschnittliche Abstand zwischen Molekülen ist viel größer als die Größe der Moleküle.
- Die Moleküle bewegen sich in zufällige Richtungen.
- Es gibt keine andere anziehende oder abstoßende Kraft zwischen diesen Molekülen.
Gültigkeit des idealen Gasgesetzes
Da ideales Gas als eines definiert ist, bei dem alle Kollisionen zwischen Atomen oder Molekülen vollkommen elastisch sind und bei dem es keine intermolekularen Anziehungskräfte gibt, gibt es in der Natur kein wirklich ideales Gas. Andererseits nähern sich alle realen Gase bei niedrigen Drücken (Dichten) dem Idealzustand an . Bei niedrigen Drücken sind Moleküle weit genug voneinander entfernt, dass sie nicht miteinander interagieren.
Mit anderen Worten ist das ideale Gasgesetz nur bei relativ niedrigen Drücken (relativ zum kritischen Druck p cr ) und hohen Temperaturen (relativ zur kritischen Temperatur T cr ) genau . Bei diesen Parametern beträgt der Kompressibilitätsfaktor Z = pv / RT ungefähr 1 . Der Kompressibilitätsfaktor wird verwendet, um Abweichungen von der idealen Situation zu berücksichtigen. Dieser Korrekturfaktor ist abhängig von Druck und Temperatur für jedes betrachtete Gas.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.