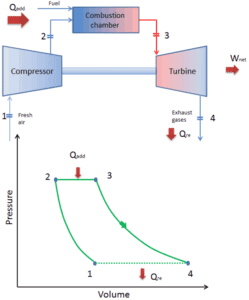
Ciclo Brayton – Motor de turbina
En 1872, un ingeniero estadounidense, George Bailey Brayton, avanzó el estudio de los motores térmicos patentando un motor de combustión interna a presión constante, que inicialmente usaba gas vaporizado pero luego usaba combustibles líquidos como el queroseno. Este motor térmico se conoce como ” Motor Listo de Brayton “ . Significa que el motor Brayton original usaba un compresor de pistón y un expansor de pistón en lugar de una turbina de gas y un compresor de gas.
Hoy en día, los modernos motores de turbina de gas y los motores de inyección de aire también son motores de calor de presión constante, por lo tanto, describimos su termodinámica por el ciclo de Brayton . En general, el ciclo de Brayton describe el funcionamiento de un motor térmico de presión constante .
Es uno de los ciclos termodinámicos más comunes que se pueden encontrar en las centrales eléctricas de turbinas de gas o en aviones. A diferencia del ciclo de Carnot , el ciclo de Brayton no ejecuta procesos isotérmicos , ya que estos deben realizarse muy lentamente. En un ciclo Brayton ideal , el sistema que ejecuta el ciclo experimenta una serie de cuatro procesos: dos procesos isentrópicos (adiabáticos reversibles) alternados con dos procesos isobáricos.
Dado que el principio de Carnot establece que ningún motor puede ser más eficiente que un motor reversible ( un motor térmico de Carnot ) que opera entre los mismos depósitos de alta temperatura y baja temperatura, una turbina de gas basada en el ciclo Brayton debe tener una eficiencia menor que la eficiencia de Carnot.
Una gran turbina de gas de un solo ciclo típicamente produce, por ejemplo, 300 megavatios de energía eléctrica y tiene una eficiencia térmica del 35-40%. Las plantas modernas de turbina de gas de ciclo combinado (CCGT), en las que el ciclo termodinámico consta de dos ciclos de planta de energía (por ejemplo, el ciclo Brayton y el ciclo Rankine), pueden lograr una eficiencia térmica de alrededor del 55%.
Ciclo Brayton – pV, diagrama Ts
El ciclo de Brayton a menudo se representa en un diagrama de volumen de presión (diagrama pV ) y en un diagrama de temperatura-entropía ( diagrama Ts ).
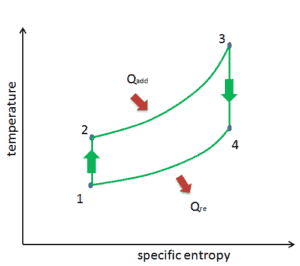
Cuando se trazan en un diagrama de volumen de presión , los procesos isobáricos siguen las líneas isobáricas para el gas (las líneas horizontales), los procesos adiabáticos se mueven entre estas líneas horizontales y el área delimitada por la ruta completa del ciclo representa el trabajo total que se puede hacer durante uno ciclo.
El diagrama de temperatura-entropía ( diagrama Ts) en el que el estado termodinámico se especifica mediante un punto en un gráfico con entropía específica (s) como eje horizontal y temperatura absoluta (T) como eje vertical. Los diagramas Ts son una herramienta útil y común, particularmente porque ayuda a visualizar la transferencia de calor durante un proceso. Para procesos reversibles (ideales), el área bajo la curva Ts de un proceso es el calor transferido al sistema durante ese proceso.
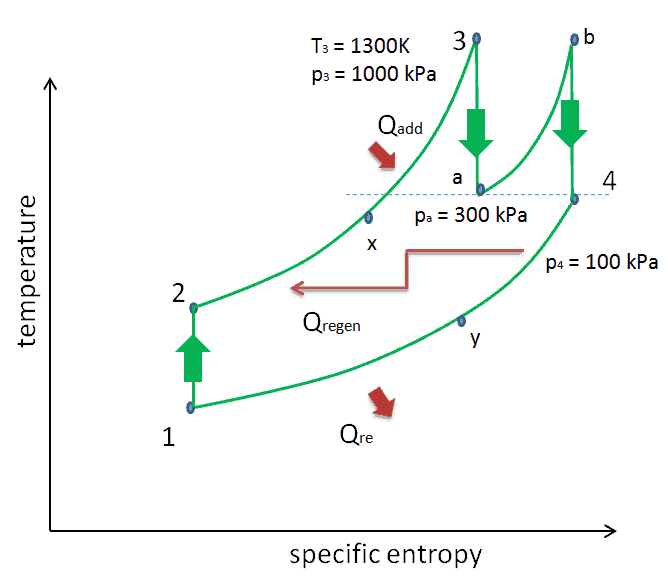
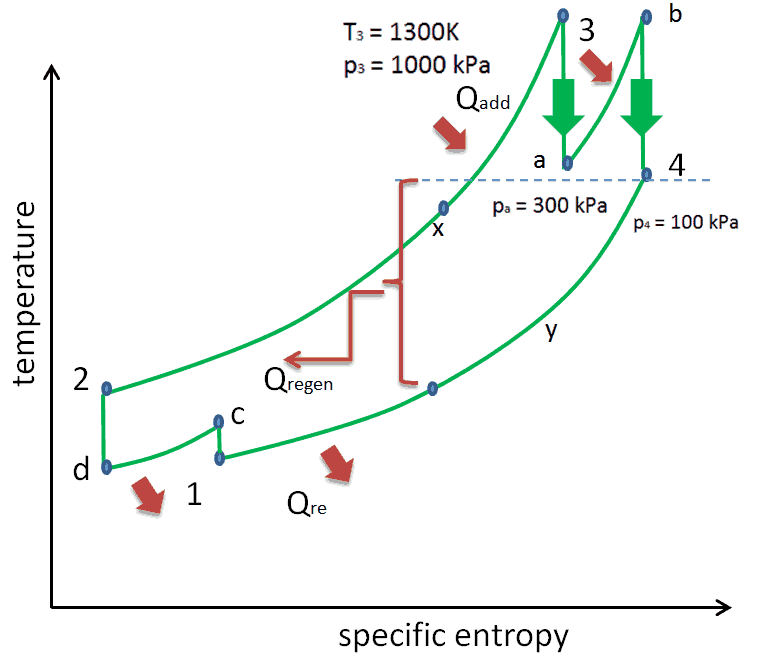
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.