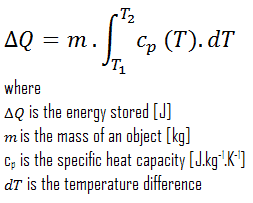Absorción de calor
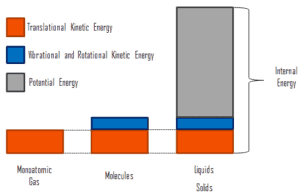 En termodinámica , la energía interna (también llamada energía térmica ) se define como la energía asociada con formas microscópicas de energía . Es una cantidad extensa , depende del tamaño del sistema o de la cantidad de sustancia que contiene. La unidad SI de energía interna es el julio (J) . Es la energía contenida dentro del sistema, excluyendo la energía cinética de movimiento del sistema como un todo y la energía potencial del sistema. Las formas microscópicas de energía incluyen aquellas debidas a la rotación , vibración, traslación e interacciones.entre las moléculas de una sustancia. Ninguna de estas formas de energía se puede medir o evaluar directamente, pero se han desarrollado técnicas para evaluar el cambio en la suma total de todas estas formas microscópicas de energía.
En termodinámica , la energía interna (también llamada energía térmica ) se define como la energía asociada con formas microscópicas de energía . Es una cantidad extensa , depende del tamaño del sistema o de la cantidad de sustancia que contiene. La unidad SI de energía interna es el julio (J) . Es la energía contenida dentro del sistema, excluyendo la energía cinética de movimiento del sistema como un todo y la energía potencial del sistema. Las formas microscópicas de energía incluyen aquellas debidas a la rotación , vibración, traslación e interacciones.entre las moléculas de una sustancia. Ninguna de estas formas de energía se puede medir o evaluar directamente, pero se han desarrollado técnicas para evaluar el cambio en la suma total de todas estas formas microscópicas de energía.
Absorción de calor
Además, la energía se puede almacenar en los enlaces químicos entre los átomos que forman las moléculas. Este almacenamiento de energía a nivel atómico incluye energía asociada con estados orbitales de electrones, espín nuclear y fuerzas de unión en el núcleo.

La energía térmica también puede ser absorbida y almacenada de manera muy efectiva. Hoy en día, la situación en los mercados energéticos es diferente. El aumento de los precios de las fuentes de energía convencional y la conciencia ambiental han contribuido a aumentar el uso de energías renovables y la eficiencia energética. El almacenamiento de energía térmica forma un componente clave de una planta de energía para mejorar su capacidad de envío, especialmente para concentrar plantas de energía solar (CSP). El almacenamiento de energía térmica (TES) se logra con tecnologías muy diferentes. Hay tres métodos utilizados y que aún se están investigando para almacenar energía térmica.
- Almacenamiento de calorías sensible (SHS)
- Almacenamiento de calor latente (LHS)
- Almacenamiento termoquímico
Absorción en calor sensible
La forma más directa es el almacenamiento de calor sensible . El almacenamiento de calor sensible se basa en elevar la temperatura de un líquido o sólido para almacenar calor y liberarlo con la disminución de temperatura cuando se requiera. Los volúmenes necesarios para almacenar energía en la escala que necesita el mundo son extremadamente grandes. Los materiales utilizados en el almacenamiento de calor sensible deben tener una alta capacidad calorífica y también un alto punto de ebullición o fusión. Aunque este método de almacenamiento de calor es actualmente menos eficaz para el almacenamiento de calor, es menos complicado en comparación con el calor latente o químico y es económico.
Desde el punto de vista termodinámico, el almacenamiento de calor sensible se basa en el aumento de entalpía del material en el almacén, ya sea líquido o sólido en la mayoría de los casos. El efecto sensible es un cambio de temperatura. El calor almacenado se puede obtener mediante la ecuación:
Absorción en calor latente
Un enfoque común para el almacenamiento de energía térmica es utilizar materiales conocidos como materiales de cambio de fase (PCM). Estos materiales almacenan calor cuando experimentan un cambio de fase , por ejemplo, de sólido a líquido, de líquido a gas o de sólido a sólido (cambio de una forma cristalina a otra sin cambio de fase física).
El cambio de fase ” sólido a líquido ” es el más utilizado, pero también es de interés el cambio de sólido a sólido. Estos materiales se pueden utilizar como una forma eficaz de almacenar energía térmica (energía solar, electricidad fuera de horas pico, calor residual industrial). En comparación con los sistemas de almacenamiento de calor sensible, el almacenamiento de calor latente tiene las ventajas de una alta densidad de almacenamiento (debido al alto calor de fusión latente ) y la naturaleza isotérmica del proceso de almacenamiento. El calor de fusión o el calor de evaporación es mucho mayor que la capacidad calorífica específica. La comparación entre el almacenamiento de calor latente y el almacenamiento de calor sensible muestra que en el almacenamiento de calor latente las densidades de almacenamiento son típicamente de 5 a 10 veces más altas.
En general, los efectos del calor latente asociados con el cambio de fase son significativos. El calor latente , también conocido como entalpía de vaporización (cambio de fase de líquido a vapor) o entalpía de fusión (cambio de fase de sólido a líquido), es la cantidad de calor que se agrega o elimina de una sustancia para producir un cambio en fase. Esta energía descompone las fuerzas de atracción intermoleculares y también debe proporcionar la energía necesaria para expandir la sustancia (el trabajo pΔV ). Cuando se agrega calor latente , no se produce ningún cambio de temperatura. [/ Lgc_column]
Absorción en energía química
Uno de los tres enfoques posibles para el almacenamiento de energía térmica es utilizar reacciones termoquímicas reversibles . La ventaja más importante del método de almacenamiento termoquímico es que la entalpía de reacción es considerablemente mayor que el calor específico o el calor de fusión. Por tanto, la densidad de almacenamiento es mucho mejor. En las reacciones químicas , la energía se almacena en los enlaces químicos entre los átomos que forman las moléculas. Almacen de energiaa nivel atómico incluye la energía asociada con los estados orbitales de los electrones. Ya sea que una reacción química absorba o libere energía, no hay un cambio general en la cantidad de energía durante la reacción. Eso se debe a la ley de conservación de la energía , que establece que:
La energía no se puede crear ni destruir . La energía puede cambiar de forma durante una reacción química .
Un ejemplo de un sistema de almacenamiento experimental basado en energía de reacción química es la tecnología de hidrato de sal . El sistema es especialmente ventajoso para el almacenamiento de energía térmica estacional . El sistema utiliza la energía de reacción creada cuando las sales se hidratan o deshidratan. Funciona almacenando calor en un recipiente que contiene una solución de hidróxido de sodio (NaOH) al 50%. El calor (por ejemplo, del uso de un colector solar) se almacena evaporando el agua en una reacción endotérmica. Cuando se agrega agua nuevamente, se libera calor en una reacción exotérmica a 50 ° C. Los sistemas actuales funcionan con una eficiencia del 60%.
Absorción de calor radiante
 En capítulos anteriores, hemos discutido la convección y la conducción , que requieren la presencia de materia como medio para llevar el calor de la región más caliente a la más fría. Pero un tercer tipo de transferencia de calor, la transferencia de calor por radiación , ocurre sin ningún medio. En general, la transferencia de calor por radiación de una superficie a otra es la radiación que sale de la primera superficie por la otra menos la que llega desde la segunda superficie. La transferencia de calor por radiación está mediada por radiación electromagnética , conocida como radiación térmica , que surge debido a la temperatura de un cuerpo.
En capítulos anteriores, hemos discutido la convección y la conducción , que requieren la presencia de materia como medio para llevar el calor de la región más caliente a la más fría. Pero un tercer tipo de transferencia de calor, la transferencia de calor por radiación , ocurre sin ningún medio. En general, la transferencia de calor por radiación de una superficie a otra es la radiación que sale de la primera superficie por la otra menos la que llega desde la segunda superficie. La transferencia de calor por radiación está mediada por radiación electromagnética , conocida como radiación térmica , que surge debido a la temperatura de un cuerpo.
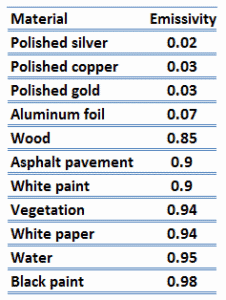
Otra propiedad de radiación importante de una superficie es su capacidad de absorción , α , que es la fracción de la energía de radiación incidente en una superficie que es absorbida por la superficie. Al igual que la emisividad, el valor de la absortividad está en el rango 0 <α <1.
Según su definición, un cuerpo negro , que es un cuerpo físico idealizado, absorbe toda la radiación electromagnética incidente , independientemente de la frecuencia o el ángulo de incidencia. Es decir, un cuerpo negro es un absorbente perfecto. Dado que para los objetos reales la absortividad es menor que la unidad, un objeto real no puede absorber toda la luz incidente. La absorción incompleta puede deberse a que parte de la luz incidente se transmite a través del cuerpo o que parte de ella se refleja en la superficie del cuerpo.
En general, la absortividad y la emisividad están interconectadas por la Ley de radiación térmica de Kirchhoff , que establece:
Para un cuerpo arbitrario que emite y absorbe radiación térmica en equilibrio termodinámico, la emisividad es igual a la absortividad.
emisividad ε = absortividad α
Tenga en cuenta que la radiación visible ocupa una banda muy estrecha del espectro de 0,4 a 0,76 nm, no podemos hacer ningún juicio sobre la negrura de una superficie sobre la base de observaciones visuales. Por ejemplo, considere el papel blanco que refleja la luz visible y, por lo tanto, parece blanco. Por otro lado, es importante negro para la radiación infrarroja ( absortividad α = 0,94 ) ya que absorben fuertemente la radiación de longitud de onda larga.