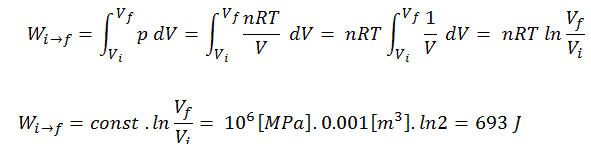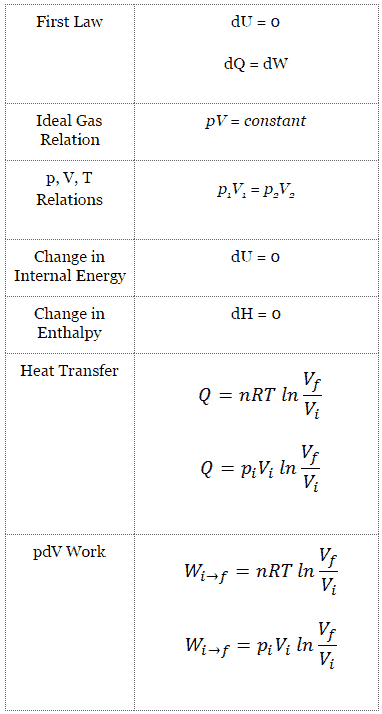Ejemplo de proceso isotérmico
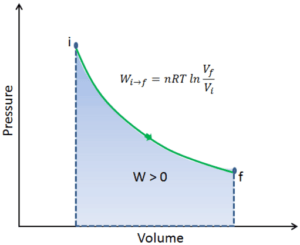
Suponga una expansión isotérmica de helio (i → f) en un pistón sin fricción (sistema cerrado). La expansión del gas es impulsada por la absorción de energía térmica Q add . El gas se expande desde el volumen inicial de 0.001 m 3 y simultáneamente la carga externa del pistón disminuye lenta y continuamente de 1 MPa a 0.5 MPa. Dado que el helio se comporta casi como un gas ideal, use la ley del gas ideal para calcular el volumen final de la cámara y luego calcule el trabajo realizado por el sistema, cuando la temperatura del gas es igual a 400 K.
Solución:
El volumen final del gas, V f , se puede calcular utilizando la relación p, V, T para el proceso isotérmico:
p i V i = p f V f ⇒ V f = p i V i / p f = 2 x 0.001 m 3 = 0.002 m 3
Para calcular tales procesos, necesitaríamos saber cómo varía la presión con el volumen para el proceso real por el cual el sistema cambia del estado i al estado f . Como durante este proceso la presión interna no fue constante, el trabajo p∆V realizado por el pistón debe calcularse utilizando la siguiente integral:
Por convención, un valor positivo para el trabajo indica que el trabajo lo realiza el sistema en su entorno. Un valor negativo indica que el trabajo se realiza en el sistema por su entorno. El trabajo pΔV es igual al área bajo la curva de proceso trazada en el diagrama de presión-volumen.
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.