Quelle est la pression
 La pression est une mesure de la force exercée par unité de surface sur les limites d’une substance. L’unité standard de pression dans le système SI est le Newton par mètre carré ou pascal (Pa) . Mathématiquement:
La pression est une mesure de la force exercée par unité de surface sur les limites d’une substance. L’unité standard de pression dans le système SI est le Newton par mètre carré ou pascal (Pa) . Mathématiquement:
p = F / A
où
- p est la pression
- F est la force normale
- A est l’aire de la frontière
Pascal est défini comme la force de 1N qui s’exerce sur la surface unitaire.
- 1 Pascal = 1 N / m 2
- 1 MPa 10 6 N / m 2
- 1 bar 10 5 N / m 2
- 1 kPa 10 3 N / m 2
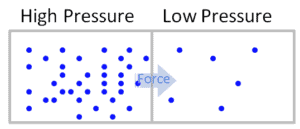
En général, la pression ou la force exercée par unité de surface sur les limites d’une substance est causée par les collisions des molécules de la substance avec les limites du système. Lorsque les molécules frappent les murs, elles exercent des forces qui tentent de pousser les murs vers l’extérieur. Les forces résultant de toutes ces collisions provoquent la pression exercée par un système sur son environnement. La pression en tant que variable intensive est constante dans un système fermé. Il n’est vraiment pertinent que dans les systèmes liquides ou gazeux.
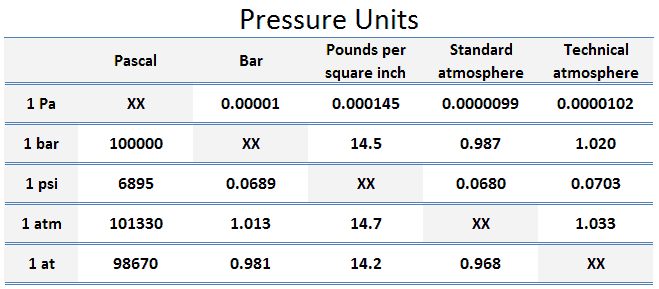
Échelles de pression – Unités de pression
Pascal – Unité de pression
Comme nous l’avons vu, l’ unité SI de pression et de contrainte est le pascal .
- 1 pascal 1 N / m 2 = 1 kg / (ms 2 )
Pascal est défini comme un newton par mètre carré. Cependant, pour la plupart des problèmes d’ingénierie, il s’agit d’une unité assez petite, il est donc pratique de travailler avec des multiples du pascal: le kPa , la barre et le MPa .
- 1 MPa 10 6 N / m 2
- 1 bar 10 5 N / m 2
- 1 kPa 10 3 N / m 2
L’unité de mesure appelée atmosphère standard ( atm ) est définie comme:
- 1 atm = 101,33 kPa
L’atmosphère standard se rapproche de la pression moyenne au niveau de la mer à 45 ° de latitude N. Notez qu’il y a une différence entre l’ atmosphère standard (atm) et l’ atmosphère technique (at).
Une atmosphère technique est une unité de pression non SI égale à un kilogramme de force par centimètre carré.
- 1 à = 98,67 kPa
Livres par pouce carré – psi
L’unité standard dans le système anglais est la livre-force par pouce carré (psi) . C’est la pression résultant d’une force d’une livre-force appliquée à une zone d’un pouce carré.
- 1 psi 1 lbf / in 2 = 4,45 N / (0,0254 m) 2 ≈ 6895 kg / m 2
Par conséquent, une livre par pouce carré équivaut à environ 6895 Pa.
L’unité de mesure appelée atmosphère standard (atm) est définie comme:
- 1 atm = 14,7 psi
L’atmosphère standard se rapproche de la pression moyenne au niveau de la mer à 45 ° de latitude N. Notez qu’il y a une différence entre l’ atmosphère standard (atm) et l’ atmosphère technique (at).
Une atmosphère technique est une unité de pression non SI égale à un kilogramme de force par centimètre carré.
- 1 at = 14,2 psi
Bar – Unité de pression
La barre est une unité de pression métrique . Il ne fait pas partie du Système international d’unités (SI). La barre est couramment utilisée dans l’ industrie et la météorologie , et un instrument utilisé en météorologie pour mesurer la pression atmosphérique est appelé baromètre.
Une barre équivaut exactement à 100 000 Pa et est légèrement inférieure à la pression atmosphérique moyenne sur Terre au niveau de la mer ( 1 bar = 0,9869 atm). La pression atmosphérique est souvent indiquée en millibars, où la pression standard au niveau de la mer est définie comme 1013 mbar, 1,013 bar ou 101,3 (kPa).
Parfois, «Bar (a)» et «bara» sont utilisés pour indiquer les pressions absolues et «bar (g)» et «barg» pour les pressions manométriques.
Pression absolue vs pression manométrique
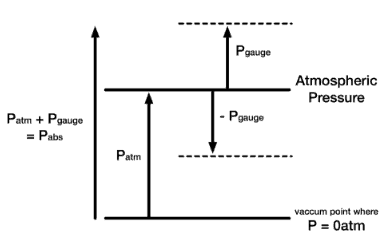 La pression décrite ci-dessus est appelée pression absolue . Souvent , il est important de faire la distinction entre pression absolue et la pression de la jauge . Dans cet article, le terme pression fait référence à la pression absolue, sauf indication contraire explicite. Mais en ingénierie, nous avons souvent affaire à des pressions, qui sont mesurées par certains appareils. Bien que les pressions absolues doivent être utilisées dans les relations thermodynamiques, les appareils de mesure de pression indiquent souvent la différence entre la pression absolue dans un système et la pression absolue de l’atmosphère existant à l’extérieur de l’appareil de mesure. Ils mesurent la pression manométrique .
La pression décrite ci-dessus est appelée pression absolue . Souvent , il est important de faire la distinction entre pression absolue et la pression de la jauge . Dans cet article, le terme pression fait référence à la pression absolue, sauf indication contraire explicite. Mais en ingénierie, nous avons souvent affaire à des pressions, qui sont mesurées par certains appareils. Bien que les pressions absolues doivent être utilisées dans les relations thermodynamiques, les appareils de mesure de pression indiquent souvent la différence entre la pression absolue dans un système et la pression absolue de l’atmosphère existant à l’extérieur de l’appareil de mesure. Ils mesurent la pression manométrique .
- Pression absolue. Lorsque la pression est mesurée par rapport à un vide parfait, elle est appelée pression absolue (psia). Les livres par pouce carré absolu (psia) sont utilisées pour indiquer clairement que la pression est relative à un vide plutôt qu’à la pression atmosphérique ambiante. Étant donné que la pression atmosphérique au niveau de la mer est d’environ 101,3 kPa (14,7 psi), cela s’ajoutera à toute lecture de pression effectuée dans l’air au niveau de la mer.
- Pression manométrique. Lorsque la pression est mesurée par rapport à la pression atmosphérique (14,7 psi), elle est appelée pression manométrique (psig). Le terme pression relative est appliqué lorsque la pression dans le système est supérieure à la pression atmosphérique locale, p atm . Cette dernière échelle de pression a été développée car presque tous les manomètres enregistrent zéro lorsqu’ils sont ouverts sur l’atmosphère. Les pressions manométriques sont positives si elles sont supérieures à la pression atmosphérique et négatives si elles sont inférieures à la pression atmosphérique.
jauge p = p absolu – p absolu; au m
- Pression atmosphérique. La pression atmosphérique est la pression dans l’air ambiant à la surface de la Terre – ou «près» de celle-ci. La pression atmosphérique varie avec la température et l’altitude au-dessus du niveau de la mer. La pression atmosphérique standard se rapproche de la pression moyenne au niveau de la mer à 45 ° de latitude nord. La pression atmosphérique standard est définie au niveau de la mer à 273 o K (0 o C) et est:
- 101325 Pa
- 1.01325 bar
- 14,696 psi
- 760 mmHg
- 760 torr
- Pression manométrique négative – Pression de vide. Lorsque la pression atmosphérique locale est supérieure à la pression dans le système, le terme pression de vide est utilisé. Un vide parfait correspondrait à une pression nulle absolue. Il est certes possible d’avoir une pression manométrique négative, mais pas possible d’avoir une pression absolue négative. Par exemple, une pression absolue de 80 kPa peut être décrite comme une pression manométrique de -21 kPa (c’est-à-dire 21 kPa en dessous d’une pression atmosphérique de 101 kPa).
p vide = p absolu; atm – p absolu
Par exemple, un pneu de voiture pompé jusqu’à 2,5 atm (36,75 psig) au-dessus de la pression atmosphérique locale (disons 1 atm ou 14,7 psia localement), aura une pression absolue de 2,5 + 1 = 3,5 atm (36,75 + 14,7 = 51,45 psia ou 36,75 psig).
En revanche, les turbines à vapeur à condensation (dans les centrales nucléaires ) évacuent la vapeur à une pression bien inférieure à la pression atmosphérique (par exemple à 0,08 bar ou 8 kPa ou 1,16 psia) et dans un état partiellement condensé. En unités relatives, il s’agit d’une pression manométrique négative d’environ – 0,92 bar, – 92 kPa ou – 13,54 psig.
Loi du gaz parfait
Toute équation qui relie la pression, la température et le volume spécifique d’une substance est appelée une équation d’état . L’ équation d’état la plus simple et la plus connue pour les substances en phase gazeuse est l’ équation d’état du gaz parfait . Émile Clapeyron l’a déclaré pour la première fois en 1834 comme une combinaison de la loi empirique de Boyle, de la loi de Charles et de la loi d’Avogadro. Cette équation prédit le comportement pvT d’un gaz de façon assez précise pour les gaz dilués ou à basse pression. Dans un gaz parfait, les molécules n’ont pas de volume et n’interagissent pas. Selon la loi du gaz parfait, la pression varie linéairement avec la température et la quantité , et inversement avec le volume .
pV = nRT
où:
- p est la pression absolue du gaz
- n est la quantité de substance
- T est la température absolue
- V est le volume
- R est la constante de gaz idéale ou universelle,égale au produit de la constante de Boltzmann et de la constante d’Avogadro,
Dans cette équation, le symbole R est une constante appelée constante de gaz universelle qui a la même valeur pour tous les gaz, à savoir R = 8,31 J / mol K.
La puissance de la loi du gaz parfait réside dans sa simplicité . Lorsque deux variables thermodynamiques, p, v et T sont données , la troisième peut être facilement trouvée. Un gaz parfait est défini comme celui dans lequel toutes les collisions entre atomes ou molécules sont parfaitement élastiques et où il n’y a pas de forces d’attraction intermoléculaires. Un gaz parfait peut être visualisé comme une collection de sphères parfaitement dures qui entrent en collision mais qui, autrement, n’interagissent pas entre elles. En réalité, aucun gaz réel n’est comme un gaz parfait et donc aucun gaz réel ne suit complètement la loi ou l’équation du gaz parfait. À des températures proches d’un point d’ébullition des gaz, une augmentation de la pression provoquera de la condensation et une diminution drastique du volume. A des pressions très élevées, les forces intermoléculaires d’un gaz sont importantes. Cependant, la plupart des gaz sont en accord approximatif à des pressions et des températures supérieures à leur point d’ébullition.
Pressions typiques en ingénierie – Exemples
Le pascal (Pa) en tant qu’unité de mesure de pression est largement utilisé dans le monde et a largement remplacé l’ unité de livres par pouce carré (psi) , sauf dans certains pays qui utilisent encore le système de mesure impérial, y compris les États-Unis. Pour la plupart des problèmes d’ingénierie, le pascal (Pa) est une unité assez petite, il est donc pratique de travailler avec des multiples du pascal: le kPa, le MPa ou la barre. La liste suivante résume quelques exemples:
- La plupart des centrales nucléaires exploitent généralement des turbines à vapeur à condensation à plusieurs étages . Ces turbines évacuent la vapeur à une pression bien inférieure à la pression atmosphérique (par exemple à 0,08 bar ou 8 kPa ou 1,16 psia) et dans un état partiellement condensé. En unités relatives, il s’agit d’une pression manométrique négative d’environ – 0,92 bar, – 92 kPa ou – 13,54 psig.
- La pression atmosphérique standard se rapproche de la pression moyenne au niveau de la mer à 45 ° de latitude nord. La pression atmosphérique standard est définie au niveau de la mer à 273 o K (0 o C) et est:
- 101325 Pa
- 1.01325 bar
- 14,696 psi
- 760 mmHg
- 760 torr
- La surpression des pneus de voiture est d’environ 2,5 bars, 0,25 MPa ou 36 psig.
- Chaudière à tube de fumée de locomotive à vapeur: 150–250 psig
- Un étage haute pression de turbine à vapeur à condensation dans une centrale nucléaire fonctionne à l’état d’équilibre avec des conditions d’entrée de 6 MPa (60 bar ou 870 psig), t = 275,6 ° C, x = 1
- Un réacteur à eau bouillante est refroidi et modéré par de l’ eau comme un REP, mais à une pression inférieure (par exemple 7 MPa, 70 bars ou 1015 psig), ce qui permet à l’eau de bouillir à l’intérieur du récipient sous pression, produisant la vapeur qui fait fonctionner les turbines.
- Les réacteurs à eau sous pression sont refroidis et modérés par de l’eau liquide à haute pression (par exemple 16 MPa, 160 bars ou 2320 psig). À cette pression, l’eau bout à environ 350 ° C (662 ° F), ce qui fournit une marge de sous-refroidissement d’environ 25 ° C.
- Le réacteur à eau supercritique (SCWR) fonctionne à pression supercritique . Le terme supercritique dans ce contexte se réfère au point critique thermodynamique de l’eau (T CR = 374 ° C; p CR = 22,1 MPa)
- Injection directe de carburant à rampe commune: sur les moteurs diesel, elle est dotée d’une rampe d’alimentation haute pression (supérieure à 1 000 bar ou 100 MPa ou 14500 psi).
Perte de pression – Fluides
Résumé de: Perte de charge – Perte de pression
- La perte de charge ou la perte de pression sont la réduction de la charge totale (somme de la charge potentielle , de la vitesse et de la pression ) d’un fluide causée par la friction présente dans le mouvement du fluide.
- La perte de charge et la perte de charge représentent le même phénomène – les pertes par frottement dans les tuyaux et les pertes dans les composants hydrauliques, mais elles sont exprimées en unités différentes .
- La perte de charge du système hydraulique est divisée en deux catégories principales :
- Perte de charge importante – due au frottement dans des tuyaux droits
- Perte de charge mineure – due à des composants comme des valves, des coudes…
-
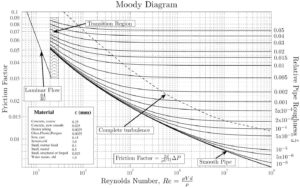
Source: Donebythesecondlaw sur Wikipédia en anglais, CC BY-SA 3.0,
https://commons.wikimedia.org/w/index.php?curid=4681366L’équation de Darcy peut être utilisée pour calculer les pertes majeures .
- Une forme spéciale de l’équation de Darcy peut être utilisée pour calculer les pertes mineures .
- Le facteur de friction pour l’écoulement du fluide peut être déterminé à l’aide d’un diagramme de Moody .
- Le facteur de friction pour l’écoulement laminaire est indépendant de la rugosité de la surface intérieure du tuyau. f = 64 / Re
- Le facteur de frottement pour un écoulement turbulent dépend fortement de la rugosité relative. Elle est déterminée par l’équation de Colebrook. Il faut noter qu’aux très grands nombres de Reynolds , le facteur de friction est indépendant du nombre de Reynolds.
- Les pertes mineures sont à peu près proportionnelle à la place du débit et par conséquent , ils peuvent être intégrés facilement dans l’équation de Darcy-Weisbach par coefficient de résistance K .
- En tant que perte de pression locale, l’accélération du fluide dans un canal chauffé peut également être envisagée.
Pression critique de l’eau
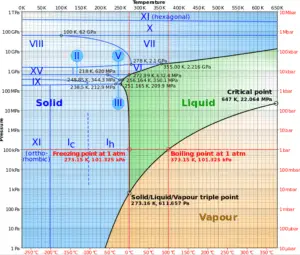
Source: wikipedia.org CC BY-SA
À une pression supérieure à la pression critique, l’ eau est dans un état spécial, appelé état fluide supercritique . Un fluide supercritique est un fluide qui est à des pressions supérieures à ses valeurs critiques thermodynamiques. Aux pressions critiques et supercritiques, un fluide est considéré comme une substance monophasée malgré le fait que toutes les propriétés thermophysiques subissent des changements importants dans les régions critiques et pseudocritiques.
Pour l’eau, les paramètres critiques sont les suivants:
- P cr = 22,09 MPa
- T cr = 374,14 ° C (ou 647,3 K)
- v cr = 0,003155 m3 / kg
- u f = u g = 2014 kJ / kg
- h f = h g = 2084 kJ / kg
- s f = s g = 4,406 kJ / kg K
Voir aussi: Point critique de l’eau
Voir aussi: Fluide supercritique
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci