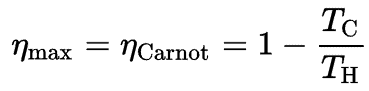Efficacité Carnot – Efficacité du moteur thermique Carnot
En 1824, Nicolas Léonard Sadi Carnot , ingénieur et physicien français, a approfondi l’étude de le deuxième principe en formant un principe (également appelé règle de Carnot ) qui définit les limites d’ efficacité maximum qu’un moteur thermique peut obtenir. En bref, ce principe stipule que l’ efficacité d’un cycle thermodynamique dépend uniquement de la différence entre les réservoirs de température chaud et froid.
Le principe de Carnot est le suivant:
- Aucun moteur ne peut être plus efficace qu’un moteur réversible ( un moteur thermique Carnot ) fonctionnant entre les mêmes réservoirs à haute et à basse température.
- Les rendements de tous les moteurs réversibles (moteurs thermiques Carnot ) fonctionnant entre les mêmes réservoirs à température constante sont les mêmes, quel que soit le principe actif utilisé ou les détails du fonctionnement.
Efficacité Carnot
La formule pour cette efficacité maximale est:
où:
- est l’efficacité du cycle Carnot, c’est-à-dire le rapport = W / Q H du travail effectué par le moteur sur l’énergie thermique entrant dans le système à partir du réservoir chaud.
- T C est la température absolue (Kelvins) du réservoir d’eau froide,
- T H est la température absolue (Kelvins) du réservoir chaud.
Exemple: efficacité de Carnot pour une centrale au charbon
Dans une centrale électrique au charbon moderne , la température de la vapeur à haute pression (T chaud ) serait d’environ 400 ° C (673 K) et T froide , la température de l’eau de la tour de refroidissement, serait d’environ 20 ° C (293 K). Pour ce type de centrale, l’efficacité maximale (idéale) sera:
= 1 – T froid / T chaud = 1 – 293/673 = 56%
Il faut l’ajouter, c’est une efficacité idéalisée . L’efficacité Carnot est valable pour les procédés réversibles. Ces processus ne peuvent pas être réalisés dans les cycles réels des centrales électriques. L’efficacité Carnot dicte que des rendements plus élevés peuvent être atteints en augmentant la température de la vapeur. Cette fonctionnalité est également valable pour les cycles thermodynamiques réels. Mais cela nécessite une augmentation des pressions à l’intérieur des chaudières ou des générateurs de vapeur . Cependant, des considérations métallurgiques imposent des limites supérieures à ces pressions. Les centrales électriques à combustibles fossiles sous-critiques, qui fonctionnent sous une pression critique (c’est-à-dire inférieure à 22,1 MPa), peuvent atteindre une efficacité de 36 à 40%. Conceptions supercritiques, qui fonctionnent à pression supercritique(c’est-à-dire supérieure à 22,1 MPa), ont des rendements d’environ 43%. Les centrales au charbon les plus efficaces et les plus complexes qui fonctionnent à des pressions «ultra critiques» (soit environ 30 MPa) et utilisent un réchauffage à plusieurs étages atteignent une efficacité d’environ 48%.
Voir aussi: Réacteur supercritique
Causes d’inefficacité
Comme cela a été discuté, une efficacité peut varier entre 0 et 1. Chaque moteur thermique est en quelque sorte inefficace. Cette inefficacité peut être attribuée à trois causes.
- Irréversibilité des processus . Il existe une limite supérieure théorique globale à l’efficacité de la conversion de la chaleur pour fonctionner dans n’importe quel moteur thermique. Cette limite supérieure est appelée efficacité Carnot . Selon le principe Carnot , aucun moteur ne peut être plus efficace qu’un moteur réversible ( un moteur thermique Carnot ) fonctionnant entre les mêmes réservoirs haute température et basse température. Par exemple, lorsque le réservoir chaud a T chaud de 400 ° C (673 K) et T froid d’environ 20 ° C (293 K), l’efficacité maximale (idéale) sera: = 1 – T froid / T chaud = 1 – 293 / 673 = 56%. Mais tous les processus thermodynamiques réels sont en quelque sorte irréversibles. Ils ne se font pas infiniment lentement. Par conséquent, les moteurs thermiques doivent avoir des rendements inférieurs aux limites de leur rendement en raison de l’irréversibilité inhérente du cycle du moteur thermique qu’ils utilisent.
- Présence de friction et de pertes de chaleur. Dans les systèmes thermodynamiques réels ou dans les moteurs thermiques réels, une partie de l’inefficacité globale du cycle est due aux pertes des composants individuels. Dans les appareils réels (tels que les turbines, les pompes et les compresseurs), un frottement mécanique , des pertes de chaleur et des pertes dans le processus de combustion entraînent des pertes d’efficacité supplémentaires.
- Inefficacité de la conception . Enfin, la dernière et aussi importante source d’inefficacité provient des compromis faits par les ingénieurs lors de la conception d’un moteur thermique (par exemple une centrale électrique). Ils doivent tenir compte des coûts et d’autres facteurs dans la conception et le fonctionnement du cycle. À titre d’exemple, considérons la conception du condenseur dans les centrales thermiques. Idéalement, la vapeur évacuée dans le condenseur n’aurait pas de sous-refroidissement . Mais les vrais condenseurs sont conçus pour sous-refroidir le liquide de quelques degrés Celsius afin d’éviter la cavitation d’aspiration dans les pompes à condensats. Mais, ce sous-refroidissement augmente l’inefficacité du cycle, car plus d’énergie est nécessaire pour réchauffer l’eau.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci