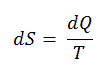Unidades de Entropia
O SI unidade de entropia é J / K . Segundo Clausius, a entropia foi definida através da mudança na entropia S de um sistema. A mudança na entropia S, quando uma quantidade de calor Q é adicionada a ela por um processo reversível a temperatura constante, é dada por:
Aqui Q é a energia transferida como calor para ou do sistema durante o processo e T é a temperatura do sistema em Kelvins durante o processo. Se assumirmos um processo isotérmico reversível , a alteração total da entropia é dada por:
∆S = S 2 – S 1 = Q / T
Nesta equação, o quociente Q / T está relacionado ao aumento do distúrbio. Uma temperatura mais alta significa maior aleatoriedade de movimento. Em temperaturas mais baixas, a adição de calor Q causa um aumento fracionário substancial no movimento molecular e na aleatoriedade. Por outro lado, se a substância já estiver quente, a mesma quantidade de calor Q adiciona relativamente pouco ao maior movimento molecular.
Exemplo: alteração de entropia no gelo derretido
Calcule a variação na entropia de 1 kg de gelo a 0 ° C, quando derretida reversivelmente em água a 0 ° C.
Por se tratar de um processo isotérmico, podemos usar:
∆S = S 2 – S 1 = Q / T
portanto, a alteração da entropia será:
∆S = 334 [kJ] / 273,15 [K] = 1,22 [kJ / K]
onde são necessários 334 quilojoules de calor para derreter 1 kg de gelo (calor latente de fusão = 334 kJ / kg) e esse calor é transferido para o sistema a 0 ° C (273,15 K).
Entropia específica
A entropia pode ser transformada em uma variável intensiva ou específica dividindo-se pela massa. Os engenheiros usam mais a entropia específica na análise termodinâmica do que a própria entropia. A entropia específica de uma substância é a sua entropia por unidade de massa. É igual à entropia total (S) dividida pela massa total (m).
s = S / m
Onde:
s = entropia específica (J / kg)
S = entropia (J)
m = massa (kg)
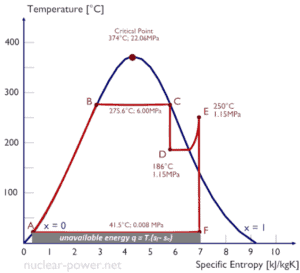
A entropia quantifica a energia de uma substância que não está mais disponível para realizar um trabalho útil. Como a entropia diz muito sobre a utilidade de uma quantidade de calor transferida na execução do trabalho, as tabelas de vapor incluem valores de entropia específica (s = S / m) como parte das informações tabuladas.
Em geral, a entropia específica é uma propriedade de uma substância, como pressão, temperatura e volume, mas não pode ser medida diretamente. Normalmente, a entropia de uma substância é dada com relação a algum valor de referência. Por exemplo, a entropia específica de água ou vapor é dada usando a referência de que a entropia específica da água é zero a 0,01 ° C e pressão atmosférica normal , onde s = 0,00 kJ / kg. O fato de o valor absoluto da entropia específica ser desconhecido não é um problema, no entanto, porque é a mudança na entropia específica (∆s) e não o valor absoluto que é importante nos problemas práticos.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.