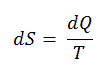Unidades de entropía
El SI unidad para la entropía es J / K . Según Clausius, la entropía se definió mediante el cambio en la entropía S de un sistema. El cambio en la entropía S, cuando se le agrega una cantidad de calor Q mediante un proceso reversible a temperatura constante, viene dado por:
Aquí Q es la energía transferida como calor hacia o desde el sistema durante el proceso, y T es la temperatura del sistema en grados Kelvin durante el proceso. Si suponemos un proceso isotérmico reversible , el cambio de entropía total viene dado por:
∆S = S 2 – S 1 = Q / T
En esta ecuación, el cociente Q / T está relacionado con el aumento del desorden. Mayor temperatura significa mayor aleatoriedad de movimiento. A temperaturas más bajas, la adición de calor Q provoca un aumento fraccional sustancial en el movimiento molecular y la aleatoriedad. Por otro lado, si la sustancia ya está caliente, la misma cantidad de calor Q agrega relativamente poco al mayor movimiento molecular.
Ejemplo: cambio de entropía en el hielo derretido
Calcule el cambio en la entropía de 1 kg de hielo a 0 ° C, cuando se derrite reversiblemente en agua a 0 ° C.
Dado que es un proceso isotérmico, podemos usar:
∆S = S 2 – S 1 = Q / T
por lo tanto, el cambio de entropía será:
∆S = 334 [kJ] / 273.15 [K] = 1.22 [kJ / K]
donde se requieren 334 kilojulios de calor para derretir 1 kg de hielo (calor de fusión latente = 334 kJ / kg) y este calor se transfiere al sistema a 0 ° C (273,15 K).
Entropía Específica
La entropía se puede convertir en una variable intensiva o específica dividiéndola por la masa. Los ingenieros usan la entropía específica en el análisis termodinámico más que la entropía misma. La entropía específica (s) de una sustancia es su entropía por unidad de masa. Es igual a la entropía total (S) dividida por la masa total (m).
s = S / m
dónde:
s = entropía específica (J / kg)
S = entropía (J)
m = masa (kg)
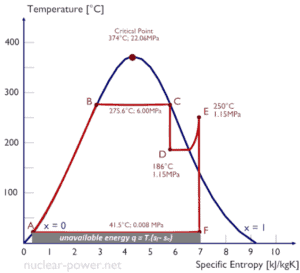
La entropía cuantifica la energía de una sustancia que ya no está disponible para realizar un trabajo útil. Debido a que la entropía dice mucho acerca de la utilidad de una cantidad de calor transferida en la realización del trabajo, las tablas de vapor incluyen valores de entropía específica (s = S / m) como parte de la información tabulada.
En general, la entropía específica es una propiedad de una sustancia, como la presión, la temperatura y el volumen, pero no se puede medir directamente. Normalmente, la entropía de una sustancia se da con respecto a algún valor de referencia. Por ejemplo, la entropía específica de agua o vapor se da usando la referencia de que la entropía específica del agua es cero a 0.01 ° C y presión atmosférica normal , donde s = 0.00 kJ / kg. Sin embargo, el hecho de que se desconozca el valor absoluto de la entropía específica no es un problema, porque es el cambio en la entropía específica (∆s) y no el valor absoluto lo que es importante en los problemas prácticos.
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.