 Bei der Kondensation sind die mit dem Phasenwechsel verbundenen latenten Wärmeeffekte ähnlich wie beim Sieden signifikant, jedoch in umgekehrter Reihenfolge. Es ist zu beachten, dass die Kondensationsenthalpie (oder Kondensationswärme ) definitionsgemäß gleich der Verdampfungsenthalpie mit dem entgegengesetzten Vorzeichen ist. Latente Wärme ist die Wärmemenge, die einer Substanz hinzugefügt oder von ihr entfernt wird, um eine Phasenänderung zu bewirken. Während der Verdampfung zerlegt diese Energie die intermolekularen Anziehungskräfte und muss auch die Energie liefern, die zur Expansion des Gases erforderlich ist (die pΔV-Arbeit ). Wenn latente Wärme hinzugefügt oder entfernt wird, tritt keine Temperaturänderung auf. Die Verdampfungsenthalpie ist eine Funktion des Drucks, bei dem diese Umwandlung stattfindet.
Bei der Kondensation sind die mit dem Phasenwechsel verbundenen latenten Wärmeeffekte ähnlich wie beim Sieden signifikant, jedoch in umgekehrter Reihenfolge. Es ist zu beachten, dass die Kondensationsenthalpie (oder Kondensationswärme ) definitionsgemäß gleich der Verdampfungsenthalpie mit dem entgegengesetzten Vorzeichen ist. Latente Wärme ist die Wärmemenge, die einer Substanz hinzugefügt oder von ihr entfernt wird, um eine Phasenänderung zu bewirken. Während der Verdampfung zerlegt diese Energie die intermolekularen Anziehungskräfte und muss auch die Energie liefern, die zur Expansion des Gases erforderlich ist (die pΔV-Arbeit ). Wenn latente Wärme hinzugefügt oder entfernt wird, tritt keine Temperaturänderung auf. Die Verdampfungsenthalpie ist eine Funktion des Drucks, bei dem diese Umwandlung stattfindet.
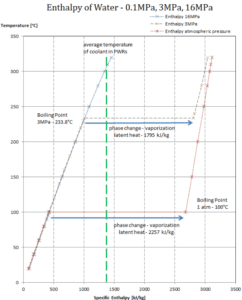
Latente Kondensationswärme – Wasser mit 0,1 MPa (atmosphärischer Druck)
h lg = – 2.257 kJ / kg
Latente Kondensationswärme – Wasser bei 3 MPa
h lg = – 1795 kJ / kg
Latente Kondensationswärme – Wasser bei 16 MPa (Druck in einem Druckhalter )
h lg = – 931 kJ / kg
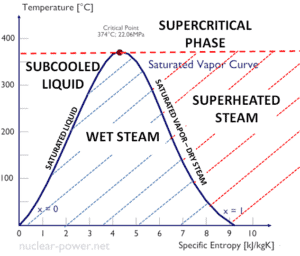
Die Kondensationswärme nimmt mit zunehmendem Druck ab, der Siedepunkt steigt an. Es verschwindet vollständig an einem bestimmten Punkt, der als kritischer Punkt bezeichnet wird . Oberhalb des kritischen Punktes sind die Flüssigkeits- und Dampfphase nicht zu unterscheiden, und die Substanz wird als überkritisches Fluid bezeichnet .
Die Kondensationswärme ist die Wärme, die freigesetzt wird, um eine Einheit gesättigten Dampfes vollständig zu leiten, und entspricht – h lg = h l – h g .
Die Wärme, die zum Schmelzen (oder Einfrieren) einer Masseeinheit an dem Stoff bei konstantem Druck erforderlich ist, ist die Schmelzwärme und entspricht h sl = h l – h s , wobei h s die Enthalpie von gesättigtem Feststoff und h l ist ist die Enthalpie einer gesättigten Flüssigkeit.
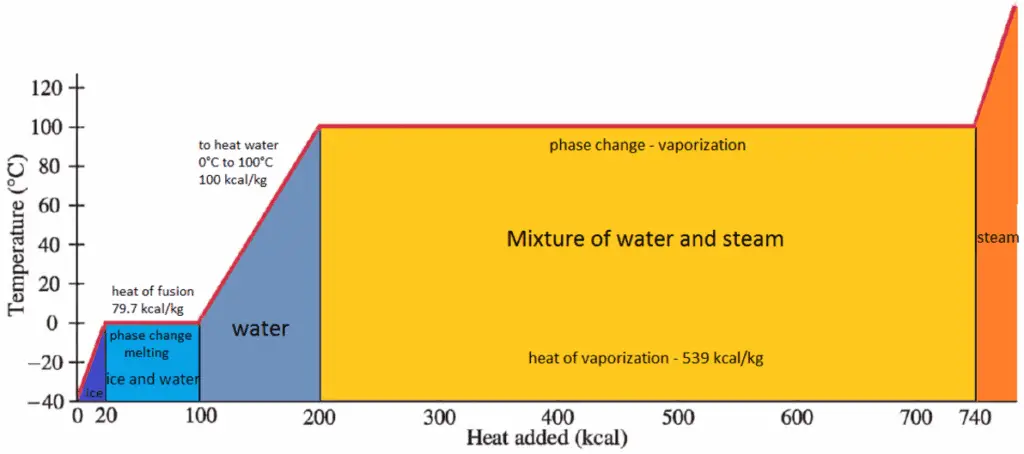 Latente Verdampfungswärme – Wasser mit 0,1 MPa. Dominanter Teil der aufgenommenen Wärme.
Latente Verdampfungswärme – Wasser mit 0,1 MPa. Dominanter Teil der aufgenommenen Wärme.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.