Sättigung
 In der Thermodynamik definiert der Begriff Sättigung einen Zustand, in dem ein Gemisch aus Dampf und Flüssigkeit bei einer gegebenen Temperatur und einem gegebenen Druck zusammen existieren kann. Die Temperatur, bei der bei einem bestimmten Druck die Verdampfung (Siedetemperatur) einsetzt, wird als Sättigungstemperatur oder Siedepunkt bezeichnet . Der Druck, bei dem bei einer bestimmten Temperatur die Verdampfung (das Sieden) einsetzt, wird als Sättigungsdruck bezeichnet.
In der Thermodynamik definiert der Begriff Sättigung einen Zustand, in dem ein Gemisch aus Dampf und Flüssigkeit bei einer gegebenen Temperatur und einem gegebenen Druck zusammen existieren kann. Die Temperatur, bei der bei einem bestimmten Druck die Verdampfung (Siedetemperatur) einsetzt, wird als Sättigungstemperatur oder Siedepunkt bezeichnet . Der Druck, bei dem bei einer bestimmten Temperatur die Verdampfung (das Sieden) einsetzt, wird als Sättigungsdruck bezeichnet.
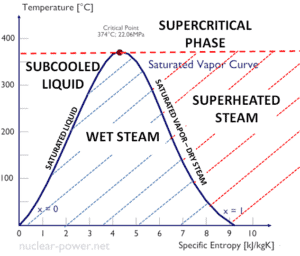
Wenn die Dampfqualität gleich 0 ist, wird dies als gesättigter flüssiger Zustand (einphasig) bezeichnet. Wenn andererseits die Dampfqualität gleich 1 ist, wird dies als gesättigter Dampfzustand oder trockener Dampf (einphasig) bezeichnet. Zwischen diesen beiden Zuständen spricht man von Dampf-Flüssigkeits-Gemisch oder Nassdampf (Zweiphasengemisch). Bei konstantem Druck ändert eine Energiezugabe nicht die Temperatur des Gemisches, sondern die Dampfqualität und das spezifische Volumen.
Zum Beispiel: Im Druckbeaufschlagungsgerät von Druckwasserreaktoren beträgt die Sättigungstemperatur etwa 350 ° C, dies entspricht jedoch dem Druck von 16,4 MPa, der im Primärkreislauf aufrechterhalten werden muss. Für eine reine Substanz besteht ein eindeutiger Zusammenhang zwischen Sättigungsdruck und Sättigungstemperatur. Je höher der Druck, desto höher die Sättigungstemperatur. Die grafische Darstellung dieser Beziehung zwischen Temperatur und Druck bei gesättigten Bedingungen wird als Dampfdruckkurve bezeichnet und ist im Phasendiagramm von Wasser zu sehen . Dieses Diagramm ist in der Abbildung dargestellt.
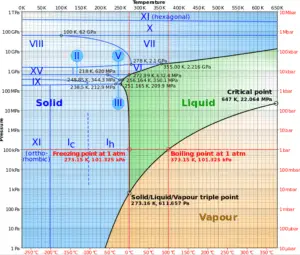
Quelle: wikipedia.org CC BY-SA
Wie aus dem Phasendiagramm von Wasser ersichtlich ist, wird in den Zweiphasenbereichen (z. B. an der Grenze der Dampf- / Flüssigphasen) durch alleinige Angabe der Temperatur der Druck und durch Angabe des Drucks die Temperatur eingestellt.
- Die Sättigungsdampfkurve ist die Kurve, die den Zweiphasenzustand und den überhitzten Dampfzustand im Ts-Diagramm trennt .
- Die Sättigungsflüssigkeitskurve ist die Kurve, die den unterkühlten Flüssigkeitszustand und den Zweiphasenzustand im Ts-Diagramm trennt .
Spezifische Enthalpie von Nassdampf
Die spezifische Enthalpie von gesättigtem flüssigem Wasser (x = 0) und trockenem Dampf (x = 1) kann aus Dampftabellen entnommen werden. Bei feuchtem Dampf kann die tatsächliche Enthalpie mit der Dampfqualität x und den spezifischen Enthalpien von gesättigtem flüssigem Wasser und trockenem Dampf berechnet werden :
h nass = h s x + (1 – x) h l
wo
h nass = Enthalpie des feuchten Dampfes (J / kg)
h s = Enthalpie von “trockenem” Dampf (J / kg)
h l = Enthalpie von gesättigtem flüssigem Wasser (J / kg)
Wie zu sehen ist, hat nasser Dampf immer eine geringere Enthalpie als trockener Dampf.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.