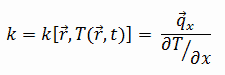Wärmeenergie und Wärme
Wärmeenergie und Wärme
Während sich Wärmeenergie auf die Gesamtenergie aller Moleküle im Objekt bezieht, ist Wärme die Energiemenge, die aufgrund ihres Temperaturunterschieds spontan von einem Körper zum anderen fließt . Wärme ist eine Energieform, aber es ist Energie auf der Durchreise . Wärme ist keine Eigenschaft eines Systems. Die Energieübertragung als Wärme erfolgt jedoch auf molekularer Ebene aufgrund eines Temperaturunterschieds .
Stellen Sie sich einen Metallblock bei hoher Temperatur vor, der aus Atomen besteht, die stark um ihre durchschnittliche Position schwingen. Bei niedrigen Temperaturen schwingen die Atome weiter, jedoch mit geringerer Intensität . Wenn ein heißerer Metallblock mit einem kühleren Block in Kontakt gebracht wird, geben die stark schwingenden Atome am Rand des heißeren Blocks ihre kinetische Energie an die weniger schwingenden Atome am Rand des kühlen Blocks ab. In diesem Fall findet zwischen diesen beiden Blöcken ein Energietransfer statt , und durch diese zufälligen Vibrationen fließt Wärme vom heißeren zum kühleren Block.
Unterscheidung von Temperatur, Wärme und Wärmeenergie
Mit Hilfe der kinetischen Theorie können diese drei Eigenschaften klar unterschieden werden.
- Die Temperatur hängt mit den kinetischen Energien der Moleküle eines Materials zusammen. Es ist die durchschnittliche kinetische Energie einzelner Moleküle.
- Interne Energie bezieht sich auf die Gesamtenergie aller Moleküle im Objekt. Es ist eine weitreichende Eigenschaft , wenn zwei gleichgewichtige heiße Stahlblöcke dieselbe Temperatur haben, aber zwei von ihnen doppelt so viel innere Energie haben wie einer.
- Schließlich ist Wärme die Energiemenge, die aufgrund ihres Temperaturunterschieds spontan von einem Körper zum anderen fließt.
Es muss hinzugefügt werden, wenn eine Temperaturdifferenz vorliegt, die Wärme spontan vom wärmeren zum kälteren System strömt . Wenn also ein 5 kg-Stahlwürfel bei 100 ° C mit einem 500 kg-Stahlwürfel bei 20 ° C in Kontakt gebracht wird, fließt Wärme von dem Würfel bei 300 ° C zu dem Würfel bei 20 ° C, obwohl die innere Energie der 20 ° C Würfel ist viel größer, weil es so viel mehr davon gibt.
Ein besonders wichtiges Konzept ist das thermodynamische Gleichgewicht . Wenn zwei Objekte in thermischen Kontakt gebracht werden , fließt im Allgemeinen Wärme zwischen ihnen, bis sie sich im Gleichgewicht befinden .
Mikroskopische Energie
Wärmeenergie – Definition
Interne Energie beinhaltet Energie im mikroskopischen Maßstab . Es kann in mikroskopische potentielle Energie, U- Pot und mikroskopische kinetische Energie, U- Kin , Komponenten unterteilt werden:
U = U Topf + U Kin
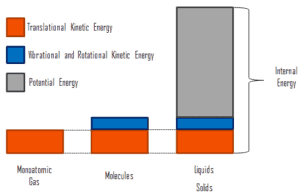 wobei die mikroskopische kinetische Energie U kin die Bewegungen aller Partikel des Systems in Bezug auf den Schwerpunktrahmen umfasst. Für ein ideales einatomiges Gas ist dies nur die translatorische kinetische Energie der linearen Bewegung der Atome. Monoatomare Partikel drehen oder vibrieren nicht. Das Verhalten des Systems wird durch die kinetische Theorie der Gase gut beschrieben. Die kinetische Theorie basiert auf der Tatsache, dass während einer elastischen Kollision zwischen einem Molekül mit hoher kinetischer Energie und einem Molekül mit niedriger kinetischer Energie ein Teil der Energie auf das Molekül mit niedriger kinetischer Energie übertragen wird. Für mehratomige Gase gibt es jedoch Rotations- undauch kinetische Schwingungsenergie .
wobei die mikroskopische kinetische Energie U kin die Bewegungen aller Partikel des Systems in Bezug auf den Schwerpunktrahmen umfasst. Für ein ideales einatomiges Gas ist dies nur die translatorische kinetische Energie der linearen Bewegung der Atome. Monoatomare Partikel drehen oder vibrieren nicht. Das Verhalten des Systems wird durch die kinetische Theorie der Gase gut beschrieben. Die kinetische Theorie basiert auf der Tatsache, dass während einer elastischen Kollision zwischen einem Molekül mit hoher kinetischer Energie und einem Molekül mit niedriger kinetischer Energie ein Teil der Energie auf das Molekül mit niedriger kinetischer Energie übertragen wird. Für mehratomige Gase gibt es jedoch Rotations- undauch kinetische Schwingungsenergie .
Die mikroskopische potentielle Energie U pot beinhaltet die chemischen Bindungen zwischen den Atomen, aus denen die Moleküle bestehen, die Bindungskräfte im Kern und auch die physikalischen Kraftfelder innerhalb des Systems (z. B. elektrische oder magnetische Felder).
In Flüssigkeiten und Feststoffen gibt es einen signifikanten Anteil der potentiellen Energie, die mit den intermolekularen Anziehungskräften verbunden ist .
Wärmeleitfähigkeit
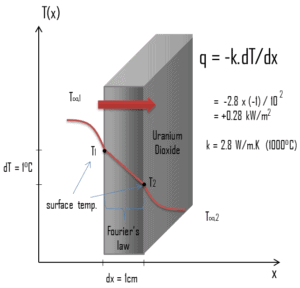 Die Wärmeübertragungseigenschaften eines festen Materials werden durch eine Eigenschaft gemessen, die als Wärmeleitfähigkeit k (oder λ) bezeichnet wird und in W / mK gemessen wird . Es ist ein Maß für die Fähigkeit eines Stoffes, Wärme durch Wärmeleitung durch ein Material zu übertragen. Beachten Sie, dass das Fourier-Gesetz für alle Materie gilt, unabhängig von ihrem Zustand (fest, flüssig oder gasförmig). Daher gilt es auch für Flüssigkeiten und Gase.
Die Wärmeübertragungseigenschaften eines festen Materials werden durch eine Eigenschaft gemessen, die als Wärmeleitfähigkeit k (oder λ) bezeichnet wird und in W / mK gemessen wird . Es ist ein Maß für die Fähigkeit eines Stoffes, Wärme durch Wärmeleitung durch ein Material zu übertragen. Beachten Sie, dass das Fourier-Gesetz für alle Materie gilt, unabhängig von ihrem Zustand (fest, flüssig oder gasförmig). Daher gilt es auch für Flüssigkeiten und Gase.
Die Wärmeleitfähigkeit der meisten Flüssigkeiten und Feststoffe variiert mit der Temperatur. Bei Dämpfen kommt es auch auf den Druck an. Allgemein:
Die meisten Materialien sind nahezu homogen, daher können wir normalerweise k = k (T) schreiben . Ähnliche Definitionen sind mit Wärmeleitfähigkeiten in y- und z-Richtung (k y , k z ) verbunden, aber für ein isotropes Material ist die Wärmeleitfähigkeit unabhängig von der Übertragungsrichtung, k x = k y = k z = k.
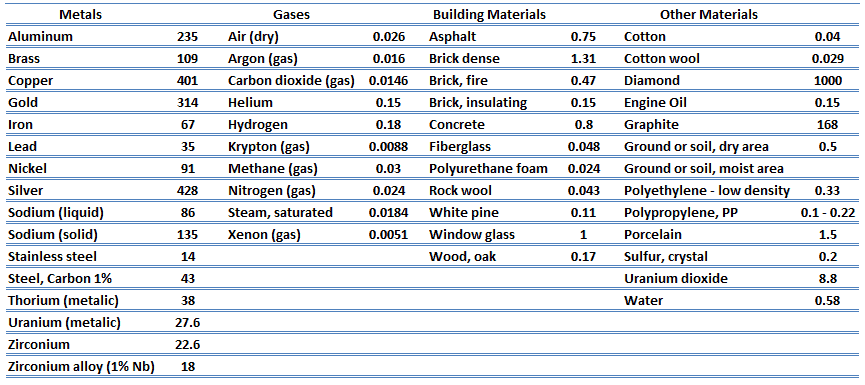
Aus der vorstehenden Gleichung folgt, dass der Wärmeleitungsfluss mit zunehmender Wärmeleitfähigkeit zunimmt und mit zunehmender Temperaturdifferenz zunimmt. Im Allgemeinen ist die Wärmeleitfähigkeit eines Feststoffs größer als die einer Flüssigkeit, die größer als die eines Gases ist. Dieser Trend ist hauptsächlich auf Unterschiede im intermolekularen Abstand für die beiden Materiezustände zurückzuführen. Insbesondere hat Diamant die höchste Härte und Wärmeleitfähigkeit aller Schüttgüter.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.