Échelles de température
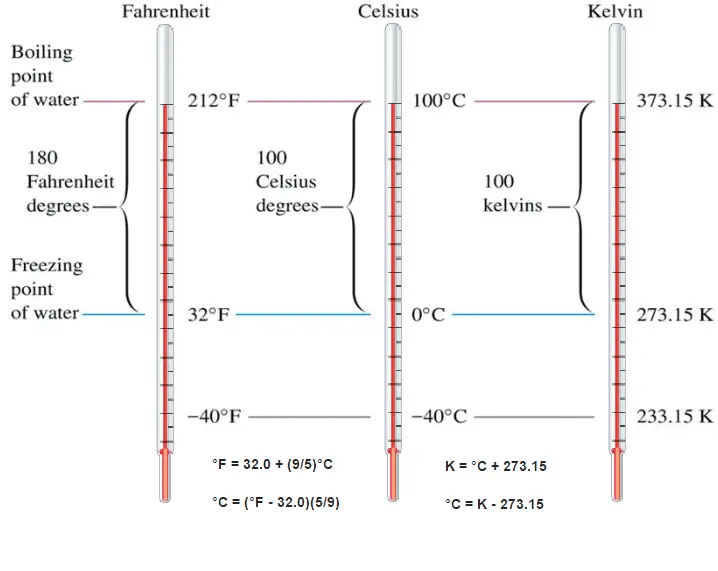 Lors de l’utilisation d’un thermomètre, nous devons marquer une échelle sur la paroi du tube avec des chiffres. Nous devons définir une échelle de température . Une échelle de température est un moyen de mesurer la température par rapport à un point de départ (0 ou zéro) et à une unité de mesure .
Lors de l’utilisation d’un thermomètre, nous devons marquer une échelle sur la paroi du tube avec des chiffres. Nous devons définir une échelle de température . Une échelle de température est un moyen de mesurer la température par rapport à un point de départ (0 ou zéro) et à une unité de mesure .
Ces chiffres sont arbitraires et, historiquement, de nombreux systèmes différents ont été utilisés. Par exemple, cela a été réalisé en définissant certaines occurrences physiques à des températures données, telles que les points de congélation et d’ ébullition de l’eau , et en les définissant respectivement à 0 et 100.
Il existe plusieurs échelles et unités pour mesurer la température. Les plus courants sont:
Zéro absolu
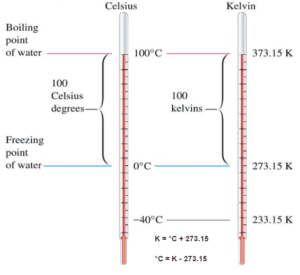
L’ échelle de température absolue qui correspond à l’échelle Celsius est appelée l’échelle Kelvin (K), et l’échelle absolue qui correspond à l’échelle Fahrenheit est appelée l’échelle Rankine (R). Les points zéro sur les deux échelles absolues représentent le même état physique. Les relations entre les échelles de température absolue et relative sont illustrées dans les équations suivantes.
Kelvin – Celsius
K = ° C + 273,15
° C = K – 273,15
Rankine – Fahrenheit
R = ° F + 460
° F = R – 460
Zéro absolu
Une telle échelle a pour point zéro . La température théorique la plus froide est appelée zéro absolu , à laquelle le mouvement thermique des atomes et des molécules atteint son minimum. Il s’agit d’un état dans lequel l’enthalpie et l’entropie d’un gaz parfait refroidi atteint sa valeur minimale, prise à 0. Classiquement , ce serait un état d’ immobilité , mais l’ incertitude quantique dicte que les particules possèdent toujours une énergie finie au point zéro . Le zéro absolu est noté 0 K sur l’échelle Kelvin, −273,15 ° C sur l’échelle Celsius et −459,67 ° F sur l’échelle Fahrenheit.
Zéro absolu et troisième loi de la thermodynamique
La troisième loi de la thermodynamique stipule:
L’entropie d’un système se rapproche d’une valeur constante lorsque la température approche du zéro absolu.
Sur la base de preuves empiriques, cette loi stipule que l’entropie d’une substance cristalline pure est nulle au zéro absolu de la température, 0 K et qu’il est impossible, par quelque procédé que ce soit, idéalisé, de réduire la température d’un système au zéro absolu en un nombre fini d’étapes. Cela nous permet de définir un point zéro pour l’énergie thermique d’un corps.
Température artificielle la plus basse
Selon Guiness World Records, la température artificielle la plus basse atteinte à ce jour est de 450 picokelvins au-dessus du zéro absolu (seulement un demi-milliardième de degré au-dessus du zéro absolu). Il a été réalisé par une équipe de scientifiques du Massachusetts Institute of Technology, Cambridge, Massachusetts, USA.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci