Direção de Processos Termodinâmicos
 Muitos processos termodinâmicos procedem naturalmente em uma direção, mas não o contrário. Por exemplo, quando existe uma diferença de temperatura , o calor flui espontaneamente do sistema mais quente para o sistema mais frio , nunca o contrário. De fato, esse fluxo de calor (de um corpo mais frio para um sistema mais quente) não violaria a primeira lei da termodinâmica , ou seja, a energia seria conservada. Mas isso não acontece na natureza.
Muitos processos termodinâmicos procedem naturalmente em uma direção, mas não o contrário. Por exemplo, quando existe uma diferença de temperatura , o calor flui espontaneamente do sistema mais quente para o sistema mais frio , nunca o contrário. De fato, esse fluxo de calor (de um corpo mais frio para um sistema mais quente) não violaria a primeira lei da termodinâmica , ou seja, a energia seria conservada. Mas isso não acontece na natureza.
Por exemplo, queimar gasolina para abastecer carros é um processo de conversão de energia em que confiamos. A energia química da gasolina é convertida em energia térmica , que é convertida em energia mecânica que faz o carro se mover. A energia mecânica foi convertida em energia cinética . Quando usamos os freios para parar um carro, essa energia cinética é convertida por fricção de volta ao calor, ou energia térmica . Nesta direção inversa, existem muitos dispositivos que convertem parcialmente o calor em energia mecânica. Mas você não pode construir uma máquina que converta calor completamente em energia mecânica. Sempre haverá perdas significativas de energia.
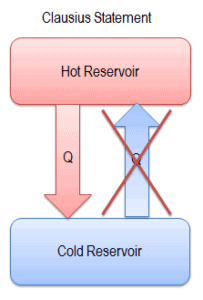
As direções dos processos termodinâmicos estão sujeitas à segunda lei da termodinâmica, especialmente à Declaração Clausius da Segunda Lei .
“É impossível construir um dispositivo que opere em um ciclo e cujo único efeito seja a transferência de calor de um corpo mais frio para um corpo mais quente”.
O calor não pode fluir espontaneamente do sistema frio para o sistema quente sem que seja executado trabalho externo no sistema. É exatamente isso que os refrigeradores e bombas de calor realizam. Em uma geladeira, o calor flui do frio para o quente, mas somente quando forçado por um trabalho externo, as geladeiras são acionadas por motores elétricos que exigem trabalho de seu entorno para operar.
As declarações Clausius e Kelvin-Planck demonstraram ser equivalentes.