Beispiele
Sublimation
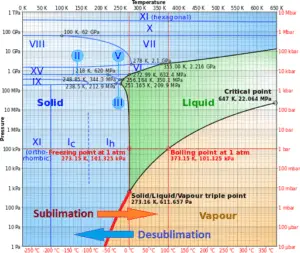
Im Allgemeinen ist Sublimation eine Phasenänderung einer Substanz direkt von der festen in die Gasphase, ohne die flüssige Zwischenphase zu durchlaufen. Sublimation ist eine endotherme Phasenänderung , die bei Temperaturen und Drücken unterhalb des Tripelpunkts einer Substanz in ihrem Phasendiagramm auftritt .
Betrachten Sie das Eis bei -10 ° C und einem Druck von 500 Pa. In diesem Fall führt die Wärmeübertragung auf das Eis zunächst zu einem Temperaturanstieg auf -8 ° C. Zu diesem Zeitpunkt geht das Eis jedoch in dem als Sublimation bekannten Prozess direkt von der festen Phase in die Dampfphase über. Die entsprechende Wärme heißt Sublimationswärme L s . Eine weitere Wärmeübertragung würde zu einer Überhitzung des Dampfes führen.
Da Sublimation eine endotherme Phasenänderung ist, benötigt sie zusätzliche Energie. Diese zusätzliche benötigte Energie kann durch Addition der Schmelzenthalpie und der Verdampfungsenthalpie berechnet werden und wird als Sublimationsenthalpie (auch Sublimationswärme genannt) bezeichnet.
Bei einigen Substanzen ist die Sublimation viel einfacher als das Verdampfen aus der Schmelze. Es hängt von ihrem Tripelpunkt ab. Wenn der Druck seines Tripelpunkts zu hoch ist, ist es schwierig, sie als Flüssigkeiten zu erhalten.
Der umgekehrte Prozess der Sublimation ist die Desublimation, bei der eine Substanz direkt von einem Gas in eine feste Phase übergeht.
Desublimation

Im Allgemeinen ist Desublimation (oder Abscheidung ) ein Phasenübergang einer Substanz direkt von der Gasphase in die feste Phase, ohne die flüssige Zwischenphase zu durchlaufen. Desublimation ist eine exotherme Phasenänderung , die bei Temperaturen und Drücken tritt unterhalb einer Substanz des Tripelpunktes in ihrem Phasendiagramm.
Betrachten Sie den Wasserdampf bei -5 ° C und einem Druck von 500 Pa. In diesem Fall führt der Dampf zu einer Temperatursenkung auf -8 ° C, wenn dem Wasserdampf Wärme entzogen wird. Zu diesem Zeitpunkt gelangt der Dampf jedoch in dem als Desublimation bekannten Prozess direkt von der Gasphase in die feste Phase. Die entsprechende Wärme heißt Sublimationswärme L s .
Da Desublimation eine exotherme Phasenänderung ist, setzt sie Energie frei. Diese freigesetzte Energie kann durch Addition der Schmelzenthalpie und der Verdampfungsenthalpie berechnet werden und wird als Sublimationsenthalpie (auch Sublimationswärme genannt) bezeichnet.
Bei einigen Substanzen ist die Desublimation viel einfacher als das Durchlaufen der flüssigen Phase. Es hängt von ihrem Tripelpunkt ab. Wenn der Druck seines Tripelpunkts zu hoch ist, ist es schwierig, sie als Flüssigkeiten zu erhalten.
Der umgekehrte Prozess der Desublimation ist die Sublimation, bei der eine Substanz direkt von einer festen in eine Gasphase übergeht.
Ein Beispiel für Desublimation ist die Bildung von Frost auf einem Blatt im Winter. Damit eine Desublimation stattfinden kann, muss einem Gas Wärmeenergie entzogen werden. Wenn das Blatt kalt genug wird, kann Wasserdampf in der das Blatt umgebenden Luft daher genügend Wärmeenergie verlieren, um sich direkt in einen Feststoff zu verwandeln.
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.