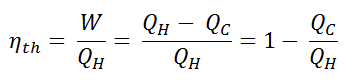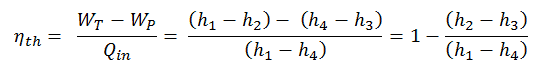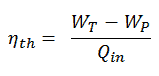Eficiencia térmica de la turbina de vapor
En general, la eficiencia térmica , η º , de cualquier motor de calor se define como la relación de la obra lo hace, W , para el calor de entrada a la alta temperatura, Q H .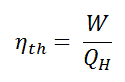
La eficiencia térmica , η th , representa la fracción de calor , Q H , que se convierte en trabajo . Dado que la energía se conserva de acuerdo con la primera ley de la termodinámica y la energía no se puede convertir para funcionar por completo, la entrada de calor, Q H , debe ser igual al trabajo realizado, W, más el calor que se debe disipar como calor residual Q C en el ambiente. Por lo tanto, podemos reescribir la fórmula para la eficiencia térmica como:
Esta es una fórmula muy útil, pero aquí expresamos la eficiencia térmica utilizando la primera ley en términos de entalpía .
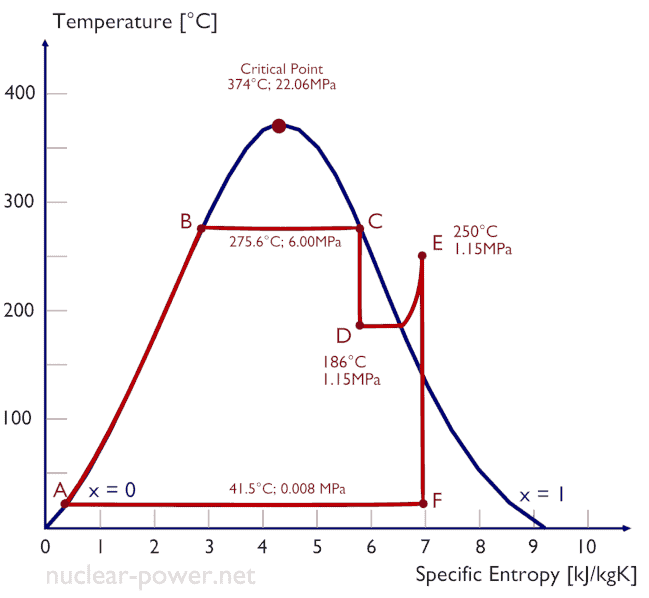
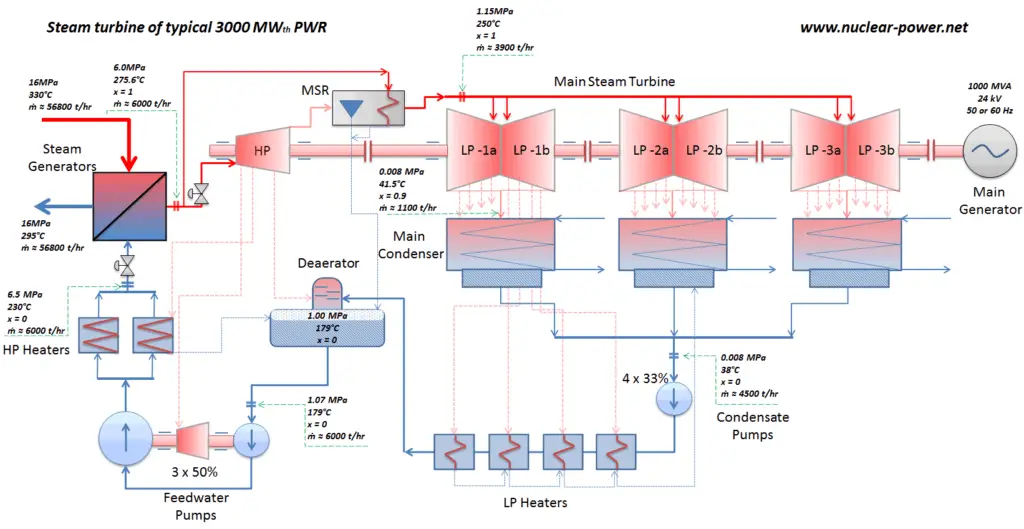
Típicamente, la mayoría de las plantas de energía nuclear opera turbinas de vapor de condensación de etapas múltiples . En estas turbinas, la etapa de alta presión recibe vapor (este vapor es vapor casi saturado – x = 0.995 – punto C en la figura; 6 MPa ; 275.6 ° C) desde un generador de vapor y lo expulsa al separador-recalentador de humedad (punto D ) El vapor debe recalentarse para evitar daños que puedan ocasionar a las aspas de la turbina de vapor el vapor de baja calidad . El recalentador calienta el vapor (punto D) y luego el vapor se dirige a la etapa de baja presión de la turbina de vapor, donde se expande (punto E a F). El vapor agotado se condensa en el condensador y está a una presión muy por debajo de la atmosférica (presión absoluta de0.008 MPa ), y está en un estado parcialmente condensado (punto F), típicamente de una calidad cercana al 90%.
En este caso, los generadores de vapor, la turbina de vapor, los condensadores y las bombas de agua de alimentación constituyen un motor térmico, sujeto a las limitaciones de eficiencia impuestas por la segunda ley de la termodinámica . En el caso ideal (sin fricción, procesos reversibles, diseño perfecto), este motor térmico tendría una eficiencia de Carnot de= 1 – T frío / T caliente = 1 – 315/549 = 42.6%
donde la temperatura del depósito caliente es 275.6 ° C (548.7K), la temperatura del depósito frío es 41.5 ° C (314.7K). Pero la central nuclear es el motor térmico real , en el que los procesos termodinámicos son de alguna manera irreversibles. No se hacen infinitamente lento. En dispositivos reales (como turbinas, bombas y compresores) una fricción mecánica y pérdidas de calor causan pérdidas adicionales de eficiencia.
Para calcular la eficiencia térmica del ciclo de Rankine más simple (sin recalentamiento), los ingenieros utilizan la primera ley de la termodinámica en términos de entalpía en lugar de en términos de energía interna.
La primera ley en términos de entalpía es:
dH = dQ + Vdp
En esta ecuación, el término Vdp es un proceso de flujo de trabajo. Este trabajo, Vdp , se utiliza para sistemas de flujo abierto como una turbina o una bomba en la que hay un “dp” , es decir, un cambio de presión. No hay cambios en el volumen de control . Como puede verse, esta forma de ley simplifica la descripción de la transferencia de energía . A presión constante , el cambio de entalpía es igual a la energía transferida del ambiente a través del calentamiento:
Proceso isobárico (Vdp = 0):
dH = dQ → Q = H 2 – H 1
En una entropía constante , es decir, en un proceso isentrópico, el cambio de entalpía es igual al trabajo del proceso de flujo realizado en o por el sistema:
Proceso isentrópico (dQ = 0):
dH = Vdp → W = H 2 – H 1
Es obvio, será muy útil en el análisis de los dos ciclos termodinámicos utilizados en la ingeniería de energía, es decir, en el ciclo de Brayton y el ciclo de Rankine.
La entalpía se puede convertir en una variable intensiva o específica dividiéndola por la masa . Los ingenieros usan la entalpía específica en el análisis termodinámico más que la entalpía misma. Se tabula en las tablas de vapor junto con un volumen específico y una energía interna específica . La eficiencia térmica de dicho ciclo simple de Rankine y en términos de entalpías específicas sería:
Es una ecuación muy simple y para determinar la eficiencia térmica puede usar datos de tablas de vapor .
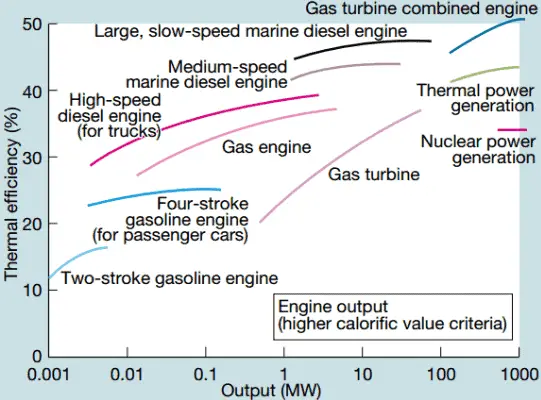
Eficiencia térmica de la turbina de vapor
En las centrales nucleares modernas, la eficiencia térmica general es de aproximadamente un tercio (33%), por lo que se necesitan 3000 MWth de energía térmica de la reacción de fisión para generar 1000 MWe de energía eléctrica. La razón radica en una temperatura de vapor relativamente baja ( 6 MPa ; 275.6 ° C). Se pueden lograr mayores eficiencias aumentando la temperaturadel vapor Pero esto requiere un aumento de las presiones dentro de las calderas o generadores de vapor. Sin embargo, las consideraciones metalúrgicas ponen límites superiores a tales presiones. En comparación con otras fuentes de energía, la eficiencia térmica del 33% no es mucho. Pero debe tenerse en cuenta que las centrales nucleares son mucho más complejas que las centrales de combustibles fósiles y es mucho más fácil quemar combustibles fósiles que generar energía a partir de combustibles nucleares. Las plantas de energía de combustible fósil subcrítico, que funcionan bajo presión crítica (es decir, por debajo de 22.1 MPa), pueden lograr una eficiencia de 36 a 40%.
Causas de ineficiencia
Como se discutió, una eficiencia puede variar entre 0 y 1. Cada motor térmico es de alguna manera ineficiente. Esta ineficiencia puede atribuirse a tres causas.
- Irreversibilidad de los procesos . Existe un límite superior teórico general para la eficiencia de la conversión de calor para trabajar en cualquier motor térmico. Este límite superior se llama eficiencia de Carnot . Según el principio de Carnot , ningún motor puede ser más eficiente que un motor reversible ( un motor térmico de Carnot ) que opera entre los mismos depósitos de alta temperatura y baja temperatura. Por ejemplo, cuando el depósito caliente tiene T caliente de 400 ° C (673K) y T frío de aproximadamente 20 ° C (293K), la eficiencia máxima (ideal) será: = 1 – T frío / T caliente = 1 – 293 / 673 = 56%. Pero todos los procesos termodinámicos reales son de alguna manera irreversibles.. No se hacen infinitamente lento. Por lo tanto, los motores térmicos deben tener eficiencias más bajas que los límites en su eficiencia debido a la irreversibilidad inherente del ciclo del motor térmico que usan.
- Presencia de fricción y pérdidas de calor. En sistemas termodinámicos reales o en motores de calor real, una parte de la ineficiencia general del ciclo se debe a las pérdidas de los componentes individuales. En dispositivos reales (como turbinas, bombas y compresores), una fricción mecánica , pérdidas de calor y pérdidas en el proceso de combustión causan pérdidas adicionales de eficiencia.
- Ineficiencia de diseño . Finalmente, la última y también importante fuente de ineficiencias son los compromisos asumidos por los ingenieros al diseñar un motor térmico (por ejemplo, una central eléctrica). Deben considerar el costo y otros factores en el diseño y operación del ciclo. Como ejemplo, considere un diseño del condensador en las centrales térmicas. Idealmente, el vapor extraído al condensador no tendría subenfriamiento . Pero los condensadores reales están diseñados para subenfriar el líquido unos pocos grados centígrados para evitar la cavitación por succión en las bombas de condensado. Pero, este subenfriamiento aumenta la ineficiencia del ciclo, porque se necesita más energía para recalentar el agua.
Mejora de la eficiencia térmica – Turbina de vapor
Existen varios métodos, ¿cómo puede mejorar la eficiencia térmica del ciclo de Rankine? Suponiendo que la temperatura máxima está limitada por la presión dentro del recipiente a presión del reactor, estos métodos son:
- Presiones de caldera y condensador
- Sobrecalentamiento y recalentamiento
- Regeneración de calor
- Ciclo supercrítico de Rankine
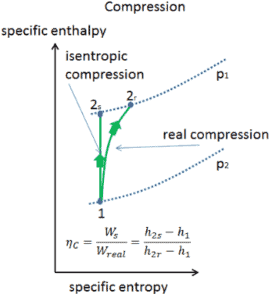
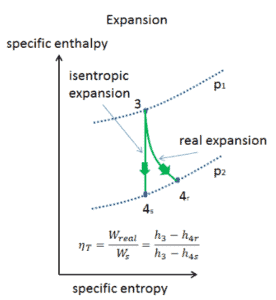
Eficiencia isentrópica: turbina, bomba
En capítulos anteriores supusimos que la expansión del vapor es isentrópica y, por lo tanto, usamos T 4, como la temperatura de salida del gas. Estos supuestos solo son aplicables con ciclos ideales.
La mayoría de los dispositivos de flujo constante (turbinas, compresores, boquillas) funcionan en condiciones adiabáticas, pero no son realmente isentrópicos, sino que están idealizados como isentrópicos para fines de cálculo. Definimos los parámetros η T , η P , η N , como una relación entre el trabajo real realizado por el dispositivo y el trabajo del dispositivo cuando se opera en condiciones isentrópicas (en el caso de una turbina). Esta relación se conoce como la eficiencia de la turbina isentrópica / bomba / boquilla . Estos parámetros describen qué tan eficientemente una turbina, compresor o boquilla se aproxima a un dispositivo isentrópico correspondiente. Este parámetro reduce la eficiencia general y el rendimiento del trabajo. Para turbinas, el valor de η T es típicamente de 0.7 a 0.9 (70-90%).
Ver también: proceso isentrópico
Turbina de vapor: problema con la solución
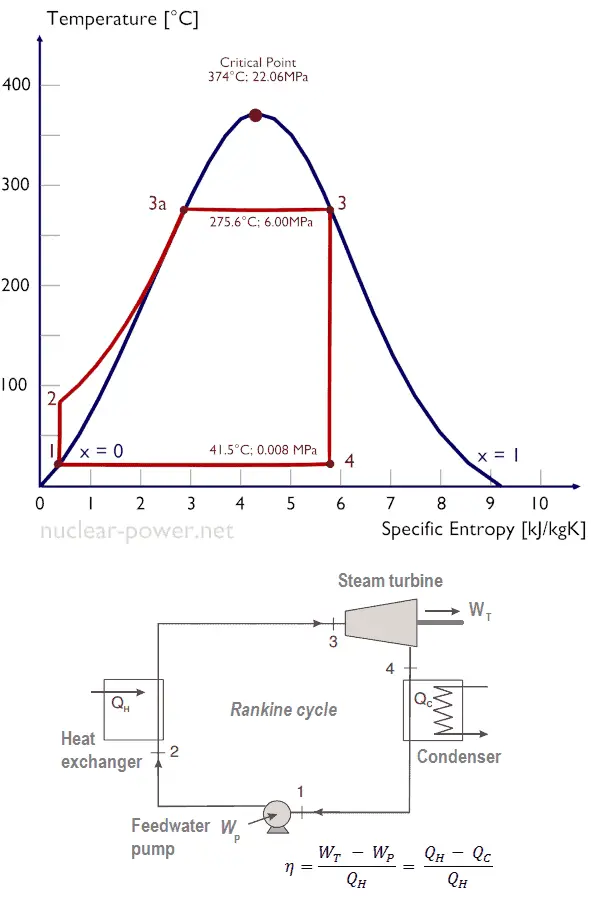 Supongamos el ciclo de Rankine , que es uno de los ciclos termodinámicos más comunes en las centrales térmicas. En este caso, suponga un ciclo simple sin recalentamiento y sin turbina de vapor de condensación funcionando con vapor saturado (vapor seco). En este caso, la turbina opera en estado estable con condiciones de entrada de 6 MPa, t = 275.6 ° C, x = 1 (punto 3). El vapor sale de esta etapa de la turbina a una presión de 0.008 MPa, 41.5 ° C yx = ??? (punto 4).
Supongamos el ciclo de Rankine , que es uno de los ciclos termodinámicos más comunes en las centrales térmicas. En este caso, suponga un ciclo simple sin recalentamiento y sin turbina de vapor de condensación funcionando con vapor saturado (vapor seco). En este caso, la turbina opera en estado estable con condiciones de entrada de 6 MPa, t = 275.6 ° C, x = 1 (punto 3). El vapor sale de esta etapa de la turbina a una presión de 0.008 MPa, 41.5 ° C yx = ??? (punto 4).
Calcular:
- la calidad del vapor del vapor de salida
- la diferencia de entalpía entre estos dos estados (3 → 4), que corresponde al trabajo realizado por el vapor, W T .
- la diferencia de entalpía entre estos dos estados (1 → 2), que corresponde a la labor realizada por las bombas, W P .
- La diferencia de entalpía entre estos dos estados (2 → 3), que corresponde al calor neto agregado en el generador de vapor
- la eficiencia termodinámica de este ciclo y compare este valor con la eficiencia de Carnot
1)
Como no conocemos la calidad exacta del vapor del vapor de salida, tenemos que determinar este parámetro. El estado 4 está fijado por la presión p 4 = 0.008 MPa y el hecho de que la entropía específica es constante para la expansión isentrópica (s 3 = s 4 = 5.89 kJ / kgK para 6 MPa ). La entropía específica del agua líquida saturada (x = 0) y el vapor seco (x = 1) puede seleccionarse de las tablas de vapor . En caso de vapor húmedo, la entropía real se puede calcular con la calidad del vapor, x, y las entropías específicas de agua líquida saturada y vapor seco:
s 4 = s v x + (1 – x) s l
dónde
s 4 = entropía de vapor húmedo (J / kg K) = 5.89 kJ / kgK
s v = entropía de vapor “seco” (J / kg K) = 8.227 kJ / kgK (para 0.008 MPa)
s l = entropía de agua líquida saturada (J / kg K) = 0.592 kJ / kgK (para 0.008 MPa)
De esta ecuación, la calidad del vapor es:
x 4 = ( s 4 – s l ) / ( s v – s l ) = (5.89 – 0.592) / (8.227 – 0.592) = 0.694 = 69.4%
2)
La entalpía para el estado 3 puede seleccionarse directamente de las mesas de vapor, mientras que la entalpía para el estado 4 debe calcularse utilizando la calidad del vapor:
h 3, v = 2785 kJ / kg
h 4, húmedo = h 4, v x + (1 – x) h 4, l = 2576. 0.694 + (1 – 0.694). 174 = 1787 + 53,2 = 1840 kJ / kg
Entonces el trabajo realizado por el vapor, W T, es
W T = Δh = 945 kJ / kg
3)
La entalpía para el estado 1 puede seleccionarse directamente de las mesas de vapor:
h 1, l = 174 kJ / kg
El estado 2 está fijado por la presión p 2 = 6.0 MPa y el hecho de que la entropía específica es constante para la compresión isentrópica (s 1 = s 2 = 0.592 kJ / kgK para 0.008 MPa ). Para esta entropía s 2 = 0.592 kJ / kgK y p 2 = 6.0 MPa encontramos h 2, subenfriado en tablas de vapor para agua comprimida (usando interpolación entre dos estados).
h 2, subenfriado = 179.7 kJ / kg
Entonces el trabajo realizado por las bombas, W P, es
W P = Δh = 5.7 kJ / kg
4)
La diferencia de entalpía entre (2 → 3), que corresponde al calor neto agregado en el generador de vapor, es simplemente:
Q add = h 3, v – h 2, subenfriado = 2785 – 179.7 = 2605.3 kJ / kg
Tenga en cuenta que no hay regeneración de calor en este ciclo. Por otro lado, la mayor parte del calor agregado es para la entalpía de vaporización (es decir, para el cambio de fase).
5)
En este caso, los generadores de vapor, la turbina de vapor, los condensadores y las bombas de agua de alimentación constituyen un motor térmico, sujeto a las limitaciones de eficiencia impuestas por la segunda ley de la termodinámica . En el caso ideal (sin fricción, procesos reversibles, diseño perfecto), este motor térmico tendría una eficiencia de Carnot de
η Carnot = 1 – T frío / T caliente = 1 – 315/549 = 42.6%
donde la temperatura del depósito caliente es de 275.6 ° C (548.7 K), la temperatura del depósito frío es de 41.5 ° C (314.7K).
La eficiencia termodinámica de este ciclo se puede calcular mediante la siguiente fórmula:
así
η th = (945 – 5.7) / 2605.3 = 0.361 = 36.1%
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.