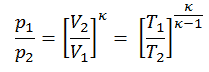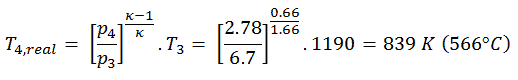Proceso adiabático
Un proceso adiabático es un proceso termodinámico , en el que no hay transferencia de calor dentro o fuera del sistema (Q = 0). El sistema puede considerarse perfectamente aislado . En un proceso adiabático, la energía se transfiere solo como trabajo. La suposición de que no hay transferencia de calor es muy importante, ya que podemos usar la aproximación adiabática solo en procesos muy rápidos . En estos procesos rápidos, no hay tiempo suficiente para que la transferencia de energía como calor tenga lugar hacia o desde el sistema.
En dispositivos reales (como turbinas, bombas y compresores) se producen pérdidas de calor y pérdidas en el proceso de combustión, pero estas pérdidas suelen ser bajas en comparación con el flujo de energía general y podemos aproximar algunos procesos termodinámicos por el proceso adiabático.
Ver también: Primera ley de la termodinámica.
Ver también: Ley del gas ideal
Ver también: Qué es la entalpía
Expansión adiabática – Compresión adiabática
Ver también: ¿Qué es un gas ideal?
En un gas ideal , las moléculas no tienen volumen y no interactúan. Según la ley de los gases ideales , la presión varía linealmente con la temperatura y la cantidad, e inversamente con el volumen .
pV = nRT
dónde:
- p es la presión absoluta del gas
- n es la cantidad de sustancia
- T es la temperatura absoluta
- V es el volumen
- R es la constante de gas ideal, o universal, igual al producto de la constante de Boltzmann y la constante de Avogadro,
En esta ecuación, el símbolo R es una constante llamada constante de gas universal que tiene el mismo valor para todos los gases, es decir, R = 8.31 J / mol K.
El proceso adiabático se puede expresar con la ley de los gases ideales como:
pV κ = constante
o
p 1 V 1 κ = p 2 V 2 κ
en el que κ = c p / c v es la relación de los calores específicos (o capacidades de calor ) para el gas. Uno para presión constante (c p ) y otro para volumen constante (c v ) . Tenga en cuenta que esta relación κ = c p / c v es un factor para determinar la velocidad del sonido en un gas y otros procesos adiabáticos.
Otra relación p, V, T
En un diagrama pV , el proceso ocurre a lo largo de una línea (llamada adiabat ) que tiene la ecuación p = constante / V κ . Para un proceso ideal de gas y politrópico, el caso n = κ corresponde a un proceso adiabático.
Ejemplo de expansión adiabática
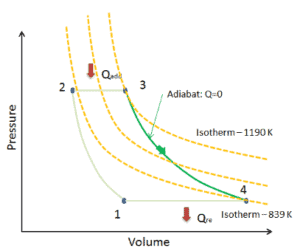
Suponga una expansión adiabática de helio ( 3 → 4 ) en una turbina de gas . Dado que el helio se comporta casi como un gas ideal , use la ley del gas ideal para calcular la temperatura de salida del gas ( T 4, real ). En estas turbinas, la etapa de alta presión recibe gas (punto 3 en la figura; p 3 = 6.7 MPa ; T 3 = 1190 K (917 ° C)) de un intercambiador de calor y lo expulsa a otro intercambiador de calor, donde la presión de salida es p 4 = 2.78 MPa (punto 4) .
Solución:
La temperatura de salida del gas, T 4, real , puede calcularse utilizando la relación p, V, T para el proceso adiabático. Tenga en cuenta que, es la misma relación que para el proceso isentrópico , por lo tanto, los resultados deben ser idénticos. En este caso, calculamos la expansión para diferentes turbinas de gas (menos eficientes) como en el caso de la expansión isentrópica en la turbina de gas.
En esta ecuación, el factor para helio es igual a κ = c p / c v = 1.66 . De la ecuación anterior se deduce que la temperatura de salida del gas, T 4, real , es:
Ver también: relación de Mayer
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.