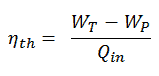Exemple de cycle de Rankine – Problème de solution
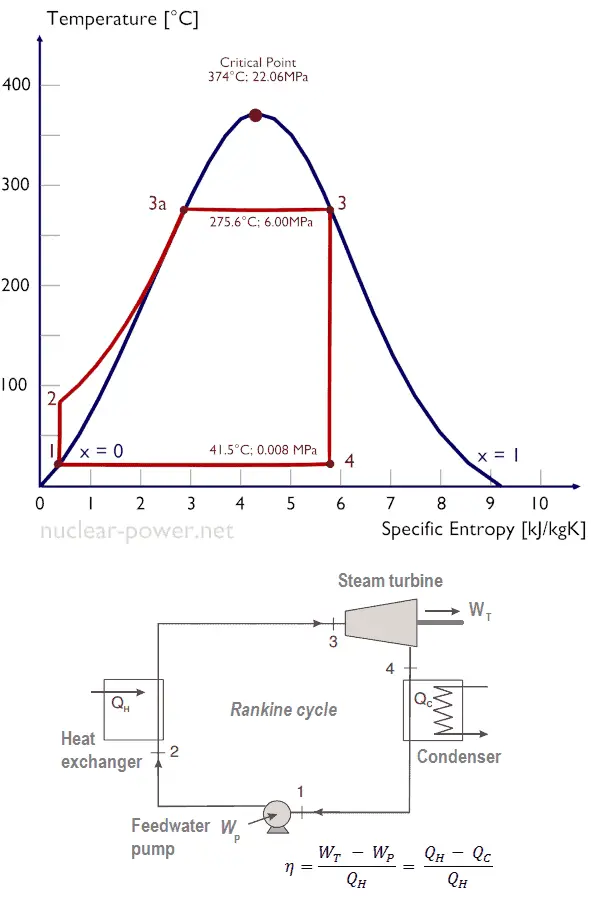 Supposons le cycle de Rankine , qui est l’un des cycles thermodynamiques les plus courants dans les centrales thermiques. Dans ce cas, supposons un cycle simple sans réchauffage et sans turbine à vapeur à condensation fonctionnant à la vapeur saturée (vapeur sèche). Dans ce cas, la turbine fonctionne en régime permanent avec des conditions d’entrée de 6 MPa, t = 275,6 ° C, x = 1 (point 3). La vapeur quitte cette étape de la turbine à une pression de 0,008 MPa, 41,5 ° C et x = ??? (point 4).
Supposons le cycle de Rankine , qui est l’un des cycles thermodynamiques les plus courants dans les centrales thermiques. Dans ce cas, supposons un cycle simple sans réchauffage et sans turbine à vapeur à condensation fonctionnant à la vapeur saturée (vapeur sèche). Dans ce cas, la turbine fonctionne en régime permanent avec des conditions d’entrée de 6 MPa, t = 275,6 ° C, x = 1 (point 3). La vapeur quitte cette étape de la turbine à une pression de 0,008 MPa, 41,5 ° C et x = ??? (point 4).
Calculer:
- la qualité de vapeur de la vapeur de sortie
- la différence d’enthalpie entre ces deux états (3 → 4), ce qui correspond au travail effectué par la vapeur, W T .
- la différence d’enthalpie entre ces deux états (1 → 2), qui correspond au travail effectué par les pompes, W P .
- la différence d’enthalpie entre ces deux états (2 → 3), qui correspond à la chaleur nette ajoutée dans le générateur de vapeur
- l’efficacité thermodynamique de ce cycle et comparer cette valeur avec l’efficacité de Carnot
1)
Comme nous ne connaissons pas la qualité de vapeur exacte de la vapeur de sortie, nous devons déterminer ce paramètre. L’état 4 est fixé par la pression p 4 = 0,008 MPa et le fait que l’ entropie spécifique est constante pour la dilatation isentrope (s 3 = s 4 = 5,89 kJ / kgK pour 6 MPa ). L’entropie spécifique de l’eau liquide saturée (x = 0) et de la vapeur sèche (x = 1) peut être sélectionnée à partir des tables de vapeur . En cas de vapeur humide, l’entropie réelle peut être calculée avec la qualité de la vapeur x et les entropies spécifiques de l’eau liquide saturée et de la vapeur sèche:
s 4 = s v x + (1 – x) s l
où
s 4 = entropie de vapeur humide (J / kg K) = 5,89 kJ / kgK
s v = entropie de vapeur «sèche» (J / kg K) = 8,227 kJ / kgK (pour 0,008 MPa)
s l = entropie d’eau liquide saturée (J / kg K) = 0,592 kJ / kgK (pour 0,008 MPa)
D’après cette équation, la qualité de la vapeur est:
x 4 = ( s 4 – s l ) / ( s v – s l ) = (5,89 – 0,592) / (8,227 – 0,592) = 0,694 = 69,4%
2)
L’enthalpie pour l’état 3 peut être prélevée directement dans les tables de vapeur, tandis que l’enthalpie pour l’état 4 doit être calculée en utilisant la qualité de la vapeur:
h 3, v = 2785 kJ / kg
h 4, humide = h 4, v x + (1 – x) h 4, l = 2576. 0,694 + (1 – 0,694). 174 = 1787 + 53,2 = 1840 kJ / kg
Ensuite, le travail effectué par la vapeur, W T, est
W T = Δh = 945 kJ / kg
3)
L’enthalpie pour l’état 1 peut être sélectionnée directement dans les tables à vapeur:
h 1, l = 174 kJ / kg
L’état 2 est fixé par la pression p 2 = 6,0 MPa et le fait que l’entropie spécifique est constante pour la compression isentropique (s 1 = s 2 = 0,592 kJ / kgK pour 0,008 MPa ). Pour cette entropie s 2 = 0,592 kJ / kgK et p 2 = 6,0 MPa, nous trouvons h 2, sous-refroidi dans les tables de vapeur pour l’eau comprimé (en utilisant l’interpolation entre deux états).
h 2, sous-refroidi = 179,7 kJ / kg
Ensuite, le travail effectué par les pompes, W P, est
W P = Δh = 5,7 kJ / kg
4)
La différence d’enthalpie entre (2 → 3), qui correspond à la chaleur nette ajoutée dans le générateur de vapeur, est simplement:
Q add = h 3, v – h 2, sous-refroidi = 2785 – 179,7 = 2605,3 kJ / kg
Notez qu’il n’y a pas de régénération de chaleur dans ce cycle. En revanche, la plus grande partie de la chaleur ajoutée est destinée à l’enthalpie de vaporisation (c’est-à-dire au changement de phase).
5)
Dans ce cas, les générateurs de vapeur, les turbines à vapeur, les condenseurs et les pompes à eau d’alimentation constituent un moteur thermique, soumis aux limitations d’efficacité imposées par la deuxième loi de la thermodynamique . Dans le cas idéal (pas de frottement, processus réversibles, conception parfaite), ce moteur thermique aurait une efficacité Carnot de
η Carnot = 1 – T froid / T chaud = 1 – 315/549 = 42,6%
où la température du réservoir chaud est de 275,6 ° C (548,7 K), la température du réservoir froid est de 41,5 ° C (314,7 K).
L’efficacité thermodynamique de ce cycle peut être calculée par la formule suivante:
donc
η th = (945 – 5,7) / 2605,3 = 0,361 = 36,1%
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci