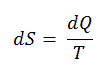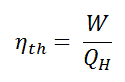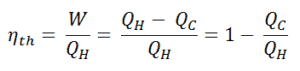Segunda Lei da Termodinâmica
A entropia de qualquer sistema isolado nunca diminui. Em um processo termodinâmico natural, a soma das entropias dos sistemas termodinâmicos em interação aumenta.
 Esta lei indica a irreversibilidade dos processos naturais . Processos reversíveis são uma ficção teórica útil e conveniente, mas não ocorrem na natureza. A partir desta lei, é impossível construir um dispositivo que opere em um ciclo e cujo único efeito seja a transferência de calor de um corpo mais frio para um corpo mais quente. Segue-se que máquinas perpétuas de movimento do segundo tipo são impossíveis.
Esta lei indica a irreversibilidade dos processos naturais . Processos reversíveis são uma ficção teórica útil e conveniente, mas não ocorrem na natureza. A partir desta lei, é impossível construir um dispositivo que opere em um ciclo e cujo único efeito seja a transferência de calor de um corpo mais frio para um corpo mais quente. Segue-se que máquinas perpétuas de movimento do segundo tipo são impossíveis.
A segunda lei da termodinâmica é um princípio geral, que vai além das limitações impostas pela primeira lei da termodinâmica . A primeira lei é usada para relacionar e avaliar as várias energias envolvidas em um processo. No entanto, nenhuma informação sobre a direção do processo pode ser obtida pela aplicação da primeira lei. A segunda lei da termodinâmica impõe restrições à direção da transferência de calor e estabelece um limite superior para a eficiência da conversão de calor em trabalho em motores térmicos . Portanto, a segunda lei é diretamente relevante para muitos problemas práticos importantes.
Uma das áreas de aplicação da segunda lei da termodinâmica é o estudo de sistemas de conversão de energia. Por exemplo, não é possível converter toda a energia obtida de um carvão em uma usina a carvão ou de um reator nuclear em uma usina nuclear em energia elétrica. Deve haver perdas no processo de conversão.
Direção de Processos Termodinâmicos
Muitos processos termodinâmicos procedem naturalmente em uma direção, mas não o contrário. Por exemplo, quando existe uma diferença de temperatura , o calor flui espontaneamente do sistema mais quente para o mais frio , nunca o contrário. De fato, esse fluxo de calor (de um corpo mais frio para um sistema mais quente) não violaria a primeira lei da termodinâmica , ou seja, a energia seria conservada. Mas isso não acontece na natureza.
Por exemplo, queimar gasolina para abastecer carros é um processo de conversão de energia em que confiamos. A energia química da gasolina é convertida em energia térmica , que é convertida em energia mecânica que faz o carro se mover. A energia mecânica foi convertida em energia cinética . Quando usamos os freios para parar um carro, essa energia cinética é convertida por fricção de volta ao calor, ou energia térmica . Nesta direção inversa, existem muitos dispositivos que convertem o calor parcialmente em energia mecânica. Mas você não pode construir uma máquina que converta calor completamente em energia mecânica. Sempre haverá perdas significativas de energia.
As direções dos processos termodinâmicos estão sujeitas à segunda lei da termodinâmica, especialmente à Declaração Clausius da Segunda Lei .
Várias declarações da lei
A segunda lei da termodinâmica pode ser expressa de várias maneiras específicas. Cada declaração expressa a mesma lei. Listados abaixo estão três que são frequentemente encontrados.
- Declaração Clausius
- Declaração de Kelvin-Planck
- Entropia e a Segunda Lei
Antes dessas declarações, devemos lembrar o trabalho de um engenheiro e físico francês, Nicolas Léonard Sadi Carnot, que avançou o estudo da segunda lei, formando um princípio ( também chamado de regra de Carnot ) que especifica limites para a máxima eficiência que qualquer motor térmico pode obter .
Clausius Declaração da Segunda Lei
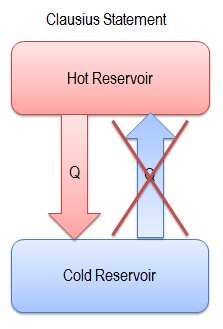 Uma das primeiras declarações da Segunda Lei da Termodinâmica foi feita por R. Clausius em 1850 . Ele afirmou o seguinte.
Uma das primeiras declarações da Segunda Lei da Termodinâmica foi feita por R. Clausius em 1850 . Ele afirmou o seguinte.
“É impossível construir um dispositivo que opere em um ciclo e cujo único efeito seja a transferência de calor de um corpo mais frio para um corpo mais quente”.
O calor não pode fluir espontaneamente do sistema frio para o sistema quente sem que seja executado um trabalho externo no sistema. É exatamente isso que os refrigeradores e as bombas de calor realizam. Em uma geladeira, o calor flui do frio para o quente, mas somente quando forçado por um trabalho externo, as geladeiras são acionadas por motores elétricos que exigem trabalho do ambiente para operar.
As declarações Clausius e Kelvin-Planck demonstraram ser equivalentes.
Declaração da Segunda Lei de Kelvin-Planck
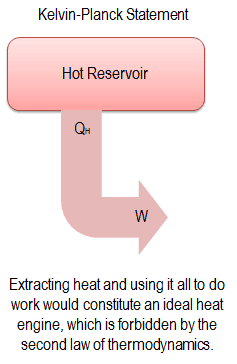 “É impossível construir um dispositivo que opera em um ciclo e não produz outro efeito senão a produção de trabalho e a transferência de calor de um único corpo”.
“É impossível construir um dispositivo que opera em um ciclo e não produz outro efeito senão a produção de trabalho e a transferência de calor de um único corpo”.
Esta declaração opera com o termo ” reservatório térmico ” ou ” reservatório único “. Um reservatório é um objeto grande, no qual a temperatura permanece constante enquanto a energia é extraída. Esse sistema pode ser aproximado de várias maneiras – pela atmosfera da Terra, grandes massas de água como lagos, oceanos e assim por diante.
A declaração Kelvin-Planck não exclui a existência de um sistema que desenvolve uma quantidade líquida de trabalho a partir de uma transferência de calor extraída de um reservatório térmico. De acordo com esta declaração, um sistema em ciclo não pode desenvolver uma quantidade líquida positiva de trabalho a partir de uma transferência de calor extraída de um reservatório térmico.
Entropia e a Segunda Lei
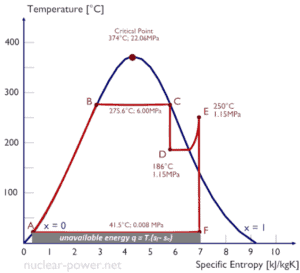
Uma conseqüência da segunda lei da termodinâmica é o desenvolvimento da propriedade física da matéria, conhecida como entropia (S) . A alteração nesta propriedade é usada para determinar a direção na qual um determinado processo continuará. A entropia quantifica a energia de uma substância que não está mais disponível para realizar um trabalho útil . Isso se refere à segunda lei, uma vez que a segunda lei prevê que nem todo o calor fornecido a um ciclo pode ser transformado em uma quantidade igual de trabalho; alguma rejeição de calor deve ocorrer.
Veja também: Entropia
Segundo Clausius, a entropia foi definida através da mudança na entropia S de um sistema. A mudança na entropia S, quando uma quantidade de calor Q é adicionada a ela por um processo reversível a temperatura constante, é dada por:
Aqui Q é a energia transferida como calor para ou do sistema durante o processo, e T é a temperatura do sistema em Kelvins durante o processo. A unidade SI de entropia é J / K .
A segunda lei da termodinâmica também pode ser expressa como ∆S≥0 para um ciclo fechado.
Em palavras:
A entropia de qualquer sistema isolado nunca diminui. Em um processo termodinâmico natural, a soma das entropias dos sistemas termodinâmicos em interação aumenta.
∆S≥0
Como a entropia diz muito sobre a utilidade de uma quantidade de calor transferida na execução do trabalho, as tabelas de vapor incluem valores de entropia específica (s = S / m) como parte das informações tabuladas.
Motores térmicos
As fontes de energia sempre desempenharam um papel muito importante no desenvolvimento da sociedade humana. A energia é geralmente definida como o potencial de trabalhar ou produzir calor . Às vezes, é como a “moeda” para executar o trabalho. Uma das propriedades mais maravilhosas do universo é que a energia pode ser transformada de um tipo para outro e transferida de um objeto para outro .
Em geral, é fácil produzir energia térmica realizando trabalhos , por exemplo, por qualquer processo de atrito. Mas conseguir trabalho com energia térmica é mais difícil . Está intimamente associado ao conceito de entropia . Por exemplo, a eletricidade é particularmente útil, pois possui uma entropia muito baixa (é altamente solicitada) e pode ser convertida em outras formas de energia com muita eficiência .
Às vezes, a energia mecânica está diretamente disponível, por exemplo, energia eólica e hidrelétrica. Mas a maior parte de nossa energia vem da queima de combustíveis fósseis (carvão, petróleo e gás) e de reações nucleares . Atualmente, o combustível fóssil ainda é a fonte de energia predominante no mundo. Mas a queima de combustíveis fósseis gera apenas energia térmica , portanto essas fontes de energia são chamadas de ” fontes de energia primária “, que devem ser convertidas em fonte de energia secundária , chamadas de portadores de energia ( energia elétrica etc.). Para converter energia térmica em outra forma de energia, um motor térmico deve ser usado.
Em geral, um motor térmico é um dispositivo que converte energia química em calor ou energia térmica e depois em energia mecânica ou em energia elétrica.
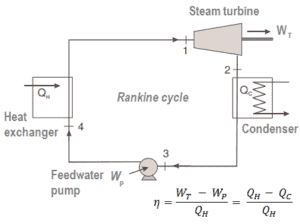
Muitos motores térmicos operam de maneira cíclica, adicionando energia na forma de calor em uma parte do ciclo e usando essa energia para realizar trabalhos úteis em outra parte do ciclo.
Por exemplo, como é típico em todas as usinas térmicas convencionais , o calor é usado para gerar vapor que aciona uma turbina a vapor conectada a um gerador que produz eletricidade. Geradores de vapor, turbinas a vapor, condensadores e bombas de água de alimentação constituem um motor térmico , sujeito às limitações de eficiência impostas pela segunda lei da termodinâmica . Nas modernas usinas nucleares, a eficiência termodinâmica geral é de cerca deum terço (33%), então são necessários 3000 MWth de energia térmica da reação de fissão para gerar 1000 MWe de energia elétrica.
Tipos de motores térmicos
Em geral, os motores térmicos são classificados de acordo com um local de combustão como:
- Motor de combustão externa. Por exemplo, os motores a vapor são motores de combustão externa, onde o fluido de trabalho é separado dos produtos de combustão.
- Motor de combustão interna. Um exemplo típico de motor de combustão interna é um motor usado no automóvel, no qual a alta temperatura é alcançada queimando a mistura gasolina-ar no próprio cilindro.
A categorização detalhada é baseada em um fluido de trabalho usado no ciclo termodinâmico:
- Ciclos de gás. Nestes ciclos, o fluido de trabalho é sempre um gás. O ciclo Otto e o ciclo Diesel (usado são automóveis) também são exemplos típicos de ciclos somente de gás. Os modernos motores de turbina a gás e os motores a jato de respiração, também baseados no ciclo apenas de gás, seguem o ciclo de Brayton.
- Ciclos líquidos. Ciclos apenas líquidos são bastante exóticos. Nestes ciclos, o fluido de trabalho é sempre um líquido. O mecanismo líquido Malone é um exemplo de ciclo somente líquido. O motor líquido Malone era uma modificação do ciclo de Stirling, usando a água como fluido de trabalho em vez de gás
- Ciclos com alterações de fase. Os motores a vapor são exemplos típicos de motores externos com mudança de fase do fluido de trabalho.
Exemplo de motor térmico
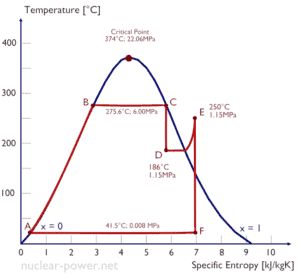
Motores a vapor e geladeiras são exemplos típicos de motores externos com mudança de fase do fluido de trabalho. O ciclo termodinâmico típico usado para analisar esse processo é chamado de ciclo Rankine , que geralmente usa água como fluido de trabalho.
O ciclo Rankine descreve de perto os processos em motores térmicos a vapor comumente encontrados na maioria das usinas termelétricas . As fontes de calor usadas nessas usinas são geralmente a combustão de combustíveis fósseis, como carvão, gás natural ou também a fissão nuclear .
Uma usina nuclear ( usina nuclear) se parece com uma usina termelétrica padrão, com uma exceção. A fonte de calor na usina nuclear é um reator nuclear . Como é típico em todas as centrais térmicas convencionais, o calor é usado para gerar vapor que aciona uma turbina a vapor conectada a um gerador que produz eletricidade.
Normalmente, a maioria das usinas nucleares opera turbinas a vapor de condensação de vários estágios . Nessas turbinas, o estágio de alta pressão recebe vapor (esse vapor é quase saturado – x = 0,995 – ponto C na figura; 6 MPa ; 275,6 ° C) de um gerador de vapor e o esgota para o separador-reaquecedor de umidade (ponto D ) O vapor deve ser reaquecido para evitar danos que possam ser causados às pás da turbina a vapor por vapor de baixa qualidade . O reaquecedor aquece o vapor (ponto D) e, em seguida, o vapor é direcionado para o estágio de baixa pressão da turbina a vapor, onde se expande (pontos E a F). O vapor exaurido condensa no condensador e está a uma pressão bem abaixo da atmosférica (pressão absoluta de0,008 MPa ) e está em um estado parcialmente condensado (ponto F), tipicamente com uma qualidade próxima a 90%.
Nesse caso, geradores de vapor, turbinas a vapor, condensadores e bombas de água de alimentação constituem um motor térmico, sujeito às limitações de eficiência impostas pela segunda lei da termodinâmica . No caso ideal (sem atrito, processos reversíveis, design perfeito), este motor térmico teria uma eficiência de Carnot de
= 1 – T frio / T quente = 1 – 315/549 = 42,6%
onde a temperatura do reservatório quente é de 275,6 ° C (548,7 K), a temperatura do reservatório frio é de 41,5 ° C (314,7 K). Mas a usina nuclear é o verdadeiro motor térmico , no qual os processos termodinâmicos são de alguma forma irreversíveis. Eles não são feitos infinitamente devagar. Em dispositivos reais (como turbinas, bombas e compressores), um atrito mecânico e perdas de calor causam mais perdas de eficiência.
Portanto, usinas nucleares geralmente têm eficiência em torno de 33%. Nas modernas usinas nucleares, a eficiência termodinâmica geral é de cerca de um terço (33%); portanto, são necessários 3000 MWth de energia térmica da reação de fissão para gerar 1000 MWe de energia elétrica.
De acordo com o princípio de Carnot, é possível obter maiores eficiências aumentando a temperatura do vapor. Mas isso requer um aumento nas pressões dentro de caldeiras ou geradores de vapor. No entanto, considerações metalúrgicas impõem limites superiores a essas pressões. Deste ponto de vista, os reatores supercríticos de água são considerados um avanço promissor para as usinas nucleares devido à sua alta eficiência térmica (~ 45% vs. ~ 33% para as LWRs atuais). Os SCWRs são operados sob pressão supercrítica (ou seja, maior que 22,1 MPa).
Eficiência térmica e a segunda lei
Um mecanismo térmico ideal é um mecanismo imaginário no qual a energia extraída como calor do reservatório de alta temperatura é convertida completamente em funcionamento. Mas, de acordo com a declaração de Kelvin-Planck , esse mecanismo violaria a segunda lei da termodinâmica, porque deve haver perdas no processo de conversão. O calor líquido adicionado ao sistema deve ser maior que o trabalho líquido realizado pelo sistema.
Declaração de Kelvin-Planck:
“É impossível construir um dispositivo que opera em um ciclo e não produz outro efeito senão a produção de trabalho e a transferência de calor de um único corpo”.
Fórmula de eficiência térmica
Como resultado de esta afirmação, que definem a eficiência térmica , η th , de qualquer motor de calor como a razão entre o trabalho que faz, W , para o calor de entrada a uma temperatura elevada, Q H .
A eficiência térmica , η th , representa a fração de calor , Q H , que é convertida em trabalho . É uma medida de desempenho adimensional de um motor térmico que usa energia térmica, como uma turbina a vapor, um motor de combustão interna ou um refrigerador. Para uma refrigeração ou bombas de calor, a eficiência térmica indica até que ponto a energia adicionada pelo trabalho é convertida na produção líquida de calor. Como é um número sem dimensão, devemos sempre expressar W, Q H e Q C nas mesmas unidades.
Como a energia é conservada de acordo com a primeira lei da termodinâmica e a energia não pode ser convertida para funcionar completamente, a entrada de calor, Q H , deve ser igual ao trabalho realizado, W, mais o calor que deve ser dissipado como calor residual Q C no meio Ambiente. Portanto, podemos reescrever a fórmula da eficiência térmica como:
Para fornecer a eficiência em porcentagem, multiplicamos a fórmula anterior por 100. Observe que η th pode ser 100% apenas se o calor residual Q C for zero.
Em geral, a eficiência dos melhores motores térmicos é bastante baixa. Em suma, é muito difícil para converter energia térmica a energia mecânica . As eficiências térmicas geralmente são inferiores a 50% e geralmente muito abaixo. Tenha cuidado ao compará-lo com a eficiência da energia eólica ou hidrelétrica (turbinas eólicas não são motores de calor), não há conversão de energia entre a energia térmica e a mecânica.
Causas de ineficiência
Como foi discutido, uma eficiência pode variar entre 0 e 1. Cada mecanismo térmico é de alguma forma ineficiente. Essa ineficiência pode ser atribuída a três causas.
- Irreversibilidade de processos . Existe um limite superior teórico geral para a eficiência da conversão de calor em trabalho em qualquer motor térmico. Esse limite superior é chamado de eficiência de Carnot . De acordo com o princípio Carnot , nenhum motor pode ser mais eficiente que um motor reversível ( um motor térmico Carnot ) operando entre os mesmos reservatórios de alta temperatura e baixa temperatura. Por exemplo, quando o reservatório quente tiver T quente de 400 ° C (673K) e T frio de cerca de 20 ° C (293K), a eficiência máxima (ideal) será: = 1 – T frio / T quente = 1 – 293 / 673 = 56%. Mas todos os processos termodinâmicos reais são de alguma forma irreversíveis. Eles não são feitos infinitamente devagar. Portanto, os motores térmicos devem ter eficiências mais baixas do que os limites de eficiência devido à irreversibilidade inerente ao ciclo dos motores térmicos que utilizam.
- Presença de fricção e perdas de calor. Em sistemas termodinâmicos reais ou em motores térmicos reais, uma parte da ineficiência geral do ciclo é devida às perdas dos componentes individuais. Em dispositivos reais (como turbinas, bombas e compressores), um atrito mecânico , perdas de calor e perdas no processo de combustão causam mais perdas de eficiência.
- Ineficiência do projeto . Finalmente, a última e também importante fonte de ineficiências provém dos compromissos assumidos pelos engenheiros ao projetar um motor térmico (por exemplo, usina). Eles devem considerar o custo e outros fatores no design e operação do ciclo. Como exemplo, considere um projeto do condensador nas usinas termelétricas. Idealmente, o vapor descarregado no condensador não teria sub-resfriamento . Mas os condensadores reais são projetados para sub-resfriar o líquido em alguns graus Celsius, a fim de evitar a cavitação de sucção nas bombas de condensado. Porém, esse sub-resfriamento aumenta a ineficiência do ciclo, porque é necessária mais energia para reaquecer a água.
Eficiência térmica de motores térmicos
Em geral, a eficiência dos melhores motores térmicos é bastante baixa. Em resumo, é muito difícil converter energia térmica em energia mecânica . As eficiências térmicas geralmente são inferiores a 50% e geralmente muito abaixo.
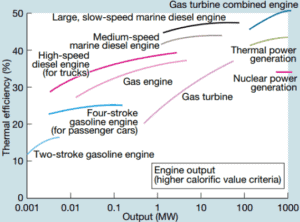
É fácil produzir energia térmica fazendo o trabalho, por exemplo, por qualquer processo de atrito. Mas conseguir trabalho com energia térmica é mais difícil. Está intimamente associado ao conceito de entropia , que quantifica a energia de uma substância que não está mais disponível para realizar um trabalho útil. Por exemplo, a eletricidade é particularmente útil, pois possui entropia muito baixa (é altamente ordenada) e pode ser convertida em outras formas de energia com muita eficiência . Tenha cuidado ao compará-lo com a eficiência da energia eólica ou hidrelétrica (turbinas eólicas não são motores de calor), não há conversão de energia entre a energia térmica e a mecânica.
A eficiência térmica de vários motores térmicos projetados ou usados hoje em dia tem uma grande variedade:
Por exemplo:
Transporte
- Em meados do século XX, uma locomotiva a vapor típica tinha uma eficiência térmica de cerca de 6% . Isso significa que para cada 100 MJ de carvão queimado, 6 MJ de potência mecânica foram produzidos.
- Um motor automotivo a gasolina típico opera com cerca de 25% a 30% de eficiência térmica. Cerca de 70-75% é rejeitado como calor residual sem ser convertido em trabalho útil, ou seja, trabalho entregue às rodas.
- Um motor automotivo a diesel típico opera em torno de 30% a 35% . Em geral, os motores que usam o ciclo Diesel geralmente são mais eficientes.
- Em 2014, novos regulamentos foram introduzidos para carros de Fórmula 1 . Esses regulamentos sobre esportes a motor levaram as equipes a desenvolver unidades de potência altamente eficientes. Segundo a Mercedes, sua unidade de potência está atingindo mais de 45% e quase 50% de eficiência térmica, ou seja, 45 a 50% da energia potencial do combustível é entregue às rodas.
- O motor diesel tem a mais alta eficiência térmica de qualquer motor de combustão prático. Os motores a diesel de baixa velocidade (usados em navios) podem ter uma eficiência térmica superior a 50% . O maior motor diesel do mundo chega a 51,7%.
Engenharia de Energia
- Conversão de energia térmica oceânica (OTEC). O OTEC é um motor térmico muito sofisticado que usa a diferença de temperatura entre águas do mar mais frias e profundas da superfície para acionar uma turbina de baixa pressão. Como a diferença de temperatura é baixa , cerca de 20 ° C, sua eficiência térmica também é muito baixa, cerca de 3% .
- Nas modernas usinas nucleares, a eficiência térmica geral é de cerca de um terço (33%); portanto, são necessários 3000 MWth de energia térmica da reação de fissão para gerar 1000 MWe de energia elétrica. Eficiências mais altas podem ser alcançadas aumentando a temperatura do vapor . Mas isso requer um aumento nas pressões dentro de caldeiras ou geradores de vapor. No entanto, considerações metalúrgicas impõem limites superiores a essas pressões. Em comparação com outras fontes de energia, a eficiência térmica de 33% não é grande. Mas deve-se notar que as usinas nucleares são muito mais complexas que as usinas de combustíveis fósseis e é muito mais fácil queimar combustíveis fósseis do que gerar energia a partir de combustíveis nucleares .
- As usinas subcríticas de combustíveis fósseis, que são operadas sob pressão crítica (ou seja, inferiores a 22,1 MPa), podem atingir uma eficiência de 36 a 40%.
- Os reatores supercríticos de água são considerados um avanço promissor para as usinas nucleares devido à sua alta eficiência térmica (~ 45% vs. ~ 33% para as LWRs atuais).
- As usinas supercríticas de combustíveis fósseis, que são operadas sob pressão supercrítica (ou seja, superior a 22,1 MPa), têm eficiência em torno de 43% . As usinas elétricas a carvão mais eficientes e também muito complexas, operadas a pressões “ultra-críticas” (ou seja, cerca de 30 MPa) e que utilizam reaquecimento em vários estágios, atingem cerca de 48% de eficiência.
- As modernas instalações de turbina a gás de ciclo combinado (CCGT), nas quais o ciclo termodinâmico consiste em dois ciclos de usina (por exemplo, o ciclo de Brayton e o ciclo Rankine), podem atingir uma eficiência térmica de cerca de 55% , em contraste com um vapor de ciclo único usina, limitada a eficiências em torno de 35 a 45%.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.