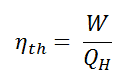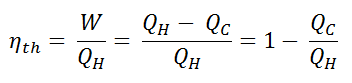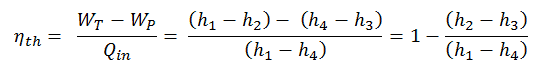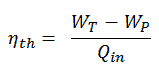Clausius-Rankine-Kreisprozess – Dampfturbinen-Zyklus
William John Macquorn Rankine , ein schottischer Ingenieur, brachte 1859 das Studium der Wärmekraftmaschinen voran, indem er das „ Handbuch der Dampfmaschine und anderer Kraftmaschinen “ veröffentlichte. Rankine entwickelte eine vollständige Theorie der Dampfmaschine und aller Wärmekraftmaschinen. Zusammen mit Rudolf Clausius und William Thomson (Lord Kelvin) leistete er einen Beitrag zur Thermodynamik, wobei er sich insbesondere auf das erste der drei thermodynamischen Gesetze konzentrierte.
Der nach ihm benannte Rankine-Zyklus beschreibt die Leistung von Dampfturbinensystemen , obwohl das theoretische Prinzip auch für Hubkolbenmotoren wie Dampflokomotiven gilt. Im Allgemeinen ist der Rankine-Zyklus ein idealisierter thermodynamischer Zyklus einer Konstantdruck-Wärmekraftmaschine, die einen Teil der Wärme in mechanische Arbeit umwandelt. In diesem Kreislauf wird die Wärme extern einem geschlossenen Kreislauf zugeführt, der üblicherweise Wasser (in flüssiger und dampfförmiger Phase) als Arbeitsmedium verwendet. Im Gegensatz zum Brayton- Zyklus unterliegt das Arbeitsfluid im Rankine-Zyklus dem Phasenwechsel von einer flüssigen in eine Dampfphase und umgekehrt.
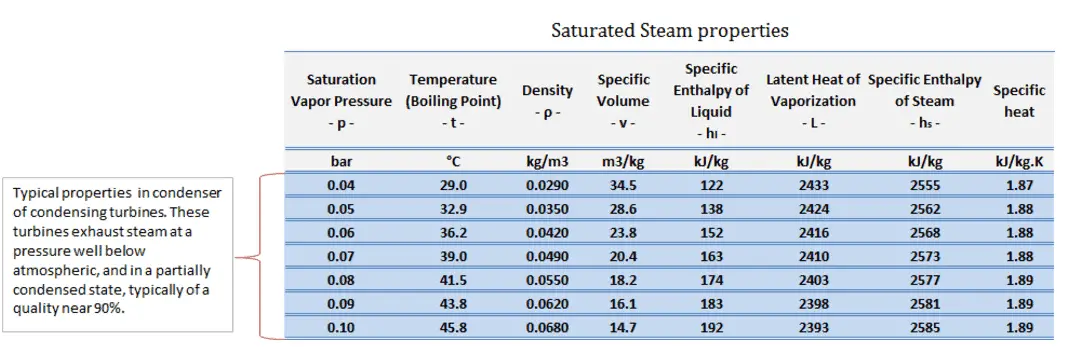
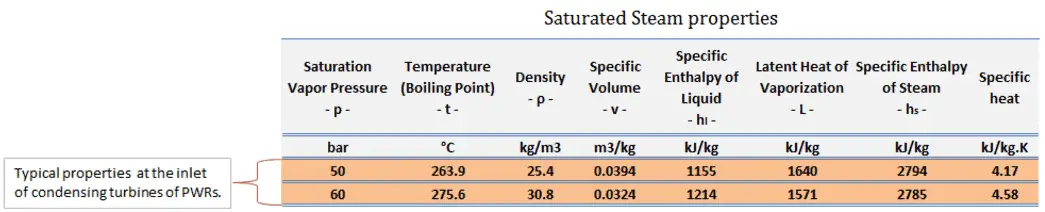
Während viele Substanzen als Arbeitsfluid im Rankine-Kreislauf (anorganisch oder sogar organisch) verwendet werden könnten, ist Wasser aufgrund seiner günstigen Eigenschaften, wie seiner ungiftigen und unreaktiven Chemie, seines Überflusses und seiner geringen Kosten, normalerweise das Fluid der Wahl. sowie seine thermodynamischen Eigenschaften. Beispielsweise hat Wasser die höchste spezifische Wärme aller gängigen Stoffe – 4,19 kJ / kg K. Darüber hinaus weist es eine sehr hohe Verdampfungswärme auf , was es zu einem wirksamen Kühlmittel und Medium in Wärmekraftwerken und anderen Energieanlagen macht. Im Fall des Rankine-Zyklus das Ideale GasgesetzKann fast nicht verwendet werden (Dampf folgt nicht pV = nRT), daher sind alle wichtigen Parameter von Wasser und Dampf in sogenannten „ Dampftabellen “ aufgeführt.
Einer der Hauptvorteile des Rankine-Zyklus ist, dass der Kompressionsprozess in der Pumpe auf einer Flüssigkeit stattfindet . Durch die Kondensation des Arbeitsdampfes zu einer Flüssigkeit (innerhalb eines Kondensators) wird der Druck am Turbinenaustritt abgesenkt und die von der Förderpumpe benötigte Energie verbraucht nur 1% bis 3% der Turbinenleistung und diese Faktoren tragen zu einem höheren Wirkungsgrad bei der Kreislauf.
Der Rankine-Zyklus ist heute der grundlegende Betriebszyklus aller thermischen Kraftwerke, in denen ein Betriebsfluid kontinuierlich verdampft und kondensiert wird. Dies ist einer der häufigsten thermodynamischen Zyklen, da die Turbine an den meisten Orten der Welt mit Dampf angetrieben wird.Im Gegensatz zum Carnot-Zyklus führt der Rankine-Zyklus keine isothermen Prozesse aus, da diese sehr langsam durchgeführt werden müssen. In einem idealen Rankine-Zyklus durchläuft das System, das den Zyklus ausführt, eine Reihe von vier Prozessen: Zwei isentrope (reversible adiabatische) Prozesse wechseln sich mit zwei isobaren Prozessen ab.
Da nach dem Carnot-Prinzip kein Motor effizienter sein kann als ein umkehrbarer Motor ( ein Carnot-Wärmemotor ), der zwischen denselben Hochtemperatur- und Niedertemperaturspeichern betrieben wird, muss eine auf dem Rankine-Zyklus basierende Dampfturbine einen niedrigeren Wirkungsgrad aufweisen als der Carnot-Wirkungsgrad.
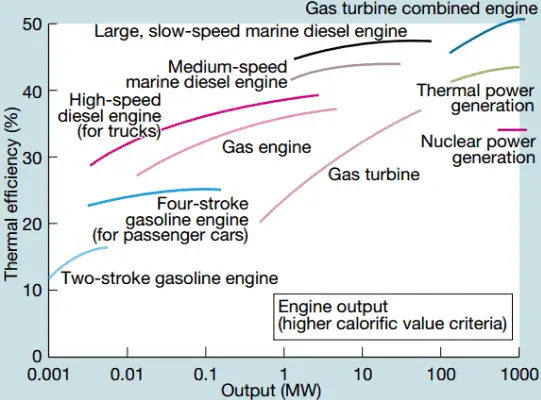
In modernen Kernkraftwerken beträgt der Gesamtwärmewirkungsgrad etwa ein Drittel (33%), sodass 3000 MWth der thermischen Leistung aus der Spaltreaktion zur Erzeugung von 1000 MWe elektrischer Leistung benötigt werden. Höhere Wirkungsgrade können durch Erhöhen der Temperatur des Dampfes erreicht werden . Dies erfordert jedoch eine Erhöhung des Drucks in Kesseln oder Dampferzeugern. Metallurgische Überlegungen setzen, drücken jedoch Obergrenzen. Im Vergleich zu anderen Energiequellen ist der thermische Wirkungsgrad von 33% nicht viel. Es muss jedoch beachtet Werden that viele KOMPLEXER Kernkraftwerke Ist als Kraftwerke mit fossilen Brennstoffen und es viel Einfacher ist, Fossile Brennstoffe zu verbrennen, aus als Kernbrennstoffen Energie zu erzeugen.
Rankine-Zyklus – Prozesse
In einem idealen Rankine-Zyklus durchläuft das den Zyklus ausführende System eine Reihe von vier Prozessen: zwei isentrope (reversible adiabatische) Prozesse im Wechsel mit zwei isobaren Prozessen:
-
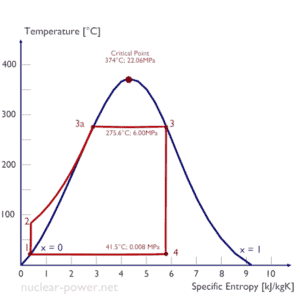
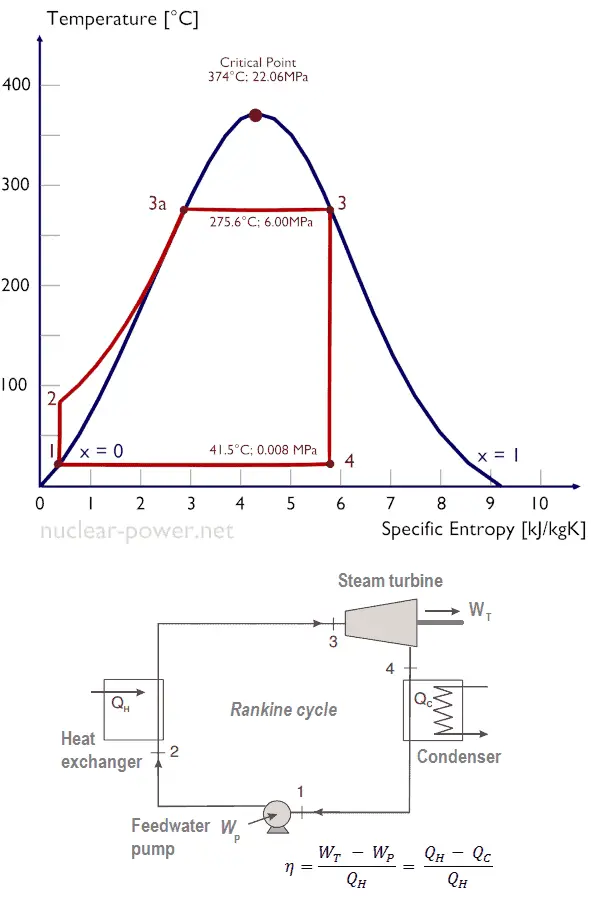
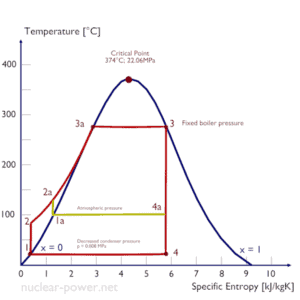
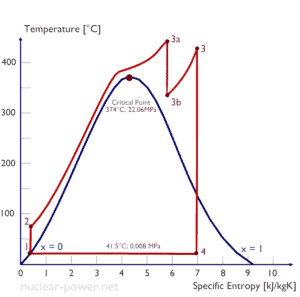
Rankine-Zyklus – Ts-Diagramm Isentrope Verdichtung (Verdichtung in Kreiselpumpen) – Das flüssige Kondensat wird durch Kreiselpumpen (meist durch Kondensatpumpen und dann durch Speisewasserpumpen) adiabatisch von Zustand 1 auf Zustand 2 verdichtet. Das flüssige Kondensat wird vom Kondensator in den Hochdruckkessel gepumpt. Dabei wirkt die Umgebung auf das Fluid, indem es seine Enthalpie (h = u+pv) erhöht und es komprimiert (erhöht seinen Druck). Andererseits bleibt die Entropie unverändert. Die für den Verdichter erforderliche Arbeit ergibt sich aus W Pumpen = H 2 – H 1 .
- Isobare Wärmezufuhr (in einem Wärmetauscher – Kessel) – In dieser Phase (zwischen Zustand 2 und Zustand 3) erfolgt eine druckkonstante Wärmeübertragung auf das flüssige Kondensat von einer externen Quelle, da die Kammer zum Ein- und Ausströmen geöffnet ist . Das Speisewasser (Sekundärkreislauf) wird bis zum Siedepunkt (2 → 3a) dieser Flüssigkeit erhitzt und anschließend im Kessel verdampft (3a → 3). Die hinzugefügte Nettowärme ist gegeben durch Q add = H 3 – H 2
- Isentrope Expansion (Expansion in einer Dampfturbine) – Dampf aus dem Kessel expandiert adiabatisch von Zustand 3 in Zustand 4 in einer Dampfturbine, um Arbeit zu verrichten und wird dann in den Kondensator abgegeben (teilkondensiert). Der Dampf verrichtet Arbeit an der Umgebung (Schaufeln der Turbine) und verliert eine Enthalpie gleich der Arbeit, die das System verlässt. Die Turbinenarbeit ist gegeben durch W T = H 4 – H 3 . Auch hier bleibt die Entropie unverändert.
- Isobare Wärmeabgabe (in einem Wärmetauscher) – In dieser Phase wird der Kreislauf durch einen Prozess mit konstantem Druck abgeschlossen, bei dem Wärme aus dem teilweise kondensierten Dampf abgegeben wird. Es findet eine Wärmeübertragung vom Dampf auf das in einem Kühlkreislauf strömende Kühlwasser statt. Der Dampf kondensiert und die Temperatur des Kühlwassers steigt. Die abgegebene Nettowärme ist gegeben durch Q re = H 4 – H 1
Während eines Rankine-Zyklus wird von den Pumpen zwischen den Zuständen 1 und 2 ( i sentropische Kompression ) Arbeit an der Flüssigkeit verrichtet . Zwischen den Stufen 3 und 4 verrichtet das Fluid in der Turbine Arbeit ( i sentrope Expansion ). Die Differenz zwischen der vom Fluid geleisteten Arbeit und der vom Fluid verrichteten Arbeit ist das vom Kreislauf erzeugte Netz und entspricht der von der Kreiskurve eingeschlossenen Fläche (im pV-Diagramm). Das Arbeitsfluid in einem Rankine-Kreislauf folgt einem geschlossenen Kreislauf und wird ständig wiederverwendet.
Wie zu sehen ist, ist es praktisch, die Enthalpie und den ersten Hauptsatz in Bezug auf die Enthalpie bei der Analyse dieses thermodynamischen Zyklus zu verwenden. Diese Form des Gesetzes vereinfacht die Beschreibung der Energieübertragung . Bei konstantem Druck , die Enthalpieänderung ist gleich die Energie aus der Umgebung durch Erhitzen übertragen:
Isobarer Prozess (Vdp = 0):
dH = dQ → Q = H 2 – H 1
Bei konstanter Entropie , dh im isentropen Prozess, entspricht die Enthalpieänderung der am oder vom System geleisteten Strömungsprozessarbeit :
Isentroper Prozess (dQ = 0):
dH = Vdp → W = H 2 – H 1
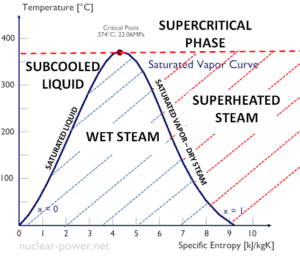
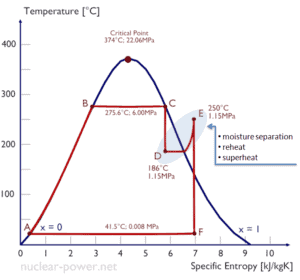
Siehe auch: Warum verwenden Energieingenieure Enthalpie? Antwort: dH = dQ + Vdp [/lgc_column] Ein isentroper Prozess ist ein thermodynamischer Prozess , bei dem die Entropie des Fluids oder Gases konstant bleibt. Dies bedeutet, dass der isentrope Prozess ein Sonderfall eines adiabatischen Prozesses ist, bei dem keine Wärme- oder Stoffübertragung stattfindet. Es handelt sich um einen reversiblen adiabatischen Prozess . Die Annahme, dass keine Wärmeübertragung stattfindet, ist sehr wichtig, da wir die adiabatische Näherung nur bei sehr schnellen Prozessen anwenden können . Isentroper Prozess und der erste Hauptsatz Für ein geschlossenes System können wir den ersten Hauptsatz der Thermodynamik in Bezug auf die Enthalpie schreiben : dH = dQ + Vdp oder dH = TdS + Vdp Isentroper Prozess (dQ = 0): dH = Vdp → W = H 2 – H 1 Ein isobarer Prozess ist ein thermodynamischer Prozess , bei dem der Druck des Systems konstant bleibt (p = const). Die Wärmeübertragung in das oder aus dem System verrichtet Arbeit, verändert aber auch die innere Energie des Systems. Da es Änderungen der inneren Energie (dU) und Änderungen des Systemvolumens (∆V) gibt, verwenden Ingenieure oft die Enthalpie des Systems, die wie folgt definiert ist: H = U + pV Isobarer Prozess und der erste Hauptsatz Die klassische Form des ersten Hauptsatzes der Thermodynamik ist die folgende Gleichung: dU = dQ – dW In dieser Gleichung ist dW gleich dW = pdV und ist bekannt als die Grenz Arbeit . Bei einem isobaren Prozess und dem idealen Gas wird ein Teil der dem System zugeführten Wärme für die Arbeit verwendet und ein Teil der zugeführten Wärme erhöht die innere Energie (Erhöhung der Temperatur). Daher ist es zweckmäßig, statt der inneren Energie die Enthalpie zu verwenden . Isobarer Prozess (Vdp = 0): dH = dQ → Q = H 2 – H 1 Bei konstanter Entropie , dh im isentropischen Prozess, entspricht die Enthalpieänderung der am oder vom System geleisteten Fließprozessarbeit . Der Rankine-Zyklus wird häufig in einem Druck-Volumen-Diagramm ( pV-Diagramm ) und in einem Temperatur-Entropie-Diagramm ( Ts-Diagramm ) aufgetragen . In einem Druck-Volumen-Diagramm aufgetragen , folgen die isobaren Prozesse den isobaren Linien für das Gas (den horizontalen Linien), adiabatische Prozesse bewegen sich zwischen diesen horizontalen Linien und die vom gesamten Radweg begrenzte Fläche stellt die gesamte Arbeit dar , die während eines Kreislauf. Das Temperatur-Entropie-Diagramm (Ts-Diagramm), in dem der thermodynamische Zustand durch einen Punkt auf einem Diagramm mit spezifischer Entropie (s) als horizontaler Achse und absoluter Temperatur (T) als vertikaler Achse angegeben wird. Ts-Diagramme sind ein nützliches und gebräuchliches Werkzeug, insbesondere weil sie dabei helfen, den Wärmeübergang während eines Prozesses zu visualisieren . Bei reversiblen (idealen) Prozessen ist die Fläche unter der Ts-Kurve eines Prozesses die während dieses Prozesses an das System übertragene Wärme . Im allgemeinen wird die thermischen Wirkungsgrad , η th , ein Wärmekraftmaschine ist als das Verhältnis der definierten Arbeits es tut, W , an den Wärmeeingang bei der hohen Temperatur, Q H . Der thermische Wirkungsgrad , η th , stellt den Anteil an Wärme , Q H , die konvertiert wird , zu arbeiten . Da Energie nach dem ersten Hauptsatz der Thermodynamik erhalten bleibt und Energie nicht vollständig in Arbeit umgewandelt werden kann , muss der Wärmeeintrag Q H gleich der geleisteten Arbeit W zuzüglich der Wärme, die als Abwärme Q C in die Umgebung. Daher können wir die Formel für den thermischen Wirkungsgrad umschreiben als: Dies ist eine sehr nützliche Formel, aber hier drücken wir den thermischen Wirkungsgrad mit dem ersten Hauptsatz in Form der Enthalpie aus . Typischerweise betreiben die meisten Kernkraftwerke mehrstufige Kondensationsdampfturbinen . In diesen Turbinen erhält die Hochdruckstufe Dampf (dieser Dampf ist fast gesättigter Dampf – x = 0,995 – Punkt C in der Abbildung; 6 MPa ; 275,6 ° C) von einem Dampferzeuger und führt ihn zum Feuchtigkeitsabscheider-Zwischenüberhitzer (Punkt D ). Der Dampf muss nachgewärmt werden, um Schäden zu vermeiden, die an den Schaufeln der Dampfturbine durch Dampf geringer Qualität verursacht werden könnten . Der Zwischenüberhitzer erhitzt den Dampf (Punkt D) und dann wird der Dampf zur Niederdruckstufe der Dampfturbine geleitet, wo er sich entspannt (Punkt E bis F). Der abgesaugte Dampf kondensiert dann im Kondensator und hat einen Druck weit unter dem Atmosphärendruck (Absolutdruck von0,008 MPa ) und befindet sich in einem teilweise kondensierten Zustand (Punkt F), typischerweise von einer Qualität nahe 90%. Dampferzeuger, Dampfturbine, Kondensator und Speisewasserpumpe bilden dabei eine Wärmekraftmaschine, die den Wirkungsgradbeschränkungen des zweiten Hauptsatzes der Thermodynamik unterliegt . Im Idealfall (keine Reibung, reversible Prozesse, perfektes Design) hätte diese Wärmekraftmaschine einen Carnot-Wirkungsgrad von = 1 – T kalt /T heiß = 1 – 315/549 = 42,6% wobei die Temperatur des heißen Reservoirs 275,6°C (548,7K) beträgt, beträgt die Temperatur des kalten Reservoirs 41,5°C (314,7K). Aber das Kernkraftwerk ist die eigentliche Wärmekraftmaschine , in der thermodynamische Prozesse irgendwie irreversibel sind. Sie werden nicht unendlich langsam gemacht. In realen Geräten (wie Turbinen, Pumpen und Kompressoren) verursachen mechanische Reibung und Wärmeverluste weitere Wirkungsgradverluste. Um den thermischen Wirkungsgrad des einfachsten Rankine-Zyklus (ohne Wiedererhitzen) zu berechnen, verwenden Ingenieure den ersten Hauptsatz der Thermodynamik in Bezug auf die Enthalpie und nicht in Bezug auf die innere Energie. Das erste Gesetz in Bezug auf die Enthalpie lautet: dH = dQ + Vdp In dieser Gleichung ist der Begriff Vdp eine Fließprozessarbeit. Diese Arbeit, Vdp , wird für offene Durchflusssysteme wie eine Turbine oder eine Pumpe verwendet, in denen ein „dp“ , dh eine Druckänderung , auftritt . Es gibt keine Änderungen der Kontrolllautstärke . Wie man sieht, vereinfacht diese Form des Gesetzes die Beschreibung der Energieübertragung . Bei konstantem Druck , die Enthalpieänderung ist gleich die Energie aus der Umgebung durch Erhitzen übertragen: Isobarer Prozess (Vdp = 0): dH = dQ → Q = H 2 – H 1 Bei konstanter Entropie , dh im isentropen Prozess, entspricht die Enthalpieänderung der am oder vom System geleisteten Strömungsprozessarbeit : Isentroper Prozess (dQ = 0): dH = Vdp → W = H 2 – H 1 Es ist offensichtlich, dass es bei der Analyse der beiden thermodynamischen Zyklen, die in der Energietechnik verwendet werden, sehr nützlich sein wird, dh des Brayton-Zyklus und des Rankine-Zyklus. Die Enthalpie kann durch Division durch die Masse zu einer intensiven oder spezifischen Größe gemacht werden . Ingenieure verwenden die spezifische Enthalpie in der thermodynamischen Analyse mehr als die Enthalpie selbst. Sie ist in den Dampftabellen zusammen mit dem spezifischen Volumen und der spezifischen inneren Energie aufgeführt . Der thermische Wirkungsgrad eines solchen einfachen Rankine-Zyklus und in Bezug auf spezifische Enthalpien wäre: Es ist eine sehr einfache Gleichung und zur Bestimmung des thermischen Wirkungsgrades können Sie Daten aus Dampftabellen verwenden . In modernen Kernkraftwerken beträgt der thermische Gesamtwirkungsgrad etwa ein Drittel (33 %), sodass 3000 MWth thermischer Leistung aus der Spaltungsreaktion benötigt werden, um 1000 MWe elektrische Leistung zu erzeugen . Der Grund liegt in der relativ niedrigen Dampftemperatur ( 6 MPa ; 275,6°C). Höhere Wirkungsgrade können durch Temperaturerhöhung erreicht werdendes Dampfes. Dies erfordert jedoch eine Erhöhung der Drücke in Kesseln oder Dampferzeugern. Jedoch setzen metallurgische Erwägungen solchen Drücken Obergrenzen. Im Vergleich zu anderen Energiequellen ist der thermische Wirkungsgrad von 33% nicht viel. Aber es muss beachtet werden, dass Kernkraftwerke viel komplexer sind als Kraftwerke mit fossilen Brennstoffen und es viel einfacher ist, fossile Brennstoffe zu verbrennen, als Energie aus Kernbrennstoff zu erzeugen. Unterkritische Kraftwerke mit fossilen Brennstoffen, die unter kritischem Druck (dh unter 22,1 MPa) betrieben werden, können einen Wirkungsgrad von 36–40 % erreichen. Wie bereits erwähnt, kann ein Wirkungsgrad zwischen 0 und 1 liegen. Jede Wärmekraftmaschine ist irgendwie ineffizient. Diese Ineffizienz kann auf drei Ursachen zurückgeführt werden. Es gibt mehrere Methoden, wie die thermische Effizienz des Rankine-Zyklus verbessert werden kann. Unter der Annahme, dass die maximale Temperatur durch den Druck im Reaktordruckbehälter begrenzt wird, sind diese Methoden: In den vorherigen Kapiteln haben wir angenommen, dass die Dampfexpansion isentrop ist und haben daher T 4,is als Austrittstemperatur des Gases verwendet. Diese Annahmen gelten nur bei idealen Zyklen. Die meisten Strömungswächter (Turbinen, Verdichter, Düsen) arbeiten unter adiabatischen Bedingungen, sind aber nicht wirklich isentrop, sondern werden für Berechnungszwecke eher als isentrop idealisiert. Wir definieren die Parameter η T , η P , η N , als Verhältnis der realen Arbeit eines Geräts zu der Arbeit eines Geräts bei Betrieb unter isentropen Bedingungen (im Falle einer Turbine). Dieses Verhältnis ist als isentropischer Turbinen-/Pumpen-/Düsenwirkungsgrad bekannt . Diese Parameter beschreiben, wie effizient sich eine Turbine, ein Verdichter oder eine Düse einem entsprechenden isentropen Gerät annähert. Dieser Parameter reduziert den Gesamtwirkungsgrad und die Arbeitsleistung. Für Turbinen beträgt der Wert von η T typischerweise 0,7 bis 0,9 (70–90%). Siehe auch: Isentroper Prozess Berechnung: 1) Da wir die genaue Dampfqualität des Abdampfes nicht kennen, müssen wir diesen Parameter ermitteln. Zustand 4 wird durch den Druck p 4 = 0,008 MPa und die Konstante der spezifischen Entropie für die isentrope Expansion (s 3 = s 4 = 5,89 kJ/kgK für 6 MPa ) festgelegt. Die spezifische Entropie von gesättigtem Flüssigwasser (x=0) und Trockendampf (x=1) kann den Dampftabellen entnommen werden . Bei Nassdampf lässt sich die tatsächliche Entropie aus der Dampfqualität x und den spezifischen Entropien von gesättigtem Flüssigwasser und Trockendampf berechnen: s 4 = s v x + (1 – x ) s l wo s 4 = Entropie des Nassdampfes (J/kg K) = 5,89 kJ/kgK s v = Entropie von „trockenem“ Dampf (J/kg K) = 8,227 kJ/kgK (für 0,008 MPa) s l = Entropie von gesättigtem flüssigem Wasser (J/kg K) = 0,592 kJ/kgK (für 0,008 MPa) Aus dieser Gleichung ergibt sich für die Dampfqualität: x 4 = ( s 4 – s l ) / ( s v – s l ) = (5,89 bis 0,592) / (8,227 bis 0,592) = 0,694 = 69,4% 2) Die Enthalpie für den Zustand 3 kann direkt aus Dampftabellen entnommen werden, während die Enthalpie für den Zustand 4 anhand der Dampfqualität berechnet werden muss: h 3, v = 2785 kJ/kg h 4, nass = h 4,v x + (1 – x ) h 4,l = 2576 . 0,694 + (1 – 0,694) . 174 = 1787 + 53,2 = 1840 kJ/kg Dann wird die Arbeit durch den Dampf gemacht, W T, ist W T = Δh = 945 kJ/kg 3) Die Enthalpie für Zustand 1 kann direkt aus den Dampftabellen ausgewählt werden: h 1, l = 174 kJ/kg Zustand 2 wird durch den Druck p 2 = 6,0 MPa und die Konstante der spezifischen Entropie für die isentrope Kompression (s 1 = s 2 = 0,592 kJ/kgK für 0,008 MPa ) festgelegt. Für diese Entropie s 2 = 0,592 kJ/kgK und p 2 = 6,0 MPa finden wir h 2, unterkühlt in Dampftabellen für komprimiertes Wasser (mittels Interpolation zwischen zwei Zuständen). h 2, unterkühlt = 179,7 kJ/kg Dann erfolgt die Arbeit der Pumpen, W P, ist W P = Δh = 5,7 kJ/kg 4) Die Enthalpiedifferenz zwischen (2 → 3), die der im Dampferzeuger zugeführten Nettowärme entspricht, beträgt einfach: Q add = h 3, v – h 2, unterkühlt = 2785 – 179,7 = 2605,3 kJ/kg Beachten Sie, dass in diesem Zyklus keine Wärmeregeneration stattfindet. Andererseits wird die meiste Wärme für die Verdampfungsenthalpie (dh für die Phasenänderung) zugeführt. 5) Dampferzeuger, Dampfturbine, Kondensator und Speisewasserpumpe bilden dabei eine Wärmekraftmaschine, die den Wirkungsgradbeschränkungen des zweiten Hauptsatzes der Thermodynamik unterliegt . Im Idealfall (keine Reibung, reversible Prozesse, perfektes Design) hätte diese Wärmekraftmaschine einen Carnot-Wirkungsgrad von η Carnot = 1 – T kalt /T heiß = 1 – 315/549 = 42,6% wobei die Temperatur des heißen Reservoirs 275,6 °C (548,7 K) beträgt, beträgt die Temperatur des kalten Reservoirs 41,5 °C (314,7 K). Der thermodynamische Wirkungsgrad dieses Kreislaufs lässt sich nach folgender Formel berechnen: alsoIsentroper Prozess
Isobarer Prozess
Rankine-Zyklus – pV, Ts-Diagramm
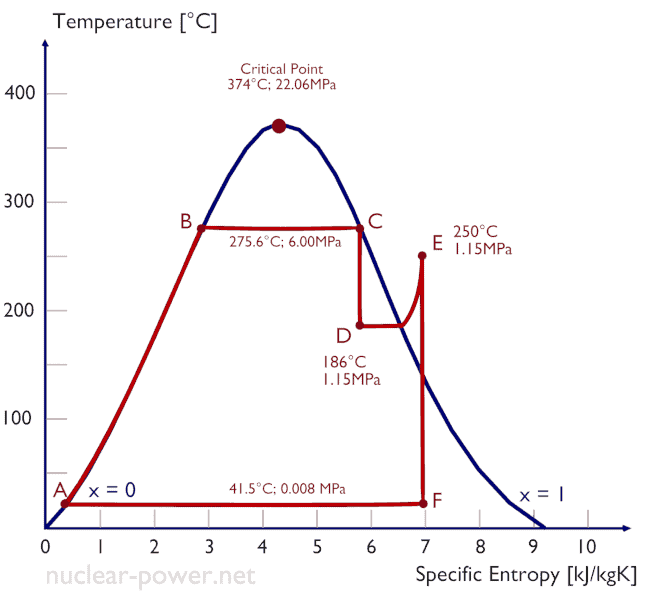
Thermische Effizienz des Rankine-Zyklus
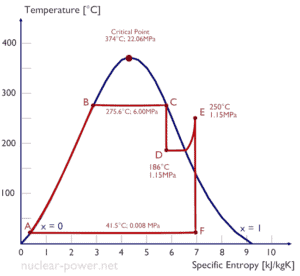
Ursachen von Ineffizienz
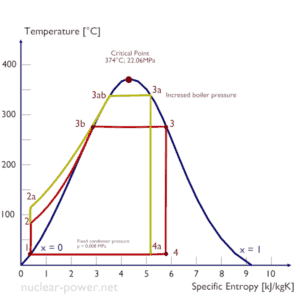
Verbesserung der thermischen Effizienz – Rankine-Zyklus
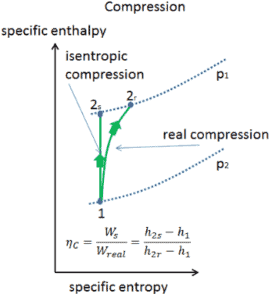
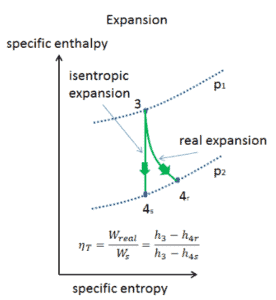
Isentroper Wirkungsgrad – Turbine, Pumpe
Rankine-Zyklus – Problem mit Lösung
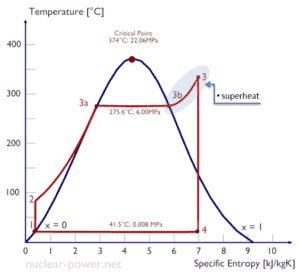
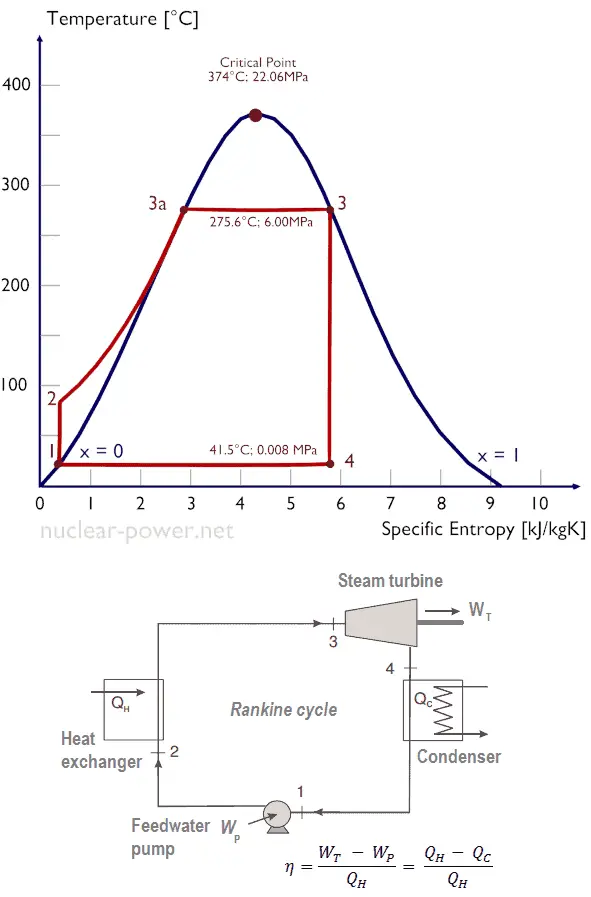 Nehmen wir den Rankine-Zyklus an , der einer der häufigsten thermodynamischen Kreisläufe in Wärmekraftwerken ist. Gehen Sie in diesem Fall von einem einfachen Kreislauf ohne Zwischenüberhitzung und ohne mit Sattdampf (Trockendampf) betriebener Kondensationsdampfturbine aus. In diesem Fall arbeitet die Turbine im stationären Zustand mit Einlassbedingungen von 6 MPa, t = 275,6°C, x = 1 (Punkt 3). Dampf verlässt diese Turbinenstufe mit einem Druck von 0,008 MPa, 41,5°C und x = ??? (Punkt 4).
Nehmen wir den Rankine-Zyklus an , der einer der häufigsten thermodynamischen Kreisläufe in Wärmekraftwerken ist. Gehen Sie in diesem Fall von einem einfachen Kreislauf ohne Zwischenüberhitzung und ohne mit Sattdampf (Trockendampf) betriebener Kondensationsdampfturbine aus. In diesem Fall arbeitet die Turbine im stationären Zustand mit Einlassbedingungen von 6 MPa, t = 275,6°C, x = 1 (Punkt 3). Dampf verlässt diese Turbinenstufe mit einem Druck von 0,008 MPa, 41,5°C und x = ??? (Punkt 4).
η th = (945 – 5,7) / 2605.3 = 0,361 = 36,1%