¿Qué es la entalpía?
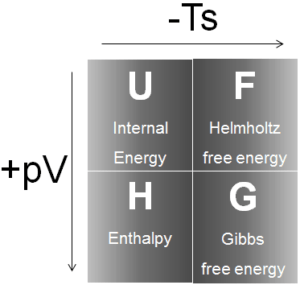
En termodinámica, la entalpía es la medida de energía en un sistema termodinámico. Es la cantidad termodinámica equivalente al contenido de calor total de un sistema. La entalpía se define como la suma de la energía interna E más el producto de la presión py el volumen V. En muchos análisis termodinámicos aparece la suma de la energía interna U y el producto de la presión py el volumen V, por lo tanto, es conveniente para dar a la combinación un nombre, entalpía y un símbolo distintivo, H.
La entalpía es la expresión preferida de los cambios de energía del sistema en muchas mediciones químicas, biológicas y físicas a presión constante . Es tan útil que está tabulado en las tablas de vapor junto con un volumen específico y una energía interna específica . Es debido al hecho, simplifica la descripción de la transferencia de energía . A presión constante, el cambio de entalpía es igual a la energía transferida desde el medio ambiente a través del calentamiento (Q = H 2 – H 1 ) u otro trabajo que no sea el trabajo de expansión. Para un proceso de presión variable, la diferencia en entalpía no es tan obvia.
Entalpía en unidades extensas
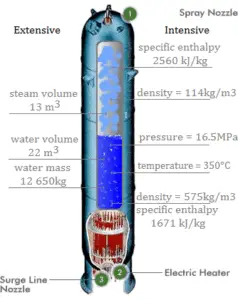
H = U + pV
La entalpía es una cantidad extensa, depende del tamaño del sistema o de la cantidad de sustancia que contiene. La unidad de entalpía del SI es el joule (J). Es la energía contenida dentro del sistema, excluyendo la energía cinética de movimiento del sistema como un todo y la energía potencial del sistema como un todo debido a los campos de fuerza externos. Es la cantidad termodinámica equivalente al contenido de calor total de un sistema.
Por otro lado, la energía puede almacenarse en los enlaces químicos entre los átomos que forman las moléculas. Este almacenamiento de energía a nivel atómico incluye energía asociada con estados orbitales de electrones, espín nuclear y fuerzas de unión en el núcleo.
La entalpía está representada por el símbolo H , y el cambio en la entalpía en un proceso es H 2 – H 1 .
Hay expresiones en términos de variables más familiares como temperatura y presión :
dH = C p dT + V (1-αT) dp
Donde C p es la capacidad calorífica a presión constante y α es el coeficiente de expansión térmica (cúbica). Para gas ideal αT = 1 y por lo tanto:
dH = C p dT
Ejemplo: Pistón sin fricción – Calor – Entalpía
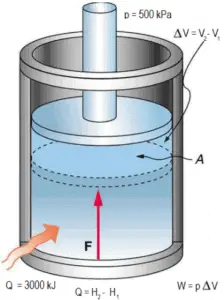
Un pistón sin fricción se utiliza para proporcionar una presión constante de 500 kPa en un cilindro que contiene vapor de agua ( vapor sobrecalentado ) de un volumen de 2 m 3 a 500 K . Calcule la temperatura final, si se agregan 3000 kJ de calor .
Solución:
Usando tablas de vapor , sabemos que la entalpía específica de dicho vapor (500 kPa; 500 K) es de aproximadamente 2912 kJ / kg . Dado que en esta condición el vapor tiene una densidad de 2.2 kg / m 3 , entonces sabemos que hay alrededor de 4.4 kg de vapor en el pistón a una entalpía de 2912 kJ / kg x 4.4 kg = 12812 kJ .
Cuando usamos simplemente Q = H 2 – H 1 , la entalpía de vapor resultante será:
H 2 = H 1 + Q = 15812 kJ
De las mesas de vapor , dicho vapor sobrecalentado (15812 / 4.4 = 3593 kJ / kg) tendrá una temperatura de 828 K (555 ° C) . Como en esta entalpía el vapor tiene una densidad de 1,31 kg / m 3 , es obvio que se ha expandido aproximadamente 2,2 / 1,31 = 1,67 (+ 67%). Por lo tanto, el volumen resultante es 2 m 3 x 1.67 = 3.34 m 3 y ∆V = 3.34 m 3 – 2 m 3 = 1.34 m 3 .
La parte p∆V de la entalpía, es decir, el trabajo realizado es:
W = p∆V = 500 000 Pa x 1.34 m 3 = 670 kJ
Entalpía en Unidades Intensivas – Entalpía Específica
La entalpía se puede convertir en una variable intensiva o específica dividiéndola por la masa . Los ingenieros usan la entalpía específica en el análisis termodinámico más que la entalpía misma. La entalpía específica (h) de una sustancia es su entalpía por unidad de masa. Es igual a la entalpía total (H) dividida por la masa total (m).
h = H / m
dónde:
h = entalpía específica (J / kg)
H = entalpía (J)
m = masa (kg)
Tenga en cuenta que la entalpía es la cantidad termodinámica equivalente al contenido total de calor de un sistema. La entalpía específica es igual a la energía interna específica del sistema más el producto de presión y volumen específico .
h = u + pv
En general, la entalpía es una propiedad de una sustancia , como la presión, la temperatura y el volumen, pero no se puede medir directamente. Normalmente, la entalpía de una sustancia se da con respecto a algún valor de referencia. Por ejemplo, la entalpía específica de agua o vapor se da usando la referencia de que la entalpía específica de agua es cero a 0.01 ° C y presión atmosférica normal , donde h L = 0.00 kJ / kg . Sin embargo, el hecho de que se desconozca el valor absoluto de la entalpía específica no es un problema, porque es el cambio en la entalpía específica (∆h) y no el valor absoluto lo que es importante en los problemas prácticos.
Entalpía en reacciones químicas
La entalpía es ampliamente utilizada también en química. Las reacciones químicas están determinadas por las leyes de la termodinámica . En termodinámica, la energía interna de un sistema es la energía contenida dentro del sistema, excluyendo la energía cinética de movimiento del sistema en su conjunto y la energía potencial del sistema en su conjunto debido a los campos de fuerza externos. La entalpía de una reacción química se define como el cambio de entalpía observado en un componente de un sistema termodinámico cuando un mol de sustancia reacciona por completo.
Como la mayoría de las reacciones químicas en el laboratorio son procesos de presión constante, podemos escribir el cambio en la entalpía (también conocida como entalpía de reacción) para una reacción. La entalpía de reacción puede ser positiva o negativa o cero, dependiendo de si el calor se gana o se pierde o no se pierde o gana calor. En una reacción endotérmica , los productos tienen más energía química almacenada que los reactivos. En una reacción exotérmica , lo contrario es cierto. Los productos tienen menos energía química almacenada que los reactivos. El exceso de energía generalmente se libera a los alrededores cuando ocurre la reacción.
En las reacciones químicas , la energía se almacena en los enlaces químicos entre los átomos que forman las moléculas. El almacenamiento de energía a nivel atómico incluye energía asociada con estados orbitales de electrones. Ya sea que una reacción química absorba o libere energía, no hay un cambio general en la cantidad de energía durante la reacción. Eso se debe a la ley de conservación de la energía , que establece que:
La energía no puede ser creada o destruida . La energía puede cambiar de forma durante una reacción química .
Entalpía de vaporización
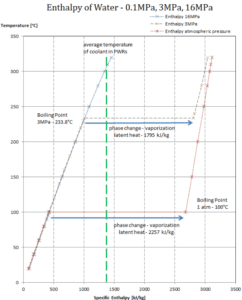
En general, cuando un material cambia de fase de sólido a líquido, o de líquido a gas, una cierta cantidad de energía está involucrada en este cambio de fase. En caso de cambio de fase de líquido a gas, esta cantidad de energía se conoce como entalpía de vaporización , (símbolo ∆H vap ; unidad: J) también conocido como calor (latente) de vaporización o calor de evaporación. El calor latente es la cantidad de calor agregado o eliminado de una sustancia para producir un cambio de fase. Esta energía descompone las fuerzas de atracción intermoleculares, y también debe proporcionar la energía necesaria para expandir el gas (el trabajo pΔV) Cuando se agrega calor latente, no ocurre cambio de temperatura. La entalpía de la vaporización es una función de la presión a la que tiene lugar esa transformación.
Calor latente de vaporización – agua a 0.1 MPa (presión atmosférica)
h lg = 2257 kJ / kg
Calor latente de vaporización: agua a 3 MPa (presión dentro de un generador de vapor)
h lg = 1795 kJ / kg
Calor latente de vaporización: agua a 16 MPa (presión dentro de un presurizador )
h lg = 931 kJ / kg
El calor de vaporización disminuye al aumentar la presión, mientras que aumenta el punto de ebullición . Se desvanece por completo en un cierto punto llamado punto crítico . Por encima del punto crítico, las fases líquida y de vapor son indistinguibles, y la sustancia se llama fluido supercrítico .
El calor de vaporización es el calor requerido para vaporizar completamente una unidad de líquido saturado (o condensar una unidad de masa de vapor saturado) y es igual a h lg = h g – h l .
El calor necesario para derretir (o congelar) una unidad de masa en la sustancia a presión constante es el calor de fusión y es igual a h sl = h l – h s , donde h s es la entalpía del sólido saturado y h l Es la entalpía del líquido saturado.
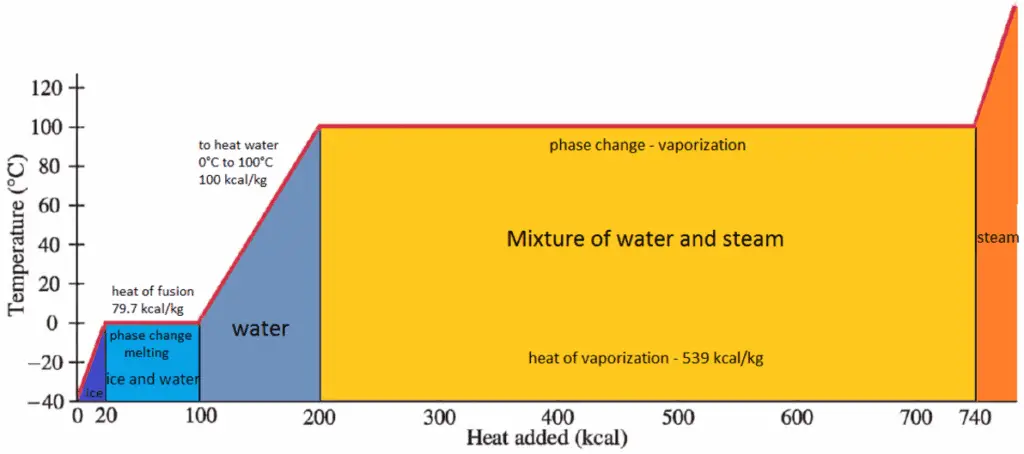
Entalpía específica de vapor húmedo
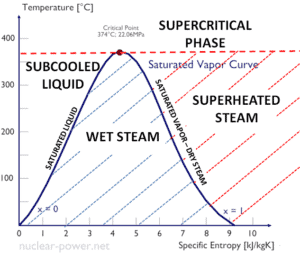 La entalpía específica de agua líquida saturada (x = 0) y vapor seco (x = 1) se puede recoger de las mesas de vapor. En caso de vapor húmedo , la entalpía real se puede calcular con la calidad del vapor, x , y las entalpías específicas de agua líquida saturada y vapor seco:
La entalpía específica de agua líquida saturada (x = 0) y vapor seco (x = 1) se puede recoger de las mesas de vapor. En caso de vapor húmedo , la entalpía real se puede calcular con la calidad del vapor, x , y las entalpías específicas de agua líquida saturada y vapor seco:
h húmedo = h s x + (1 – x) h l
dónde
h húmedo = entalpía de vapor húmedo (J / kg)
h s = entalpía de vapor “seco” (J / kg)
h l = entalpía de agua líquida saturada (J / kg)
Como se puede ver, el vapor húmedo siempre tendrá una entalpía más baja que el vapor seco.
Ejemplo:
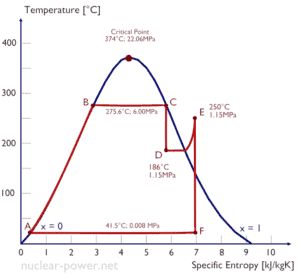
Una etapa de alta presión de la turbina de vapor funciona en estado estacionario con condiciones de entrada de 6 MPa, t = 275.6 ° C, x = 1 (punto C). El vapor sale de esta etapa de la turbina a una presión de 1,15 MPa, 186 ° C yx = 0,87 (punto D). Calcule la diferencia de entalpía entre estos dos estados.
La entalpía para el estado C puede seleccionarse directamente de las tablas de vapor, mientras que la entalpía para el estado D debe calcularse utilizando la calidad del vapor:
h 1, húmedo = 2785 kJ / kg
h 2, húmedo = h 2, s x + (1 – x) h 2, l = 2782. 0.87 + (1 – 0.87). 790 = 2420 + 103 = 2523 kJ / kg
Δh = 262 kJ / kg
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.