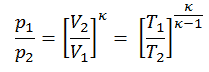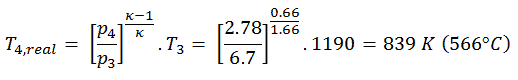Exemple d’expansion adiabatique
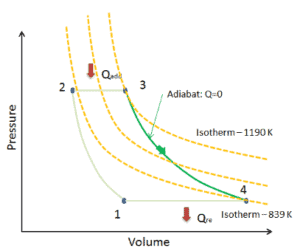
Supposons une expansion adiabatique d’hélium ( 3 → 4 ) dans une turbine à gaz . L’hélium se comportant presque comme un gaz parfait , utilisez la loi du gaz parfait pour calculer la température de sortie du gaz ( T 4, réel ). Dans ces turbines, l’étage haute pression reçoit du gaz (point 3 sur la figure; p 3 = 6,7 MPa ; T 3 = 1190 K (917 ° C)) d’un échangeur de chaleur et l’évacue vers un autre échangeur de chaleur, où la pression de sortie est p 4 = 2,78 MPa (point 4) .
Solution:
La température de sortie du gaz, T 4, réel , peut être calculée en utilisant la relation p, V, T pour le processus adiabatique. Notez que, c’est la même relation que pour le processus isentropique , donc les résultats doivent être identiques. Dans ce cas, nous calculons l’expansion pour différentes turbines à gaz (moins efficaces) comme dans le cas d’une expansion isentropique dans une turbine à gaz.
Dans cette équation, le facteur pour l’hélium est égal à κ = c p / c v = 1,66 . Il résulte de l’équation précédente que la température de sortie du gaz, T 4, réel , est:
Voir aussi: la relation de Mayer
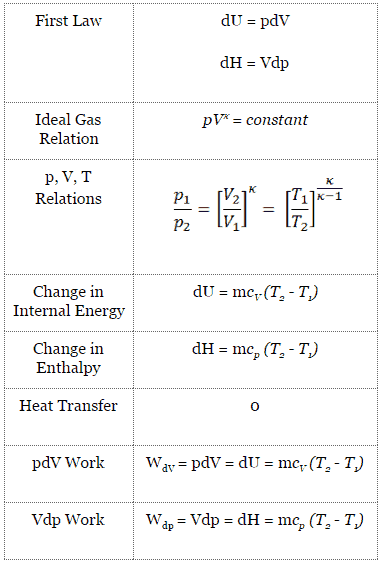
Voir aussi: Première loi de la thermodynamique
Voir aussi: Loi sur les gaz parfaits
Voir aussi: Qu’est-ce que l’enthalpie
Processus adiabatique dans les turbines à gaz
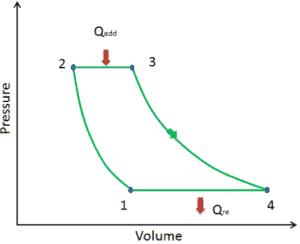
Supposons le cycle de Brayton qui décrit le fonctionnement d’un moteur thermique à pression constante . Les moteurs à turbine à gaz modernes et les moteurs à réaction à respiration aérodynamique suivent également le cycle de Brayton.
Le cycle de Brayton comprend quatre processus thermodynamiques. Deux processus adiabatiques et deux processus isobares.
- compression adiabatique – l’air ambiant est aspiré dans le compresseur, où il est mis sous pression (1 → 2). Le travail requis pour le compresseur est donné par W C = H 2 – H 1 .
- addition de chaleur isobare – l’air comprimé traverse ensuite une chambre de combustion, où le combustible est brûlé et l’air ou un autre milieu est chauffé (2 → 3). Il s’agit d’un processus à pression constante, car la chambre est ouverte pour entrer et sortir. La chaleur nette ajoutée est donnée par Q add = H 3 – H 2
- expansion adiabatique – l’air chauffé sous pression se détend ensuite sur la turbine, cède son énergie. Le travail effectué par turbine est donné par W T = H 4 – H 3
- rejet de chaleur isobare – la chaleur résiduelle doit être rejetée afin de fermer le cycle. La chaleur nette rejetée est donnée par Q re = H 4 – H 1
Comme on peut le voir, nous pouvons décrire et calculer (par exemple l’ efficacité thermique ) de tels cycles (de même pour le cycle de Rankine ) en utilisant des enthalpies .
Voir aussi: Efficacité thermique du cycle de Brayton
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci