La chaleur latente de vaporisation
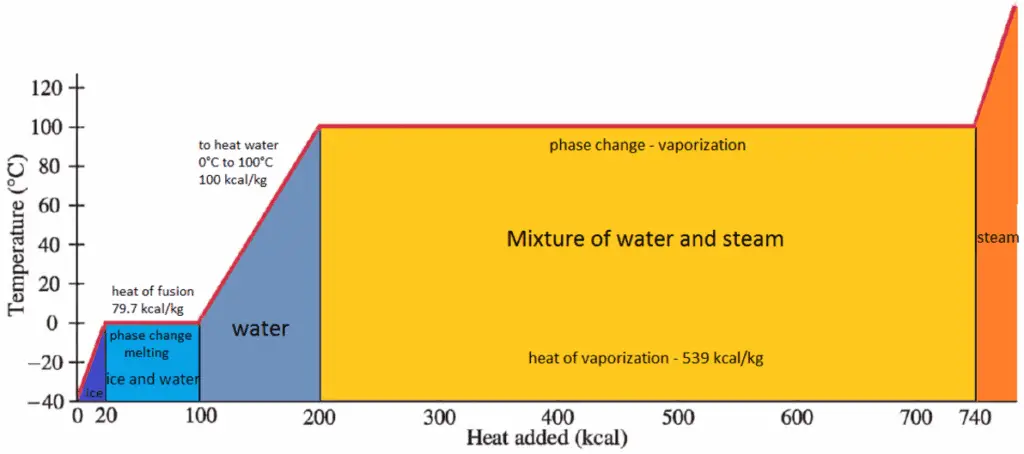
En général, lorsqu’un matériau passe de phase à solide ou de liquide à gaz, une certaine quantité d’énergie intervient dans ce changement de phase. En cas de changement de phase liquide en phase gazeuse, cette quantité d’énergie est appelée enthalpie de vaporisation (symbole ∆H vap ; unité: J), également appelée chaleur de vaporisation (latente) ou chaleur d’évaporation. La chaleur latente est la quantité de chaleur ajoutée à une substance ou retirée de celle-ci pour produire un changement de phase. Cette énergie décompose les forces d’attraction intermoléculaires et doit également fournir l’énergie nécessaire à la détente du gaz (le travail pΔV). Lorsque de la chaleur latente est ajoutée, aucun changement de température ne se produit. L’enthalpie de vaporisation est fonction de la pression à laquelle se produit cette transformation.
Chaleur de vaporisation latente – eau à 0,1 MPa (pression atmosphérique)
h lg = 2257 kJ / kg
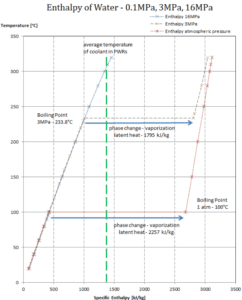
Chaleur latente de vaporisation – eau à 3 MPa (pression à l’intérieur d’un générateur de vapeur)
h lg = 1795 kJ / kg
Chaleur latente de vaporisation – eau à 16 MPa (pression à l’intérieur d’un pressuriseur )
h lg = 931 kJ / kg
La chaleur de vaporisation diminue avec l’augmentation de la pression, tandis que le point d’ébullition augmente. Il disparaît complètement à un certain point appelé le point critique . Au-dessus du point critique, les phases liquide et vapeur ne peuvent pas être distinguées et la substance est appelée fluide supercritique .
La chaleur de vaporisation est la chaleur nécessaire pour vaporiser complètement une unité de liquide saturé (ou condenser une unité de masse de vapeur saturée) et elle est égale à h lg = h g – h l .
La chaleur nécessaire pour fondre (ou congeler) une unité de masse à la substance à pression constante est la chaleur de fusion et est égale à h sl = h l – h s , où h s est l’enthalpie du solide saturé et h l est l’enthalpie du liquide saturé.
Chaleur latente de vaporisation – eau à 0,1 MPa. Partie dominante de la chaleur absorbée.
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci