Thermodynamische Prozesse
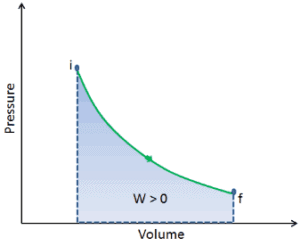 Ein thermodynamischer Prozess ist definiert als ein Wechsel von einem Gleichgewichtsmakrostaten zu einem anderen Makrostaten. Der Anfangs- und Endzustand sind die bestimmenden Elemente des Prozesses. Während eines solchen Prozesses geht ein System von einem Anfangszustand i aus , der durch einen Druck p i , ein Volumen V i und eine Temperatur T i beschrieben wird , und geht durch verschiedene quasistatische Zustände in einen Endzustand f über , der durch einen Druck p f , a beschrieben wird Volumen V f und eine Temperatur T f . In diesem ProzessEnergie kann vom oder in das System übertragen werden und auch Arbeiten können von oder am System ausgeführt werden. Ein Beispiel für einen thermodynamischen Prozess ist das Erhöhen des Drucks eines Gases bei konstanter Temperatur. Im folgenden Abschnitt finden Sie Beispiele für thermodynamische Prozesse, die für die Konstruktion von Wärmekraftmaschinen von höchster Bedeutung sind .
Ein thermodynamischer Prozess ist definiert als ein Wechsel von einem Gleichgewichtsmakrostaten zu einem anderen Makrostaten. Der Anfangs- und Endzustand sind die bestimmenden Elemente des Prozesses. Während eines solchen Prozesses geht ein System von einem Anfangszustand i aus , der durch einen Druck p i , ein Volumen V i und eine Temperatur T i beschrieben wird , und geht durch verschiedene quasistatische Zustände in einen Endzustand f über , der durch einen Druck p f , a beschrieben wird Volumen V f und eine Temperatur T f . In diesem ProzessEnergie kann vom oder in das System übertragen werden und auch Arbeiten können von oder am System ausgeführt werden. Ein Beispiel für einen thermodynamischen Prozess ist das Erhöhen des Drucks eines Gases bei konstanter Temperatur. Im folgenden Abschnitt finden Sie Beispiele für thermodynamische Prozesse, die für die Konstruktion von Wärmekraftmaschinen von höchster Bedeutung sind .
Arten von thermodynamischen Prozessen
Reversibler Prozess
In der Thermodynamik wird ein reversibler Prozess als ein Prozess definiert, der durch Induzieren infinitesimaler Änderungen an einer Eigenschaft des Systems umgekehrt werden kann und dabei weder das System noch die Umgebung verändert. Während des reversiblen Prozesses nimmt die Entropie des Systems nicht zu und das System befindet sich im thermodynamischen Gleichgewicht mit seiner Umgebung.
Irreversibler Prozess
In der Thermodynamik wird ein irreversibler Prozess als ein Prozess definiert, der nicht umgekehrt werden kann, ein Prozess, der nicht sowohl das System als auch die Umgebung in ihren ursprünglichen Zustand zurückversetzen kann.
Während des irreversiblen Prozesses nimmt die Entropie des Systems zu .
Zyklischer Prozess
Ein Prozess, der ein System schließlich in seinen Ausgangszustand zurückversetzt, wird als zyklischer Prozess bezeichnet . Am Ende eines Zyklus haben alle Eigenschaften den gleichen Wert wie zu Beginn. Für ein solches Verfahren, das Endzustand ist der gleiche wie der Anfangszustand , so dass die gesamte innere Energie Änderung Null sein muß.
Es muss beachtet werden, dass nach dem zweiten Hauptsatz der Thermodynamik nicht die gesamte Wärme, die einem Kreislauf zugeführt wird, in einen gleichen Arbeitsaufwand umgewandelt werden kann, sondern dass eine gewisse Wärmeabgabe stattfinden muss. Der thermische Wirkungsgrad , η th , ein Wärmekraftmaschine als das Verhältnis der Arbeits es tut, W , an den Wärmeeingang bei der hohen Temperatur, Q H . η th = W / Q – H .
Siehe auch: Reversibler Prozess
Siehe auch: Irreversibler Prozess
Siehe auch: Zyklischer Prozess
Isentropischer Prozess
Ein isentropischer Prozess ist ein thermodynamischer Prozess , bei dem die Entropie des Fluids oder Gases konstant bleibt. Dies bedeutet, dass der isentrope Prozess ein Sonderfall eines adiabatischen Prozesses ist, bei dem keine Wärme- oder Materieübertragung stattfindet. Es ist ein reversibler adiabatischer Prozess . Ein isentropischer Prozess kann auch als konstanter Entropieprozess bezeichnet werden. In der Technik ist ein solcher idealisierter Prozess sehr nützlich für den Vergleich mit realen Prozessen.
Siehe auch: Isentropischer Prozess
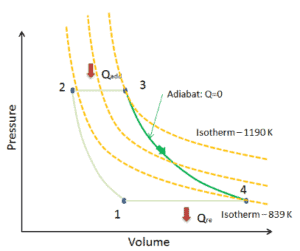
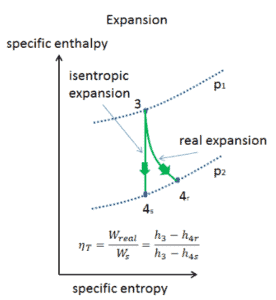
PV-Diagramm einer isentropischen Expansion von Helium (3 → 4) in einer Gasturbine.
Adiabatischer Prozess
Ein adiabatischer Prozess ist ein thermodynamischer Prozess , bei dem keine Wärmeübertragung in das System oder aus dem System erfolgt (Q = 0). Das System kann als perfekt isoliert angesehen werden . In einem adiabatischen Prozess wird Energie nur als Arbeit übertragen. Die Annahme, dass keine Wärmeübertragung stattfindet, ist sehr wichtig, da wir die adiabatische Näherung nur in sehr schnellen Prozessen verwenden können . Bei diesen schnellen Prozessen bleibt nicht genügend Zeit für die Übertragung von Energie als Wärme zum oder vom System.
In realen Geräten (wie Turbinen, Pumpen und Kompressoren) treten Wärmeverluste und Verluste im Verbrennungsprozess auf. Diese Verluste sind jedoch im Vergleich zum Gesamtenergiefluss normalerweise gering, und wir können einige thermodynamische Prozesse durch den adiabatischen Prozess approximieren.
Siehe auch: Adiabatischer Prozess
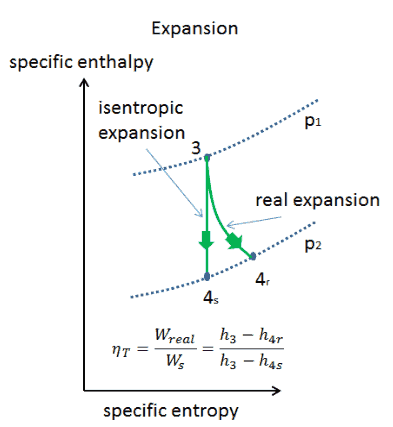
Isentropische vs. adiabatische Expansion.
Isothermer Prozess
Ein isothermer Prozess ist ein thermodynamischer Prozess , bei dem die Temperatur des Systems konstant bleibt (T = const). Die Wärmeübertragung in oder aus dem System muss typischerweise mit einer so langsamen Geschwindigkeit erfolgen, um sich durch Wärmeaustausch kontinuierlich an die Temperatur des Speichers anzupassen. In jedem dieser Zustände bleibt das thermische Gleichgewicht erhalten.
Für ein ideales Gas und einen polytropischen Prozess entspricht der Fall n = 1 einem isothermen Prozess (konstante Temperatur). Im Gegensatz zum adiabatischen Prozess , bei dem n = κ und ein System keine Wärme mit seiner Umgebung austauscht (Q = 0; ∆T ≠ 0 ) , ändert sich bei einem isothermen Prozess die innere Energie nicht (aufgrund von ∆T = 0) ) und daher ΔU = 0 (für ideale Gase) und Q ≠ 0. Ein adiabatischer Prozess ist nicht notwendigerweise ein isothermer Prozess, noch ist ein isothermer Prozess notwendigerweise adiabatisch.
Siehe auch: Isothermer Prozess
Boyle-Mariotte-Gesetz. Bei einer festen Gasmasse bei konstanter Temperatur ist das Volumen umgekehrt proportional zum Druck. Quelle: grc.nasa.gov Die NASA-Urheberrechtsrichtlinie besagt, dass „NASA-Material nicht urheberrechtlich geschützt ist, sofern nicht anders angegeben“.
Isobarer Prozess
Ein isobarer Prozess ist ein thermodynamischer Prozess , bei dem der Druck des Systems konstant bleibt (p = const). Die Wärmeübertragung in oder aus dem System funktioniert zwar, verändert aber auch die innere Energie des Systems.
Da sich die innere Energie (dU) und das Systemvolumen (∆V) ändern, verwenden Ingenieure häufig die Enthalpie des Systems, die wie folgt definiert ist:
H = U + pV
In vielen thermodynamischen Analysen ist es zweckmäßig, die Enthalpie anstelle der inneren Energie zu verwenden. Besonders im Fall des ersten Hauptsatzes der Thermodynamik .
In der Technik basieren beide sehr wichtigen thermodynamischen Kreisprozessen ( Brayton- und Rankine-Zyklus ) auf zwei isobaren Prozessen , daher ist die Untersuchung dieses Prozesses für Kraftwerke von entscheidender Bedeutung.
Siehe auch: Isobarer Prozess
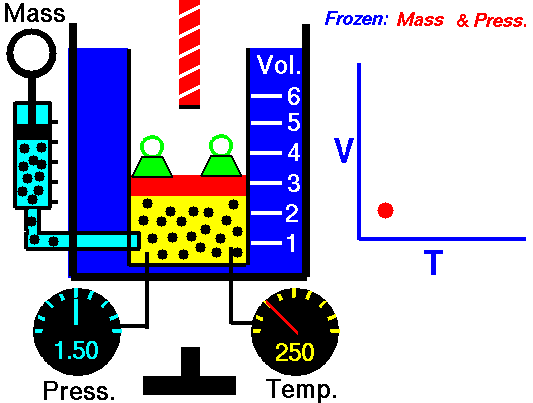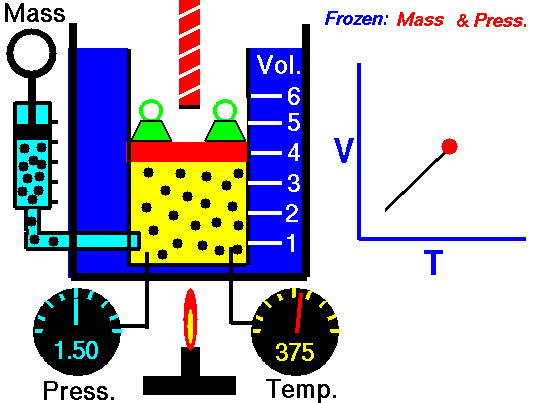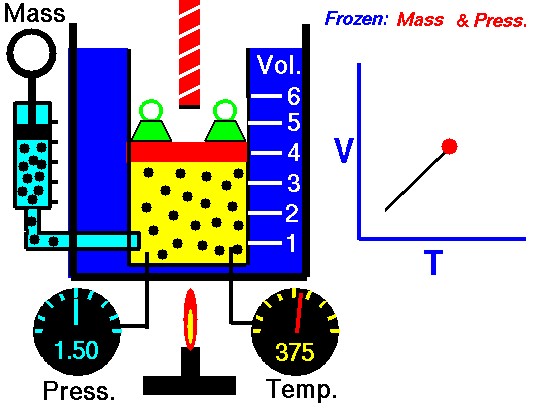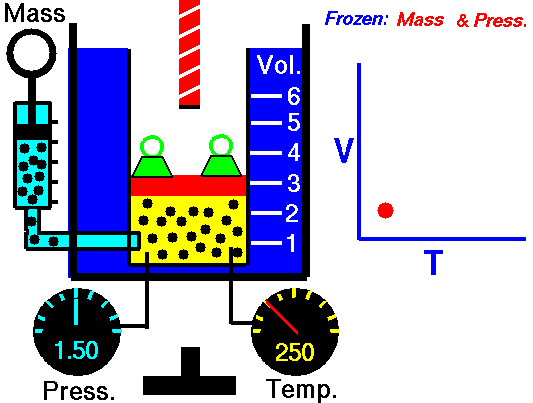
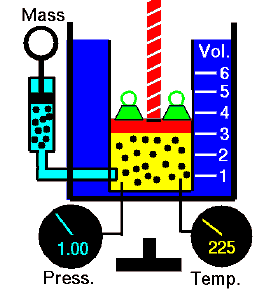
Bei einer festen Gasmasse bei konstantem Druck ist das Volumen direkt proportional zur Kelvin-Temperatur. Quelle: grc.nasa.gov Die NASA-Urheberrechtsrichtlinie besagt, dass „NASA-Material nicht urheberrechtlich geschützt ist, sofern nicht anders angegeben“.
Isochorischer Prozess
Ein isochorer Prozess ist ein thermodynamischer Prozess, bei dem das Volumen des geschlossenen Systems konstant bleibt (V = const). Es beschreibt das Verhalten von Gas im Behälter, das nicht verformt werden kann. Da das Volumen konstant bleibt, funktioniert der Wärmeübergang in oder aus dem System nicht mit p∆V , sondern ändert nur die innere Energie (die Temperatur) des Systems.
In der Konstruktion von Verbrennungsmotoren sind isochore Prozesse für ihre thermodynamischen Kreisprozessen (Otto- und Dieselzyklus) sehr wichtig, daher ist die Untersuchung dieses Prozesses für die Automobiltechnik von entscheidender Bedeutung.
Siehe auch: Isochorischer Prozess
Bei einer festen Gasmasse bei konstantem Volumen ist der Druck direkt proportional zur Kelvin-Temperatur.
Polytropischer Prozess
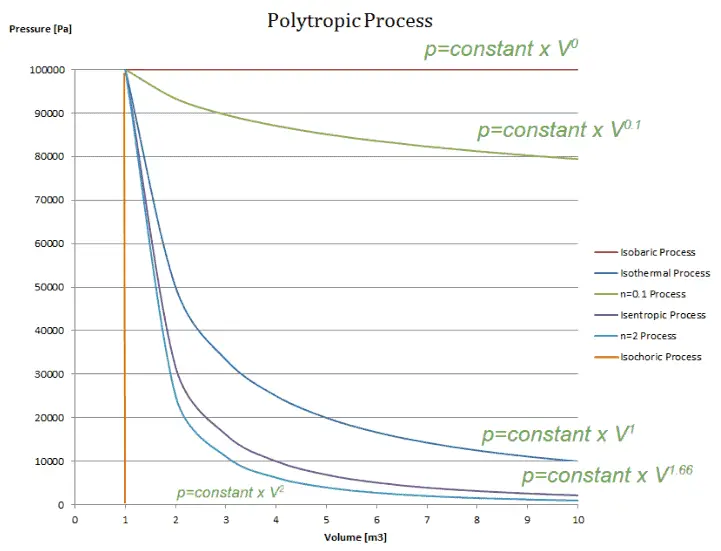
Ein polytropischer Prozess ist ein thermodynamischer Prozess, der durch die folgende Gleichung ausgedrückt werden kann:
pV n = konstant
Der polytrope Prozess kann die Gasexpansion und -kompression beschreiben, die die Wärmeübertragung einschließen . Der Exponent n ist als Polytropenindex bekannt und kann je nach Prozess einen beliebigen Wert von 0 bis ∞ annehmen.
Siehe auch: Polytropischer Prozess
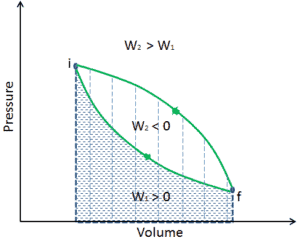
Polytrope Prozesse mit verschiedenen polytropischen Indizes.
Drosselungsprozess – Isenthalpischer Prozess
Ein Drosselprozess ist ein thermodynamischer Prozess , bei dem die Enthalpie des Gases oder Mediums konstant bleibt (h = const) . Tatsächlich ist der Drosselungsprozess einer der isenthalpischen Prozesse . Während des Drosselvorgangs werden keine Arbeiten von oder am System ausgeführt (dW = 0), und normalerweise findet keine Wärmeübertragung ( adiabatisch ) vom oder in das System (dQ = 0) statt. Andererseits kann der Drosselungsprozess nicht isentrop sein, sondern ist ein grundsätzlich irreversibler Prozess . Eigenschaften des Drosselungsprozesses:
- Keine Arbeitsübertragung
- Keine Wärmeübertragung
- Irreversibler Prozess
- Isenthalpischer Prozess
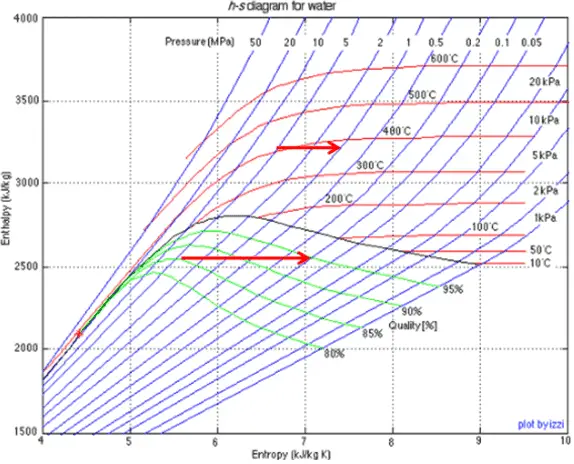
Das Drosseln des feuchten Dampfes ist auch mit der Erhaltung der Enthalpie verbunden . In diesem Fall führt eine Druckreduzierung jedoch zu einer Erhöhung der Dampfqualität .
Siehe auch: Drosselvorgang
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.