Enthalpie in Intensiveinheiten – Spezifische Enthalpie
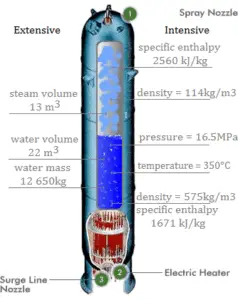
Die Enthalpie kann durch Teilen durch die Masse in eine intensive oder spezifische Variable umgewandelt werden . Ingenieure verwenden die spezifische Enthalpie in der thermodynamischen Analyse mehr als die Enthalpie selbst. Die spezifische Enthalpie (h) eines Stoffes ist seine Enthalpie pro Masseneinheit. Sie entspricht der Gesamtenthalpie (H) geteilt durch die Gesamtmasse (m).
h = H / m
wo:
h = spezifische Enthalpie (J / kg)
H = Enthalpie (J)
m = Masse (kg)
Beachten Sie, dass die Enthalpie die thermodynamische Größe ist, die dem gesamten Wärmeinhalt eines Systems entspricht. Die spezifische Enthalpie entspricht der spezifischen inneren Energie des Systems plus dem Produkt aus Druck und spezifischem Volumen .
h = u + pv
Im Allgemeinen ist die Enthalpie eine Eigenschaft einer Substanz wie Druck, Temperatur und Volumen, kann jedoch nicht direkt gemessen werden. Normalerweise wird die Enthalpie eines Stoffes in Bezug auf einen Referenzwert angegeben. Beispielsweise wird die spezifische Enthalpie von Wasser oder Dampf unter Verwendung der Referenz angegeben, dass die spezifische Enthalpie von Wasser bei 0,01 ° C und normalem atmosphärischem Druck Null ist , wobei h L = 0,00 kJ / kg . Die Tatsache, dass der absolute Wert der spezifischen Enthalpie unbekannt ist, ist jedoch kein Problem, da es die Änderung der spezifischen Enthalpie (∆h) und nicht der absolute Wert ist, der für praktische Probleme wichtig ist.
Siehe auch: Dampftabellen
Verdampfungsenthalpie
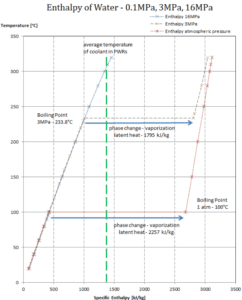
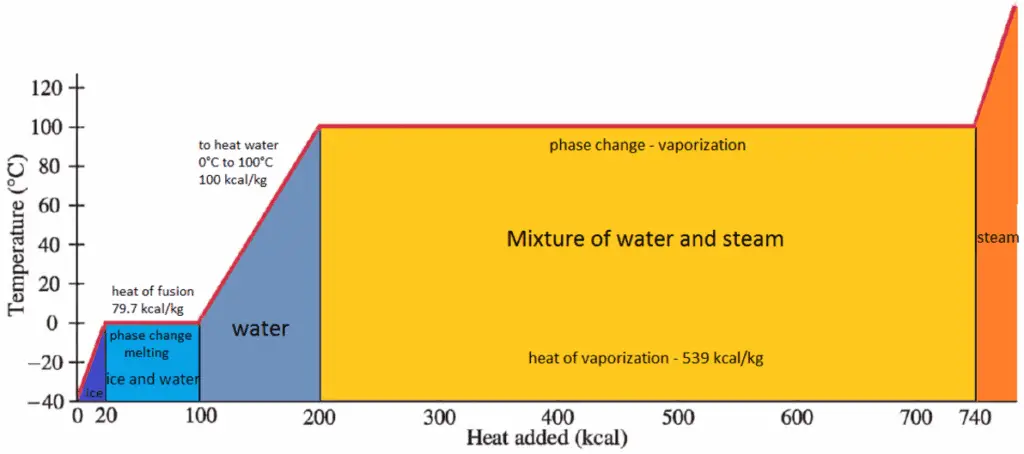
Wenn ein Material die Phase von fest zu flüssig oder von flüssig zu gasförmig ändert, ist im Allgemeinen eine bestimmte Energiemenge an dieser Phasenänderung beteiligt. Im Falle eines Phasenwechsels von Flüssigkeit zu Gas wird diese Energiemenge als Verdampfungsenthalpie (Symbol ∆H vap ; Einheit: J) bezeichnet, die auch als (latente) Verdampfungswärme oder Verdampfungswärme bezeichnet wird. Latente Wärme ist die Wärmemenge, die einer Substanz hinzugefügt oder von ihr entfernt wird, um eine Phasenänderung zu erzeugen. Diese Energie baut die intermolekularen Anziehungskräfte auf und muss auch die Energie liefern, die zur Expansion des Gases erforderlich ist (die pΔV-Arbeit). Wenn latente Wärme hinzugefügt wird, tritt keine Temperaturänderung auf. Die Verdampfungsenthalpie ist eine Funktion des Drucks, bei dem diese Umwandlung stattfindet.
Latente Verdampfungswärme – Wasser mit 0,1 MPa (atmosphärischer Druck)
h lg = 2257 kJ / kg
Latente Verdampfungswärme – Wasser mit 3 MPa (Druck in einem Dampferzeuger)
h lg = 1795 kJ / kg
Verdampfungswärme – Wasser bei 16 MPa (Druck in einem Druckhalter )
h lg = 931 kJ / kg
Die Verdampfungswärme nimmt mit zunehmendem Druck ab, während der Siedepunkt steigt. Es verschwindet vollständig an einem bestimmten Punkt, der als kritischer Punkt bezeichnet wird . Oberhalb des kritischen Punktes sind die flüssige und die dampfförmige Phase nicht zu unterscheiden, und die Substanz wird als überkritische Flüssigkeit bezeichnet .
Die Verdampfungswärme ist die Wärme, die erforderlich ist, um eine Einheit gesättigter Flüssigkeit vollständig zu verdampfen (oder eine Einheit Masse gesättigten Dampfes zu kondensieren) und gleich h lg = h g – h l .
Die Wärme, die erforderlich ist, um eine Masseeinheit an der Substanz bei konstantem Druck zu schmelzen (oder einzufrieren), ist die Schmelzwärme und ist gleich h sl = h l – h s , wobei h s die Enthalpie von gesättigtem Feststoff und h l ist ist die Enthalpie der gesättigten Flüssigkeit.
Spezifische Enthalpie von Nassdampf
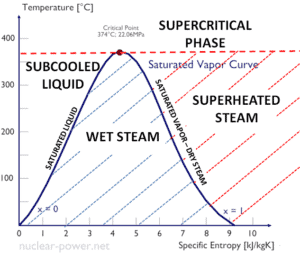 Die spezifische Enthalpie von gesättigtem flüssigem Wasser (x = 0) und trockenem Dampf (x = 1) kann aus Dampftabellen entnommen werden. Im Fall von Naßdampf kann die tatsächliche Enthalpie mit der berechnen Dampfqualität x , und den spezifischen Enthalpien gesättigten flüssigen Wasser und Trockendampf:
Die spezifische Enthalpie von gesättigtem flüssigem Wasser (x = 0) und trockenem Dampf (x = 1) kann aus Dampftabellen entnommen werden. Im Fall von Naßdampf kann die tatsächliche Enthalpie mit der berechnen Dampfqualität x , und den spezifischen Enthalpien gesättigten flüssigen Wasser und Trockendampf:
h nass = h s x + (1 – x) h l
wo
h nass = Enthalpie des feuchten Dampfes (J / kg)
h s = Enthalpie von “trockenem” Dampf (J / kg)
h l = Enthalpie von gesättigtem flüssigem Wasser (J / kg)
Wie zu sehen ist, hat nasser Dampf immer eine geringere Enthalpie als trockener Dampf.
Beispiel:
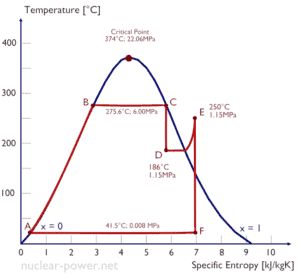
Eine Hochdruckstufe der Dampfturbine arbeitet im stationären Zustand mit Einlassbedingungen von 6 MPa, t = 275,6 ° C, x = 1 (Punkt C). Dampf verlässt diese Turbinenstufe mit einem Druck von 1,15 MPa, 186 ° C und x = 0,87 (Punkt D). Berechnen Sie die Enthalpiedifferenz zwischen diesen beiden Zuständen.
Die Enthalpie für den Zustand C kann direkt aus Dampftabellen entnommen werden, während die Enthalpie für den Zustand D anhand der Dampfqualität berechnet werden muss:
h 1, nass = 2785 kJ / kg
h 2, nass = h 2, s x + (1 – x) h 2, l = 2782. 0,87 + (1 – 0,87). 790 = 2420 + 103 = 2523 kJ / kg
Δh = 262 kJ / kg
……………………………………………………………………………………………………………………………….
Dieser Artikel basiert auf der maschinellen Übersetzung des englischen Originalartikels. Weitere Informationen finden Sie im Artikel auf Englisch. Sie können uns helfen. Wenn Sie die Übersetzung korrigieren möchten, senden Sie diese bitte an: translations@nuclear-power.com oder füllen Sie das Online-Übersetzungsformular aus. Wir bedanken uns für Ihre Hilfe und werden die Übersetzung so schnell wie möglich aktualisieren. Danke.