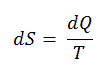O que é entalpia
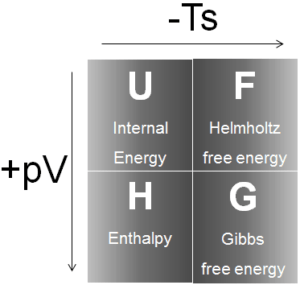
Na termodinâmica, a entalpia é a medida de energia em um sistema termodinâmico. É a quantidade termodinâmica equivalente ao conteúdo total de calor de um sistema. A entalpia é definida como a soma da energia interna E mais o produto da pressão pe volume V. Em muitas análises termodinâmicas, a soma da energia interna U e o produto da pressão pe volume V aparece, portanto, é conveniente para dar à combinação um nome, entalpia e um símbolo distinto, H.
A entalpia é a expressão preferida das mudanças de energia do sistema em muitas medições químicas, biológicas e físicas a pressão constante . É tão útil que é tabulado nas tabelas de vapor, juntamente com o volume específico e a energia interna específica . Isso se deve ao fato de simplificar a descrição da transferência de energia . Em pressão constante, a mudança de entalpia é igual à energia transferida do ambiente através do aquecimento (Q = H 2 – H 1 ) ou outro trabalho que não o trabalho de expansão. Para um processo de pressão variável, a diferença na entalpia não é tão óbvia.
Entalpia em unidades extensivas
H = U + pV
A entalpia é uma quantidade extensa, depende do tamanho do sistema ou da quantidade de substância que ele contém. A unidade SI de entalpia é o joule (J). É a energia contida no sistema, excluindo a energia cinética do movimento do sistema como um todo e a energia potencial do sistema como um todo devido a campos de força externos. É a quantidade termodinâmica equivalente ao conteúdo total de calor de um sistema.
Por outro lado, a energia pode ser armazenada nas ligações químicas entre os átomos que compõem as moléculas. Esse armazenamento de energia no nível atômico inclui energia associada a estados orbitais de elétrons, rotação nuclear e forças de ligação no núcleo.
A entalpia é representada pelo símbolo H , e a alteração na entalpia em um processo é H 2 – H 1 .
Existem expressões em termos de variáveis mais familiares, como temperatura e pressão :
dH = C p dT + V (1-aT) dp
Onde C p é a capacidade calorífica a pressão constante e α é o coeficiente de expansão térmica (cúbico). Para o gás ideal αT = 1 e, portanto:
dH = C p dT
Exemplo: Pistão sem atrito – Calor – Entalpia
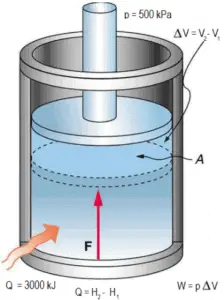
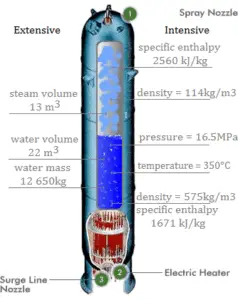
Um pistão sem atrito é usado para proporcionar uma pressão constante de 500 kPa num cilindro contendo vapor ( vapor sobreaquecido ) de um volume de 2 m 3 a 500 K . Calcule a temperatura final, se 3000 kJ de calor forem adicionados.
Solução:
Usando tabelas de vapor , sabemos que a entalpia específica desse vapor (500 kPa; 500 K) é de cerca de 2912 kJ / kg . Como nessa condição o vapor possui densidade de 2,2 kg / m 3 , sabemos que há cerca de 4,4 kg de vapor no pistão na entalpia de 2912 kJ / kg x 4,4 kg = 12812 kJ .
Quando usamos simplesmente Q = H 2 – H 1 , a entalpia resultante do vapor será:
H 2 = H 1 + Q = 15812 kJ
Nas tabelas de vapor , esse vapor superaquecido (15812 / 4,4 = 3593 kJ / kg) terá uma temperatura de 828 K (555 ° C) . Uma vez que nesta entalpia do vapor tem a densidade de 1,31 kg / m 3 , é óbvio que se expandiu em cerca de 2,2 / 1,31 = 1,67 (+ 67%). Portanto, o volume resultante é de 2 m 3 x 1,67 = 3,34 m 3 e ∆V = 3,34 m 3 – 2 m 3 = 1,34 m 3 .
A parte p∆V da entalpia, ou seja, o trabalho realizado é:
W = p∆V = 500 000 Pa x 1,34 m 3 = 670 kJ
O que é entropia
Na termodinâmica e na física estatística, a entropia é uma medida quantitativa de desordem ou da energia em um sistema para realizar o trabalho.
Na física estatística, a entropia é uma medida do distúrbio de um sistema. A que desordem se refere é realmente o número de configurações microscópicas , W , que um sistema termodinâmico pode ter quando em um estado especificado por determinadas variáveis macroscópicas ( volume , energia , pressão e temperatura ). Por “estados microscópicos”, queremos dizer os estados exatos de todas as moléculas que compõem o sistema.
Matematicamente, a definição exata é:
Entropia = (constante k de Boltzmann) x logaritmo do número de estados possíveis
S = k B logW
Essa equação, que relaciona os detalhes microscópicos, ou microestados, do sistema (via W ) ao seu estado macroscópico (via entropia S ), é a ideia principal da mecânica estatística. Em um sistema fechado, a entropia nunca diminui; portanto, no universo, a entropia está aumentando irreversivelmente. Em um sistema aberto (por exemplo, uma árvore em crescimento), a entropia pode diminuir e a ordem pode aumentar, mas apenas à custa de um aumento na entropia em outro lugar (por exemplo, no Sol).
Unidades de Entropia
O SI unidade de entropia é J / K . Segundo Clausius, a entropia foi definida através da mudança na entropia S de um sistema. A mudança na entropia S, quando uma quantidade de calor Q é adicionada a ela por um processo reversível a temperatura constante, é dada por:
Aqui Q é a energia transferida como calor para ou do sistema durante o processo, e T é a temperatura do sistema em Kelvins durante o processo. Se assumirmos um processo isotérmico reversível , a alteração total da entropia é dada por:
∆S = S 2 – S 1 = Q / T
Nesta equação, o quociente Q / T está relacionado ao aumento do distúrbio. Uma temperatura mais alta significa maior aleatoriedade de movimento. Em temperaturas mais baixas, a adição de calor Q causa um aumento fracionário substancial no movimento molecular e na aleatoriedade. Por outro lado, se a substância já estiver quente, a mesma quantidade de calor Q adiciona relativamente pouco ao maior movimento molecular.
Exemplo
Calcule a variação na entropia de 1 kg de gelo a 0 ° C, quando derretida reversivelmente em água a 0 ° C.
Por se tratar de um processo isotérmico, podemos usar:
∆S = S 2 – S 1 = Q / T
portanto, a alteração da entropia será:
∆S = 334 [kJ] / 273,15 [K] = 1,22 [kJ / K]
onde são necessários 334 quilojoules de calor para derreter 1 kg de gelo (calor latente de fusão = 334 kJ / kg) e esse calor é transferido para o sistema a 0 ° C (273,15 K).
Diagramas em Ts
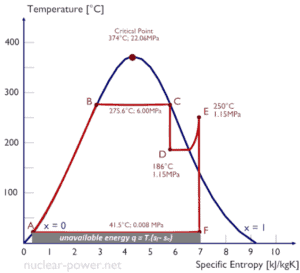
Em geral, as fases de uma substância e os relacionamentos entre suas propriedades são mais comumente mostrados nos diagramas de propriedades . Um grande número de propriedades diferentes foi definido e existem algumas dependências entre as propriedades.
Um diagrama de entropia de temperatura ( diagrama Ts ) é o tipo de diagrama mais frequentemente usado para analisar os ciclos do sistema de transferência de energia. É usado na termodinâmica para visualizar alterações de temperatura e entropia específica durante um processo ou ciclo termodinâmico.
Isso ocorre porque o trabalho realizado pelo ou no sistema e o calor adicionado ou removido do sistema podem ser visualizados no diagrama Ts . Pela definição de entropia, o calor transferido para ou de um sistema é igual à área sob a curva Ts do processo.
dQ = TdS
Um processo isentrópico é representado como uma linha vertical em um diagrama Ts, enquanto um processo isotérmico é uma linha horizontal. Em um estado idealizado, a compressão é uma bomba, a compressão em um compressor e a expansão em uma turbina são processos isentrópicos. Portanto, é muito útil em engenharia de energia, porque esses dispositivos são usados em ciclos termodinâmicos de usinas de energia.
Observe que, as premissas isentrópicas são aplicáveis apenas aos ciclos ideais. Ciclos termodinâmicos reais têm perdas de energia inerentes devido à ineficiência de compressores e turbinas.
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.