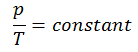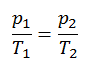Ciclo Otto – Processos
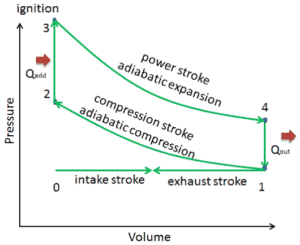
Em um ciclo Otto ideal , o sistema que executa o ciclo passa por uma série de quatro processos reversíveis internamente: dois processos isentrópicos (adiabáticos reversíveis) alternados com dois processos isocóricos:
- Compressão isentrópica (curso de compressão) – O gás (mistura combustível-ar) é comprimido adiabaticamente do estado 1 ao estado 2, conforme o pistão se move do ponto morto inferior para o ponto morto superior. O ambiente trabalha com o gás, aumentando sua energia interna (temperatura) e comprimindo-o. Por outro lado, a entropia permanece inalterada. As mudanças nos volumes e sua taxa ( V 1 / V 2 ) são conhecidas como taxa de compressão.
- Compressão isocórica (fase de ignição) – Nesta fase (entre o estado 2 e o estado 3), há um volume constante (o pistão está em repouso) transferido para o ar a partir de uma fonte externa, enquanto o pistão está em repouso no ponto morto superior . Esse processo visa representar a ignição da mistura combustível-ar injetada na câmara e a subsequente queima rápida. A pressão aumenta e a razão ( P 3 / P 2 ) é conhecida como “taxa de explosão”.
- Expansão isentrópica (golpe de energia) – O gás se expande adiabaticamente do estado 3 para o estado 4, conforme o pistão se move do ponto morto superior para o ponto morto inferior. O gás trabalha nos arredores (pistão) e perde uma quantidade de energia interna igual ao trabalho que sai do sistema. Novamente a entropia permanece inalterada. A taxa de volume ( V 4 / V 3 ) é conhecida como a razão de expansão isentrópica, mas para o ciclo Otto, é igual à taxa de compressão.
- Descompressão isocórica (curso de escape) – Nesta fase, o ciclo é concluído por um processo de volume constante no qual o calor é rejeitado do ar enquanto o pistão está no ponto morto inferior. A pressão do gás de trabalho cai instantaneamente do ponto 4 ao ponto 1. A válvula de escape se abre no ponto 4. O curso de escape ocorre imediatamente após esta descompressão. À medida que o pistão se move do ponto morto inferior (ponto 1) para o ponto morto superior (ponto 0) com a válvula de escape aberta, a mistura gasosa é ventilada para a atmosfera e o processo começa novamente.
Durante o ciclo Otto, o trabalho é realizado no gás pelo pistão entre os estados 1 e 2 ( compressão isentrópica ). O trabalho é realizado pelo gás no pistão entre os estágios 3 e 4 ( expansão isentrópica ). A diferença entre o trabalho realizado pelo gás e o trabalho realizado com o gás é o trabalho líquido produzido pelo ciclo e corresponde à área delimitada pela curva do ciclo. O trabalho produzido pelos tempos de ciclo, a taxa do ciclo (ciclos por segundo) é igual à potência produzida pelo motor Otto.
Processo isentrópico
Um processo isentrópico é um processo termodinâmico , no qual a entropia do fluido ou gás permanece constante. Isso significa que o processo isentrópico é um caso especial de um processo adiabático no qual não há transferência de calor ou matéria. É um processo adiabático reversível . A suposição de que não há transferência de calor é muito importante, pois podemos usar a aproximação adiabática apenas em processos muito rápidos .
Processo isentrópico e a primeira lei
Para um sistema fechado, podemos escrever a primeira lei da termodinâmica em termos de entalpia :
dH = dQ + Vdp
ou
dH = TdS + Vdp
Processo isentrópico (dQ = 0):
dH = Vdp → W = H 2 – H 1 → H 2 – H 1 = C P (T 2 – T 1 ) (para gás ideal )
Processo isentrópico do gás ideal
O processo isentrópico (um caso especial de processo adiabático) pode ser expresso com a lei dos gases ideais como:
pV κ = constante
ou
p 1 V 1 k = p 2 V 2 k
em que κ = c p / c v é a proporção de aquecimentos específicos (ou capacidades de calor ) para o gás. Um para pressão constante (c p ) e outro para volume constante (c v ) . Observe que essa razão κ = c p / c v é um fator na determinação da velocidade do som em um gás e em outros processos adiabáticos.
Processo Isocórico
Um processo isocórico é um processo termodinâmico, no qual o volume do sistema fechado permanece constante (V = const). Ele descreve o comportamento do gás dentro do recipiente, que não pode ser deformado. Como o volume permanece constante, a transferência de calor para dentro ou para fora do sistema não funciona , mas altera apenas a energia interna (a temperatura) do sistema.
Processo isocórico e a primeira lei
A forma clássica da primeira lei da termodinâmica é a seguinte equação:
dU = dQ – dW
Nesta equação, dW é igual a dW = pdV e é conhecido como trabalho de fronteira . Então:
dU = dQ – pdV
No processo isocórico e no gás ideal , todo o calor adicionado ao sistema será usado para aumentar a energia interna.
Processo isocórico (pdV = 0):
dU = dQ (para gás ideal)
dU = 0 = Q – W → W = Q (para gás ideal)
Processo isocórico do gás ideal
O processo isocórico pode ser expresso com a lei dos gases ideais como:
ou
Em um diagrama pV , o processo ocorre ao longo de uma linha horizontal que possui a equação V = constante.
Veja também: Lei de Guy-Lussac
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.