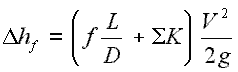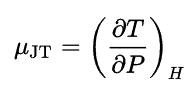Processus de limitation – Processus isenthalpique
Un processus d’étranglement est un processus thermodynamique , dans lequel l’ enthalpie du gaz ou du milieu reste constante (h = const) . En fait, le processus d’étranglement est l’un des processus isenthalpiques . Pendant le processus d’étranglement, aucun travail n’est effectué par ou sur le système (dW = 0), et généralement il n’y a pas de transfert de chaleur ( adiabatique ) depuis ou vers le système (dQ = 0). De l’autre, le processus d’étranglement ne peut pas être isentropique, c’est un processus fondamentalement irréversible . Caractéristiques du processus d’étranglement:
- Pas de transfert de travail
- Pas de transfert de chaleur
- Processus irréversible
- Processus isenthalpique
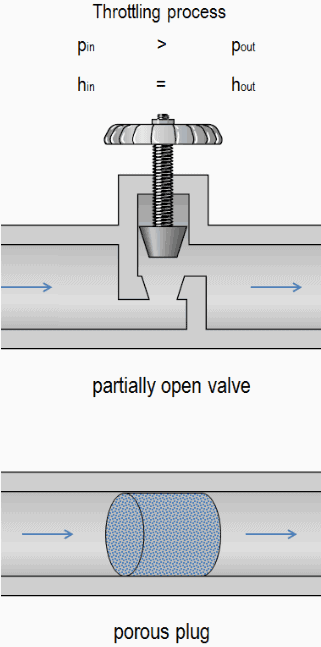
Un étranglement du débit entraîne une réduction significative de la pression , car un dispositif d’étranglement provoque une perte de pression locale . Un étranglement peut être réalisé simplement en introduisant une restriction dans une ligne à travers laquelle un gaz ou un liquide s’écoule. Cette restriction se fait généralement au moyen d’une valve partiellement ouverte ou d’un bouchon poreux. De telles pertes de charge sont généralement appelées pertes mineures , bien qu’elles représentent souvent une partie importante de la perte de charge . Les pertes mineures sont à peu près proportionnelle à la place du débit et par conséquent , ils peuvent être intégrés facilement dans l’ équation de Darcy-Weisbach par coefficient de résistance K .
Par exemple, considérons un étranglement d’un gaz parfait s’écoulant à travers une vanne partiellement ouverte. Par expérience, nous pouvons observer que: p in > p out , v in <v out , où p est la pression et v est le volume spécifique . On peut également observer que des enthalpies spécifiques restent les mêmes, c’est-à-dire h in = h out .
L’enthalpie spécifique est égale à l’ énergie interne spécifique du système plus le produit de la pression et du volume spécifique .
h = u + pv
Par conséquent, si la pression diminue, le volume spécifique doit augmenter si l’enthalpie doit rester constante (en supposant que u est constant). Parce que le débit massique est constant, le changement de volume spécifique est observé comme une augmentation de la vitesse du gaz , et cela est également vérifié par des observations.
S’il y a un changement dans l’énergie interne, u, alors il doit y avoir un changement de température . Normalement, la température du fluide baisse. Cependant, dans des cas particuliers, la température peut rester la même ou elle peut augmenter.
Effet Joule – Thomson – Coefficient de Joule Thomson
Les changements de température pendant le processus d’étranglement sont soumis à l’ effet Joule-Thomson . À température ambiante et à des pressions normales, tous les gaz, sauf l’hydrogène et l’hélium, refroidissent pendant la détente du gaz. Le refroidissement se produit parce que le travail doit être fait pour surmonter l’attraction à longue distance entre les molécules de gaz au fur et à mesure qu’elles s’éloignent. L’effet dépend de la valeur du coefficient Joule-Thomson , qui est défini comme:
Une application du processus d’étranglement se produit dans les réfrigérateurs à compression de vapeur, où une vanne d’étranglement est utilisée pour réduire la pression et réduire la température du réfrigérant de la pression à la sortie du condenseur à la pression plus faible existant dans l’évaporateur.
Limitation de la vapeur humide
La vapeur humide est caractérisée par la qualité de la vapeur , qui varie de zéro à l’unité – intervalle ouvert (0,1). L’étranglement de la vapeur humide est également associé à la conservation de l’enthalpie . L’enthalpie est conservée car aucun travail n’est effectué par ou sur le système (dW = 0), et il n’y a généralement pas de transfert de chaleur (adiabatique) depuis ou vers le système (dQ = 0). Mais dans ce cas, une diminution de la pression entraîne une augmentation de la qualité de la vapeur . Lorsque la pression diminue, une partie du liquide contenu dans la vapeur humide se vaporise et augmente la qualité de la vapeur (c’est-à-dire la fraction de sécheresse). Ce processus a lieu, car la température de saturationest plus faible à la pression inférieure. La température plus basse, la pression plus basse et la vapeur de meilleure qualité contiennent la même enthalpie que la vapeur d’origine.
Exemple: étranglement de la vapeur humide
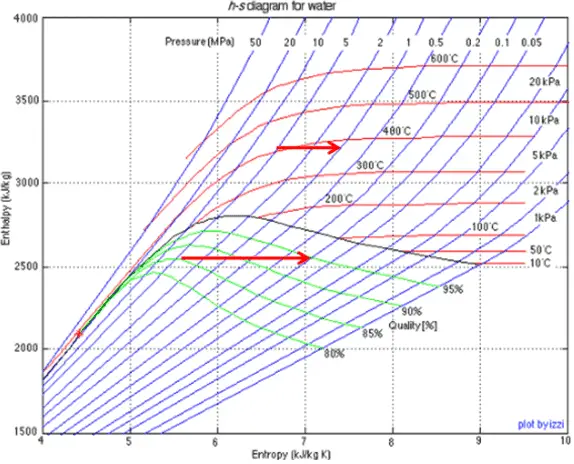
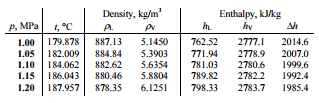
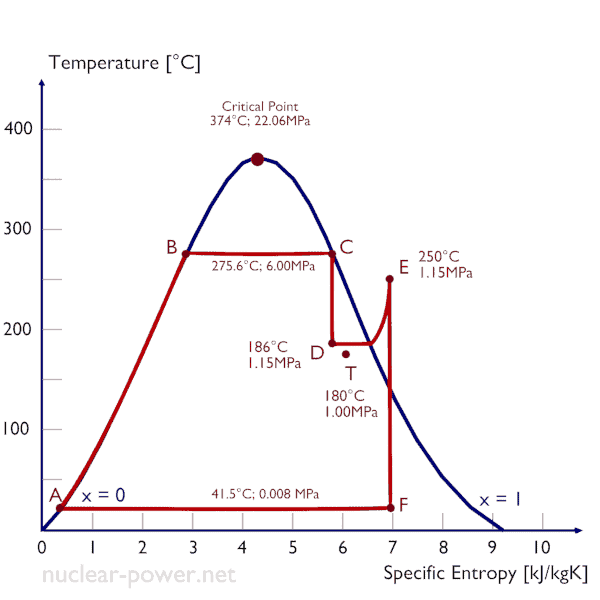
Un étage haute pression de turbine à vapeur fonctionne à l’état stable avec des conditions d’entrée de 6 MPa, t = 275,6 ° C, x = 1 (point C). La vapeur sort de cet étage de turbine à une pression de 1,15 MPa, 186 ° C et x = 0,87 (point D). Déterminez la qualité de vapeur de la vapeur lorsqu’elle est étranglée de 1,15 MPa à 1,0 MPa. Supposons que le processus est adiabatique et qu’aucun travail n’est effectué par le système.
Voir aussi: Tables Steam
Solution:
L’enthalpie pour l’état D doit être calculée en utilisant la qualité de la vapeur:
h D, humide = h D, vapeur x + (1 – x) h D, liquide = 2782. 0,87 + (1 – 0,87). 790 = 2420 + 103 = 2523 kJ / kg
Comme il s’agit d’un processus isenthalpique, nous connaissons l’enthalpie pour le point T. À partir des tables de vapeur, nous devons trouver la qualité de la vapeur en utilisant la même équation et en résolvant l’équation de la qualité de la vapeur, x:
h T, humide = h T, vapeur x + (1 – x) h T, liquide
x = ( h T, humide – h T, liquide ) / ( h T, vapeur – h T, liquide ) = (2523 – 762) / (2777 – 762) = 0,874 = 87,4%
Dans ce cas du processus d’étranglement (1,15 MPa à 1 MPa), la qualité de la vapeur augmente de 87% à 87,4% et la température diminue de 186 ° C à 179,9 ° C.
La limitation de la vapeur humide provoque généralement une augmentation de la qualité de la vapeur, une augmentation de l’entropie et une diminution de la température
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci