Ciclo Rankine – Procesos
En un ciclo ideal de Rankine, el sistema que ejecuta el ciclo se somete a una serie de cuatro procesos: dos procesos isentrópicos (adiabáticos reversibles) alternados con dos procesos isobáricos.
Ciclo Rankine – Procesos
-
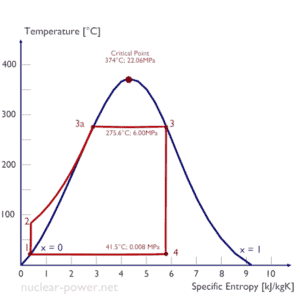
Ciclo Rankine – Diagrama Ts Compresión isentrópica (compresión en bombas centrífugas): el condensado líquido se comprime adiabáticamente del estado 1 al estado 2 mediante bombas centrífugas (generalmente mediante bombas de condensado y luego mediante bombas de agua de alimentación). El condensado líquido se bombea desde el condensador a la caldera de mayor presión. En este proceso, los alrededores trabajan en el fluido, aumentando su entalpía (h = u + pv) y comprimiéndolo (aumentando su presión). Por otro lado, la entropía permanece sin cambios. El trabajo requerido para el compresor viene dado por W Pumps = H 2 – H 1 .
- Adición de calor isobárico (en un intercambiador de calor – caldera): en esta fase (entre el estado 2 y el estado 3) hay una transferencia de calor a presión constante al condensado líquido desde una fuente externa, ya que la cámara está abierta para fluir hacia adentro y hacia afuera . El agua de alimentación (circuito secundario) se calienta desde el punto de ebullición (2 → 3a) de ese fluido y luego se evapora en la caldera (3a → 3). El calor neto agregado viene dado por Q add = H 3 – H 2
- Expansión isentrópica (expansión en una turbina de vapor): el vapor de la caldera se expande adiabáticamente del estado 3 al estado 4 en una turbina de vapor para producir trabajo y luego se descarga al condensador (parcialmente condensado). El vapor funciona en los alrededores (palas de la turbina) y pierde una cantidad de entalpía igual al trabajo que abandona el sistema. El trabajo realizado por la turbina viene dado por W T = H 4 – H 3 . Nuevamente, la entropía permanece sin cambios.
- Rechazo isobárico de calor (en un intercambiador de calor) : en esta fase, el ciclo se completa mediante un proceso de presión constante en el que el calor se rechaza del vapor parcialmente condensado. Hay una transferencia de calor del vapor al agua de enfriamiento que fluye en un circuito de enfriamiento. El vapor se condensa y la temperatura del agua de enfriamiento aumenta. El calor neto rechazado viene dado por Q re = H 4 – H 1
Durante un ciclo de Rankine, las bombas realizan el trabajo sobre el fluido entre los estados 1 y 2 ( i compresión sentrópica ). El fluido de la turbina realiza el trabajo entre las etapas 3 y 4 ( i expansión sentrópica ). La diferencia entre el trabajo realizado por el fluido y el trabajo realizado sobre el fluido es el trabajo neto producido por el ciclo y corresponde al área encerrada por la curva del ciclo (en el diagrama pV). El fluido de trabajo en un ciclo de Rankine sigue un ciclo cerrado y se reutiliza constantemente.
Como se puede ver, es conveniente utilizar la entalpía y la primera ley en términos de entalpía en el análisis de este ciclo termodinámico. Esta forma de ley simplifica la descripción de la transferencia de energía . A presión constante , el cambio de entalpía es igual a la energía transferida del ambiente a través del calentamiento:
Proceso isobárico (Vdp = 0):
dH = dQ → Q = H 2 – H 1
En una entropía constante , es decir, en un proceso isentrópico, el cambio de entalpía es igual al trabajo del proceso de flujo realizado en o por el sistema:
Proceso isentrópico (dQ = 0):
dH = Vdp → W = H 2 – H 1
Ver también: ¿Por qué los ingenieros de energía usan la entalpía? Respuesta: dH = dQ + Vdp
Proceso isentrópico
Un proceso isentrópico es un proceso termodinámico , en el cual la entropía del fluido o gas permanece constante. Significa que el proceso isentrópico es un caso especial de un proceso adiabático en el que no hay transferencia de calor o materia. Es un proceso adiabático reversible . La suposición de que no hay transferencia de calor es muy importante, ya que podemos usar la aproximación adiabática solo en procesos muy rápidos .
Proceso isentrópico y la primera ley
Para un sistema cerrado, podemos escribir la primera ley de la termodinámica en términos de entalpía :
dH = dQ + Vdp
o
dH = TdS + Vdp
Proceso isentrópico (dQ = 0):
dH = Vdp → W = H 2 – H 1
Proceso isobárico
Un proceso isobárico es un proceso termodinámico , en el cual la presión del sistema permanece constante (p = const). La transferencia de calor dentro o fuera del sistema funciona, pero también cambia la energía interna del sistema.
Dado que hay cambios en la energía interna (dU) y cambios en el volumen del sistema (∆V), los ingenieros a menudo usan la entalpía del sistema, que se define como:
H = U + pV
Proceso isobárico y la primera ley
La forma clásica de la primera ley de la termodinámica es la siguiente ecuación:
dU = dQ – dW
En esta ecuación, dW es igual a dW = pdV y se conoce como el trabajo límite . En un proceso isobárico y el gas ideal, parte del calor agregado al sistema se utilizará para hacer el trabajo y parte del calor agregado aumentará la energía interna (aumentará la temperatura). Por lo tanto, es conveniente utilizar la entalpía en lugar de la energía interna.
Proceso isobárico (Vdp = 0):
dH = dQ → Q = H 2 – H 1
En una entropía constante , es decir, en un proceso isentrópico, el cambio de entalpía es igual al trabajo del proceso de flujo realizado en o por el sistema.
Ciclo de Rankine – pV, diagrama Ts
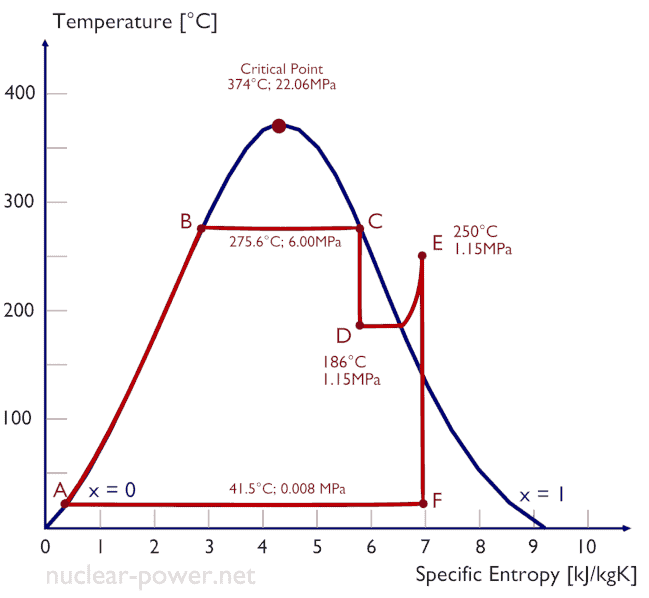
El ciclo de Rankine a menudo se representa en un diagrama de volumen de presión (diagrama pV ) y en un diagrama de temperatura-entropía ( diagrama Ts ).
Cuando se trazan en un diagrama de volumen de presión , los procesos isobáricos siguen las líneas isobáricas para el gas (las líneas horizontales), los procesos adiabáticos se mueven entre estas líneas horizontales y el área delimitada por la ruta completa del ciclo representa el trabajo total que se puede hacer durante uno ciclo.
El diagrama de temperatura-entropía ( diagrama Ts) en el que el estado termodinámico se especifica mediante un punto en un gráfico con entropía específica (s) como eje horizontal y temperatura absoluta (T) como eje vertical. Los diagramas Ts son una herramienta útil y común, particularmente porque ayuda a visualizar la transferencia de calor durante un proceso. Para procesos reversibles (ideales), el área bajo la curva Ts de un proceso es el calor transferido al sistema durante ese proceso.
……………………………………………………………………………………………………………………………….
Este artículo se basa en la traducción automática del artículo original en inglés. Para más información vea el artículo en inglés. Puedes ayudarnos. Si desea corregir la traducción, envíela a: translations@nuclear-power.com o complete el formulario de traducción en línea. Agradecemos su ayuda, actualizaremos la traducción lo antes posible. Gracias.