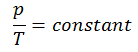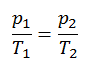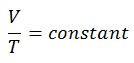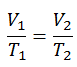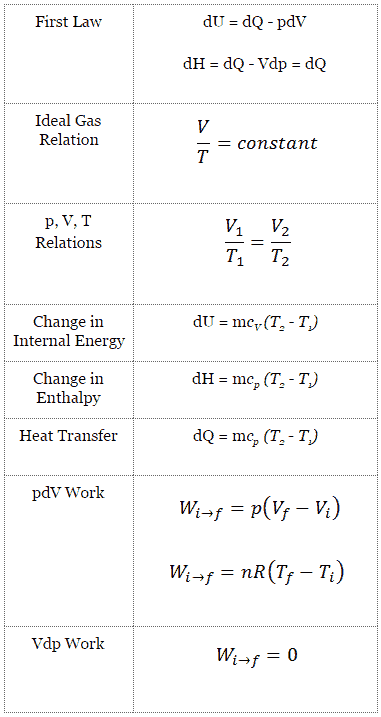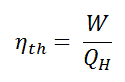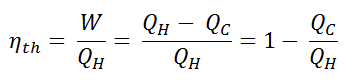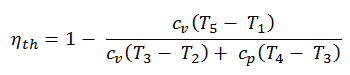Cycle diesel – moteur diesel
Le cycle double , ou cycle de pression limité , est un cycle thermodynamique qui combine le cycle Otto et le cycle Diesel . Dans le cycle double, la combustion se produit en partie à volume constant et en partie à pression constante. Il peut être utilisé pour décrire les moteurs à combustion interne. Les diagrammes pression-volume des moteurs à combustion interne actuels ne sont pas bien décrits par les cycles Otto et Diesel. Un cycle air standard qui peut être rapproché des variations de pression est le cycle double air. Une approche plus efficace consisterait à modéliser le processus de combustion des moteurs Otto et Diesel en combinant deux processus de transfert de chaleur, un processus isochore et unprocessus isobare .
Par rapport à un cycle Otto, qui suppose une addition de chaleur instantanée (une addition de chaleur isochore), dans un cycle double, de la chaleur est ajoutée partiellement à volume constant et partiellement à pression constante. Par conséquent, l’avantage est qu’il reste plus de temps pour que le combustible brûle complètement. D’autre part, l’utilisation d’un cycle double est légèrement plus complexe . L’efficacité thermique se situe entre les cycles Otto et Diesel.
Cycle de Sabathé – Processus
Dans un cycle double , le système exécutant le cycle subit une série de cinq processus: deux processus isentropiques (adiabatiques réversibles) alternés avec deux processus isochoriques et un processus isobare:
-
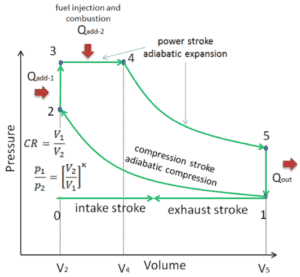
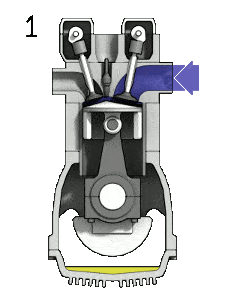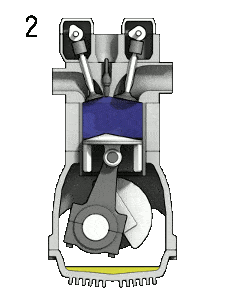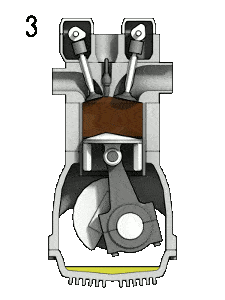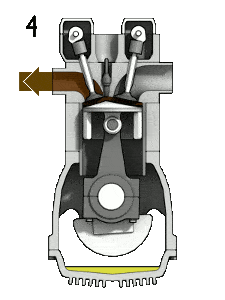
Double cycle – Diagramme pV Compression isentropique (course de compression) – Le gaz est comprimé de manière adiabatique de l’état 1 à l’état 2, lorsque le piston se déplace du point de fermeture de la soupape d’admission (1) au point mort haut. Les environs agissent sur le gaz, augmentant son énergie interne (température) et le compressant. En revanche, l’entropie reste inchangée. L’évolution des volumes et de son rapport ( V 1 / V 2 ) est connue sous le nom de taux de compression. Le taux de compression est inférieur au taux d’expansion.
- Compression isochore (phase d’allumage) – Dans cette phase (entre l’état 2 et l’état 3), il y a un transfert de chaleur à volume constant (le piston est au repos) vers l’air à partir d’une source externe tandis que le piston est au repos au point mort haut . Ce processus est similaire au processus isochore du cycle d’Otto. Il est destiné à représenter l’inflammation du mélange carburant-air injecté dans la chambre et la combustion rapide qui en résulte. La pression augmente et le rapport ( P 3 / P 2 ) est appelé «rapport d’explosion».
- Expansion isobare (course motrice) – Dans cette phase (entre l’état 3 et l’état 4), il y a un transfert de chaleur à pression constante (modèle idéalisé) vers l’air à partir d’une source externe (combustion du carburant) tandis que le piston se déplace vers le V 4 . Pendant le processus à pression constante, l’énergie pénètre dans le système sous forme de chaleur Q ajoutée , et une partie du travail se fait en déplaçant le piston.
- Expansion isentropique (course de puissance) – Le gaz se détend adiabatiquement de l’état 4 à l’état 5, lorsque le piston se déplace de V 3 au point mort bas. Le gaz travaille sur l’environnement (piston) et perd une quantité d’énergie interne égale au travail qui quitte le système. Encore une fois, l’entropie reste inchangée.
- Décompression isochore (course d’échappement) – Dans cette phase, le cycle se termine par un processus à volume constant dans lequel la chaleur est rejetée de l’air tandis que le piston est au point mort bas. La pression du gaz de travail chute instantanément du point 5 au point 1. La soupape d’échappement s’ouvre au point 5. La course d’échappement est directement après cette décompression. Lorsque le piston se déplace du point mort bas (point 1) au point mort haut (point 0) avec la soupape d’échappement ouverte, le mélange gazeux est évacué vers l’atmosphère et le processus recommence.
Pendant le cycle double, le travail est effectué sur le gaz par le piston entre les états 1 et 2 ( i compression sentropique ). Le travail se fait par le gaz sur le piston entre les étapes 2 et 3 ( i addition de chaleur sobarique ) et entre les étapes 2 et 3 ( i expansion sentropique ). La différence entre le travail effectué par le gaz et le travail effectué sur le gaz est le travail net produit par le cycle et il correspond à la zone délimitée par la courbe du cycle. Le travail produit par le cycle multiplie la vitesse du cycle (cycles par seconde) par la puissance produite par le moteur Diesel.
Processus isentropique
Un processus isentropique est un processus thermodynamique , dans lequel l’ entropie du fluide ou du gaz reste constante. Cela signifie que le processus isentropique est un cas particulier d’un processus adiabatique dans lequel il n’y a pas de transfert de chaleur ou de matière. Il s’agit d’un processus adiabatique réversible . L’hypothèse d’absence de transfert de chaleur est très importante, car nous ne pouvons utiliser l’approximation adiabatique que dans des processus très rapides .
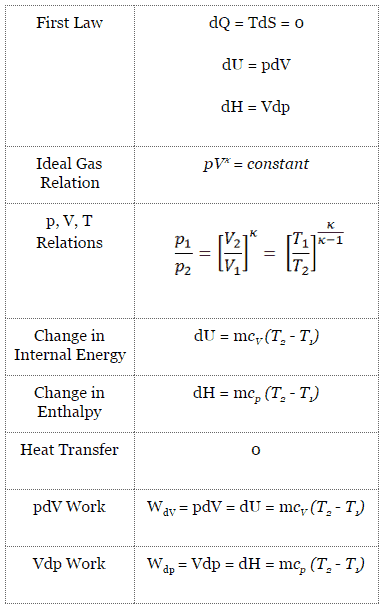
Processus isentropique et première loi
Pour un système fermé, on peut écrire la première loi de la thermodynamique en termes d’enthalpie :
dH = dQ + Vdp
ou
dH = TdS + Vdp
Processus isentropique (dQ = 0):
dH = Vdp → W = H 2 – H 1 → H 2 – H 1 = C p (T 2 – T 1 ) (pour le gaz idéal )
Processus isentropique du gaz idéal
Le processus isentropique (un cas particulier du processus adiabatique) peut être exprimé avec la loi du gaz idéal comme:
pV κ = constant
ou
p 1 V 1 κ = p 2 V 2 κ
dans laquelle κ = c p / c v est le rapport des chaleurs spécifiques (ou capacités calorifiques ) pour le gaz. Un pour une pression constante (c p ) et un pour un volume constant (c v ) . Notez que ce rapport κ = c p / c v est un facteur déterminant la vitesse du son dans un gaz et d’autres processus adiabatiques.
Processus isochorique
Un processus isochore est un processus thermodynamique, dans lequel le volume du système fermé reste constant (V = const). Il décrit le comportement du gaz à l’intérieur du conteneur, qui ne peut pas être déformé. Étant donné que le volume reste constant, le transfert de chaleur dans ou hors du système ne fonctionne pas avec le p∆V , mais modifie uniquement l’ énergie interne (la température) du système.
Processus isochorique et première loi
La forme classique de la première loi de la thermodynamique est l’équation suivante:
dU = dQ – dW
Dans cette équation, dW est égal à dW = pdV et est connu comme le travail aux limites . Alors:
dU = dQ – pdV
Dans le processus isochore et le gaz idéal , toute la chaleur ajoutée au système sera utilisée pour augmenter l’énergie interne.
Processus isochorique (pdV = 0):
dU = dQ (pour le gaz idéal)
dU = 0 = Q – W → W = Q (pour le gaz idéal)
Processus isochorique du gaz idéal
Le processus isochore peut s’exprimer avec la loi du gaz idéal comme:
ou
Sur un diagramme pV , le processus se produit le long d’une ligne horizontale qui a l’équation V = constante.
Voir aussi: Loi de Guy-Lussac
Processus isobare
Un processus isobare est un processus thermodynamique , dans lequel la pression du système reste constante (p = const). Le transfert de chaleur dans ou hors du système fonctionne, mais modifie également l’énergie interne du système.
Puisqu’il y a des changements d’ énergie interne (dU) et des changements de volume du système (∆V), les ingénieurs utilisent souvent l’ enthalpie du système, qui est définie comme:
H = U + pV
Processus isobare et première loi
La forme classique de la première loi de la thermodynamique est l’équation suivante:
dU = dQ – dW
Dans cette équation, dW est égal à dW = pdV et est connu comme le travail aux limites . Dans un procédé isobare et le gaz idéal, une partie de la chaleur ajoutée au système sera utilisée pour faire le travail et une partie de la chaleur ajoutée augmentera l’ énergie interne (augmentera la température). Par conséquent, il est commode d’utiliser l’ enthalpie au lieu de l’énergie interne.
Processus isobare (Vdp = 0):
dH = dQ → Q = H 2 – H 1
À entropie constante , c’est-à-dire dans un processus isentropique, le changement d’enthalpie est égal au travail de processus d’écoulement effectué sur ou par le système.
Processus isobare du gaz idéal
Le processus isobare peut s’exprimer avec la loi du gaz idéal comme:
ou
Sur un diagramme pV , le processus se produit le long d’une ligne horizontale (appelée isobare) qui a l’équation p = constante.
Voir aussi: Charles’s Law
Efficacité thermique pour double cycle
En général , le rendement thermique , η e , d’un moteur thermique est définie comme étant le rapport entre le travail qu’elle fait, W , à la chaleur d’ entrée à la température élevée, Q H .
L’ efficacité thermique , η th , représente la fraction de chaleur , Q H , qui est convertie en travail . Puisque l’énergie est conservée selon la première loi de la thermodynamique et que l’énergie ne peut pas être convertie pour fonctionner complètement, l’apport de chaleur, Q H , doit être égal au travail effectué, W, plus la chaleur qui doit être dissipée sous forme de chaleur résiduelle Q C dans le environnement. Par conséquent, nous pouvons réécrire la formule de l’efficacité thermique comme suit:
Par conséquent, la chaleur ajoutée et rejetée est donnée par:
Q add-1 = mc v (T 3 – T 2 )
Q add-2 = mc p (T 4 – T 3 )
Q out = mc v (T 5 – T 1 )
Par conséquent, l’efficacité thermique pour un cycle double est:
……………………………………………………………………………………………………………………………….
Cet article est basé sur la traduction automatique de l’article original en anglais. Pour plus d’informations, voir l’article en anglais. Pouvez vous nous aider Si vous souhaitez corriger la traduction, envoyez-la à l’adresse: translations@nuclear-power.com ou remplissez le formulaire de traduction en ligne. Nous apprécions votre aide, nous mettrons à jour la traduction le plus rapidement possible. Merci