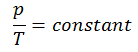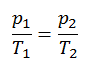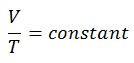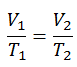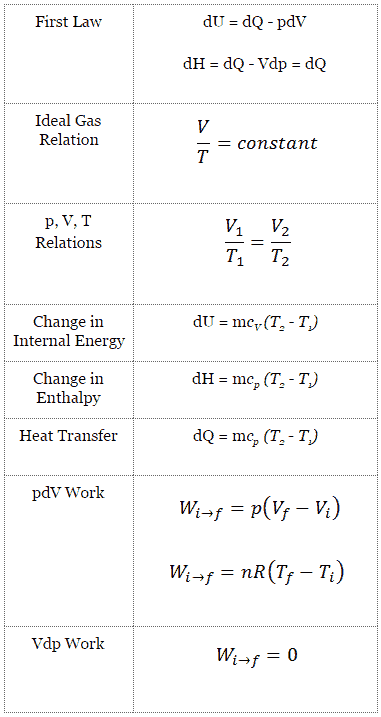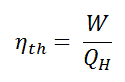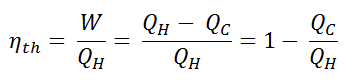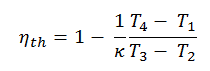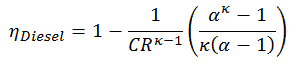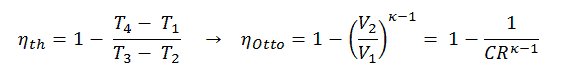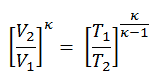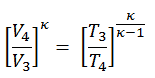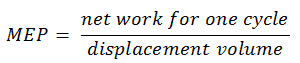Ciclo Diesel – Motor Diesel
Na década de 1890, um inventor alemão, Rudolf Diesel patenteou sua invenção de um eficiente, de combustão lenta, ignição por compressão, motor de combustão interna. O ciclo original proposto por Rudolf Diesel era um ciclo de temperatura constante. Nos anos posteriores, Diesel percebeu que seu ciclo original não funcionaria e adotou o ciclo de pressão constante, conhecido como ciclo de Diesel .
O ciclo diesel é um dos ciclos termodinâmicos mais comuns encontrados em motores de automóveis e descreve o funcionamento de um motor de pistão de ignição por compressão típico. O motor Diesel é semelhante em operação ao motor a gasolina. A diferença mais importante é que:
- Não há combustível no cilindro no início do curso de compressão; portanto, uma autoignição não ocorre nos motores a diesel.
- O motor diesel usa ignição por compressão em vez de ignição por faísca.
- Devido à alta temperatura desenvolvida durante a compressão adiabática, o combustível inflama espontaneamente à medida que é injetado. Portanto, não são necessárias velas de ignição.
- Antes do início do curso de força, os injetores começam a injetar combustível diretamente na câmara de combustão e, portanto, a primeira parte do curso de força ocorre aproximadamente à pressão constante.
- Taxas de compressão mais altas podem ser alcançadas em motores a diesel do que em motores Otto
Ciclo Diesel – Processos
Em um ciclo Diesel ideal, o sistema que executa o ciclo passa por uma série de quatro processos: dois processos isentrópicos (adiabáticos reversíveis) alternados com um processo isocórico e um processo isobárico.
-
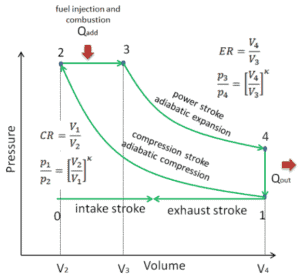
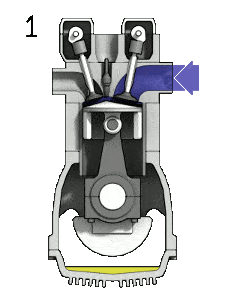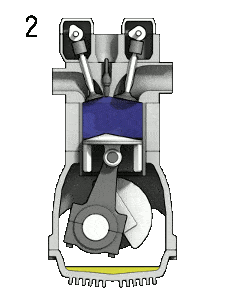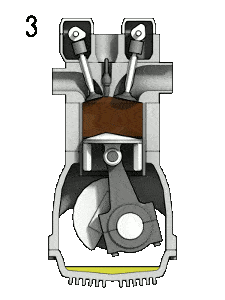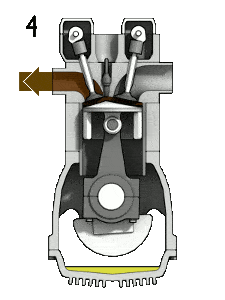
diagrama pV de um ciclo Diesel ideal Compressão isentrópica (curso de compressão) – O ar é comprimido adiabaticamente do estado 1 ao estado 2, conforme o pistão se move do ponto morto inferior para o ponto morto superior. O ambiente trabalha com o gás, aumentando sua energia interna (temperatura) e comprimindo-o. Por outro lado, a entropia permanece inalterada. As mudanças nos volumes e sua proporção ( V 1 / V 2 ) são conhecidas como taxa de compressão.
- Expansão isobárica (fase de ignição) – Nesta fase (entre o estado 2 e o estado 3), há uma transferência de calor de pressão constante (modelo idealizado) para o ar a partir de uma fonte externa (combustão de combustível injetado) enquanto o pistão está se movendo em direção ao V 3 . Durante o processo de pressão constante, a energia entra no sistema à medida que o calor Q é adicionado e uma parte do trabalho é feita movendo o pistão.
- Expansão isentrópica (poder acidente vascular cerebral) – O gás expande-se adiabaticamente de estado 3 para o estado 4, quando o pistão se move da V 3 a centro morto inferior. O gás trabalha nos arredores (pistão) e perde uma quantidade de energia interna igual ao trabalho que sai do sistema. Novamente a entropia permanece inalterada. A taxa de volume ( V 4 / V 3 ) é conhecida como taxa de expansão isentrópica.
- Descompressão isocórica (curso de exaustão) – Nesta fase, o ciclo é concluído por um processo de volume constante no qual o calor é rejeitado do ar enquanto o pistão está no ponto morto inferior. A pressão do gás de trabalho cai instantaneamente do ponto 4 para o ponto 1. A válvula de escape se abre no ponto 4. O curso de escape ocorre imediatamente após esta descompressão. À medida que o pistão se move do ponto morto inferior (ponto 1) para o ponto morto superior (ponto 0) com a válvula de escape aberta, a mistura gasosa é ventilada para a atmosfera e o processo recomeça.
Durante o ciclo diesel, o trabalho é realizado sobre o gás pelo pistão entre os estados 1 e 2 ( i compressão sentropic ). O trabalho é realizado pelo gás no pistão entre os estágios 2 e 3 ( i adição de calor sobárico ) e entre os estágios 2 e 3 ( i expansão sentrópica ). A diferença entre o trabalho realizado pelo gás e o trabalho realizado com o gás é o trabalho líquido produzido pelo ciclo e corresponde à área delimitada pela curva do ciclo. O trabalho produzido pelos tempos de ciclo, a taxa do ciclo (ciclos por segundo) é igual à potência produzida pelo motor Diesel.
Processo isentrópico
Um processo isentrópico é um processo termodinâmico , no qual a entropia do fluido ou gás permanece constante. Isso significa que o processo isentrópico é um caso especial de um processo adiabático no qual não há transferência de calor ou matéria. É um processo adiabático reversível . A suposição de que não há transferência de calor é muito importante, pois podemos usar a aproximação adiabática apenas em processos muito rápidos .
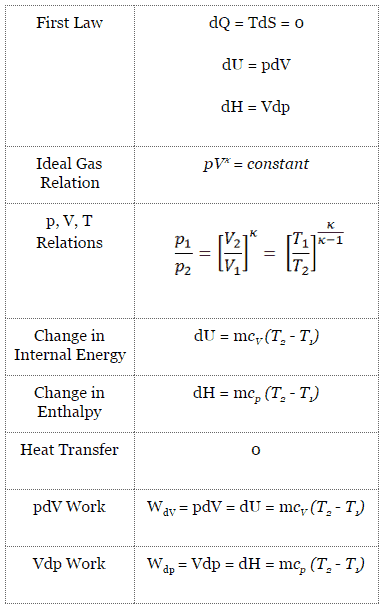
Processo isentrópico e a primeira lei
Para um sistema fechado, podemos escrever a primeira lei da termodinâmica em termos de entalpia :
dH = dQ + Vdp
ou
dH = TdS + Vdp
Processo isentrópico (dQ = 0):
dH = Vdp → W = H 2 – H 1 → H 2 – H 1 = C P (T 2 – T 1 ) (para gás ideal )
Processo isentrópico do gás ideal
O processo isentrópico (um caso especial de processo adiabático) pode ser expresso com a lei dos gases ideais como:
pV κ = constante
ou
p 1 V 1 k = p 2 V 2 k
em que κ = c p / c v é a proporção de aquecimentos específicos (ou capacidades de calor ) para o gás. Um para pressão constante (c p ) e outro para volume constante (c v ) . Observe que essa razão κ = c p / c v é um fator na determinação da velocidade do som em um gás e em outros processos adiabáticos.
Processo Isocórico
Um processo isocórico é um processo termodinâmico, no qual o volume do sistema fechado permanece constante (V = const). Ele descreve o comportamento do gás dentro do recipiente, que não pode ser deformado. Como o volume permanece constante, a transferência de calor para dentro ou para fora do sistema não funciona , mas altera apenas a energia interna (a temperatura) do sistema.
Processo isocórico e a primeira lei
A forma clássica da primeira lei da termodinâmica é a seguinte equação:
dU = dQ – dW
Nesta equação, dW é igual a dW = pdV e é conhecido como trabalho de fronteira . Então:
dU = dQ – pdV
No processo isocórico e no gás ideal , todo o calor adicionado ao sistema será usado para aumentar a energia interna.
Processo isocórico (pdV = 0):
dU = dQ (para gás ideal)
dU = 0 = Q – W → W = Q (para gás ideal)
Processo isocórico do gás ideal
O processo isocórico pode ser expresso com a lei dos gases ideais como:
ou
Em um diagrama pV , o processo ocorre ao longo de uma linha horizontal que possui a equação V = constante.
Veja também: Lei de Guy-Lussac
Processo isobárico
Um processo isobárico é um processo termodinâmico , no qual a pressão do sistema permanece constante (p = const). A transferência de calor para dentro ou para fora do sistema funciona, mas também altera a energia interna do sistema.
Como existem mudanças na energia interna (dU) e no volume do sistema (∆V), os engenheiros costumam usar a entalpia do sistema, que é definida como:
H = U + pV
Processo isobárico e a primeira lei
A forma clássica da primeira lei da termodinâmica é a seguinte equação:
dU = dQ – dW
Nesta equação, dW é igual a dW = pdV e é conhecido como trabalho de fronteira . Em um processo isobárico e no gás ideal, parte do calor adicionado ao sistema será usada para realizar o trabalho e parte do calor adicionado aumentará a energia interna (aumentará a temperatura). Portanto, é conveniente usar a entalpia em vez da energia interna.
Processo isobárico (Vdp = 0):
dH = dQ → Q = H 2 – H 1
Na entropia constante , ou seja, no processo isentrópico, a mudança de entalpia é igual ao trabalho do processo de fluxo realizado no sistema ou pelo mesmo.
Processo isobárico do gás ideal
O processo isobárico pode ser expresso com a lei do gás ideal como:
ou
Em um diagrama de pV , o processo ocorre ao longo de uma linha horizontal (chamada isobar) que possui a equação p = constante.
Veja também: Lei de Charles
Comparação de ciclos diesel reais e ideais
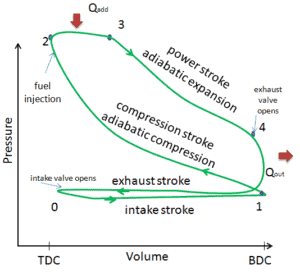 Neste artigo, é mostrado um ciclo Diesel ideal, no qual existem muitas suposições diferentes do ciclo Diesel real . As principais diferenças entre o motor Diesel real e ideal aparecem na figura. Na realidade, o ciclo ideal não ocorre e há muitas perdas associadas a cada processo. Para um ciclo real, a forma do diagrama de pV é semelhante ao ideal, mas a área (trabalho) delimitada pelo diagrama de pV é sempre menor que o valor ideal. O ciclo Diesel ideal é baseado nas seguintes premissas:
Neste artigo, é mostrado um ciclo Diesel ideal, no qual existem muitas suposições diferentes do ciclo Diesel real . As principais diferenças entre o motor Diesel real e ideal aparecem na figura. Na realidade, o ciclo ideal não ocorre e há muitas perdas associadas a cada processo. Para um ciclo real, a forma do diagrama de pV é semelhante ao ideal, mas a área (trabalho) delimitada pelo diagrama de pV é sempre menor que o valor ideal. O ciclo Diesel ideal é baseado nas seguintes premissas:
- Ciclo fechado : A maior diferença entre os dois diagramas é a simplificação dos movimentos de admissão e escape no ciclo ideal. No curso de escape, o calor Q out é ejetado para o ambiente (em um motor real, o gás sai do motor e é substituído por uma nova mistura de ar e combustível).
- Adição de calor isobárico . Em motores reais, a adição de calor nunca é isobárica.
- Sem transferência de calor
- Compressão – O gás é comprimido adiabaticamente do estado 1 ao estado 2. Nos motores reais, sempre existem algumas ineficiências que reduzem a eficiência térmica.
- Expansão. O gás se expande adiabaticamente do estado 3 para o estado 4.
- Combustão completa da mistura.
- Nenhum trabalho de bombeamento . Trabalho de bombeamento é a diferença entre o trabalho realizado durante o golpe de escape e o trabalho realizado durante o golpe de admissão. Nos ciclos reais, há uma diferença de pressão entre as pressões de exaustão e de entrada.
- Sem perda de purga . A perda de purga é causada pela abertura precoce das válvulas de escape. Isso resulta em uma perda de produção durante o curso de expansão.
- Sem perda de impacto . A perda soprada é causada pelo vazamento de gases comprimidos através de anéis de pistão e outras fendas.
- Sem perdas por atrito .
Essas suposições e perdas simplificadoras levam ao fato de que a área fechada (trabalho) do diagrama de pV para um motor real é significativamente menor que o tamanho da área (trabalho) envolvida pelo diagrama de pV do ciclo ideal. Em outras palavras, o ciclo ideal do motor superestimará o trabalho líquido e, se os motores funcionarem na mesma velocidade, maior potência produzida pelo motor real em cerca de 20% (da mesma forma que no caso do motor Otto).
Eficiência térmica para ciclo diesel
Em geral, a eficiência térmica , η th , de qualquer motor de calor é definida como a razão entre o trabalho que faz, W , para o calor de entrada a uma temperatura elevada, Q H .
A eficiência térmica , η th , representa a fração de calor , Q H , que é convertida em trabalho . Como a energia é conservada de acordo com a primeira lei da termodinâmica e a energia não pode ser convertida para funcionar completamente, a entrada de calor, Q H , deve ser igual ao trabalho realizado, W, mais o calor que deve ser dissipado como calor residual Q C no meio Ambiente. Portanto, podemos reescrever a fórmula da eficiência térmica como:
O calor absorvido ocorre durante a combustão da mistura combustível-ar, quando a faísca ocorre, aproximadamente a volume constante. Como durante um processo isocórico não há trabalho realizado pelo sistema ou sobre ele, a primeira lei da termodinâmica determina ∆U = ∆Q. Portanto, o calor adicionado e rejeitado é dado por:
Q add = mc p (T 3 – T 2 )
Q out = mc v (T 4 – T 1 )
Substituindo essas expressões pelo calor adicionado e rejeitado na expressão por eficiência térmica, obtém-se:
Essa equação pode ser reorganizada na forma com a taxa de compressão e a taxa de corte:
Onde
- η Diesel é a eficiência térmica máxima de um ciclo Diesel
- α é a razão de corte V 3 / V 2 (ou seja, a razão de volumes no final e no início da fase de combustão)
- CR é a taxa de compressão
- κ = c p / c v = 1,4
É uma conclusão muito útil, pois é desejável alcançar uma alta taxa de compressão para extrair mais energia mecânica de uma determinada massa do combustível. Como concluímos na seção anterior, a eficiência térmica do ciclo Otto padrão do ar também é uma função da taxa de compressão e κ.
Quando as comparamos com as fórmulas, pode-se observar que, para uma determinada taxa de compressão (CR), o ciclo Otto será mais eficiente que o ciclo Diesel. Mas os motores a diesel geralmente são mais eficientes, pois são capazes de operar com taxas de compressão mais altas.
Nos motores Otto comuns, a taxa de compressão tem seus limites. A taxa de compressão em um motor a gasolina geralmente não será muito superior a 10: 1. Taxas de compressão mais altas sujeitarão os motores a gasolina a bater no motor, causados pela autoignição de uma mistura não queimada, se for usado combustível com classificação mais baixa de octanagem. Nos motores a diesel, há um risco mínimo de autoignição do combustível, porque os motores a diesel são motores de ignição por compressão e não há combustível no cilindro no início do curso de compressão.
Ciclo Diesel – Problema com a Solução

Vamos assumir o ciclo Diesel, que é um dos ciclos termodinâmicos mais comuns encontrados em motores de automóveis . Um dos principais parâmetros desses motores é a mudança de volumes entre o ponto morto superior (TDC) e o ponto morto inferior (BDC). A proporção desses volumes ( V 1 / V 2 ) é conhecida como taxa de compressão . Também a relação de corte V 3 / V 2 , que é a relação dos volumes no final e no início da fase de combustão.
Neste exemplo, vamos assumir o ciclo Diesel com taxa de compressão de CR = 20: 1 e taxa de corte α = 2. O ar está a 100 kPa = 1 bar, 20 ° C (293 K) e o volume da câmara é de 500 cm³ antes do curso de compressão.
- Capacidade térmica específica a pressão constante do ar à pressão atmosférica e à temperatura ambiente: c p = 1,01 kJ / kgK.
- Capacidade térmica específica a um volume constante de ar à pressão atmosférica e à temperatura ambiente: c v = 0,718 kJ / kgK.
- κ = c p / c v = 1,4
Calcular:
- a massa de entrada de ar
- a temperatura T 2
- a pressão p 2
- a temperatura T 3
- a quantidade de calor adicionada pela queima da mistura combustível-ar
- a eficiência térmica deste ciclo
- o deputado
Solução:
1)
No início dos cálculos, temos que determinar a quantidade de gás no cilindro antes do curso de compressão. Usando a lei do gás ideal, podemos encontrar a massa:
pV = mR específico T
Onde:
- p é a pressão absoluta do gás
- m é a massa da substância
- T é a temperatura absoluta
- V é o volume
- R específico é a constante de gás específica, igual à constante de gás universal dividida pela massa molar (M) do gás ou mistura. Para ar seco R específico = 287,1 J.kg -1 .K -1 .
Portanto
m = p 1 V 1 / R específico T 1 = (100000 × 500 × 10 -6 ) / (287,1 × 293) = 5,95 × 10 -4 kg
2)
Nesse problema, todos os volumes são conhecidos:
- V 1 = V 4 = V max = 500 × 10 -6 m 3 (0,5l)
- V 2 = V min = V máx / CR = 25 × 10 -6 m 3
Observe que (V max – V min ) x número de cilindros = cilindrada total do motor
Como o processo é adiabático, podemos usar a seguinte relação p, V, T para processos adiabáticos:
portanto
T 2 = T 1 . CR k – 1 = 293. 20 0,4 = 971 K
3)
Novamente, podemos usar a lei do gás ideal para encontrar a pressão no final do curso de compressão como:
P 2 = mR específico T 2 / V 2 = 5,95 x 10 -4 x 287,1 x 971/25 x 10 -6 = 6.635.000 Pa = 66,35 barra
4)
Como o processo 2 → 3 ocorre a pressão constante, a equação ideal de estado do gás fornece
T 3 = (V 3 / V 2 ) x T 2 = 1942 K
Para calcular a quantidade de calor adicionada pela queima da mistura combustível-ar, adicione Q , precisamos usar a primeira lei da termodinâmica para o processo isobárico, que afirma:
Q add = mc p (T 3 – T 2 ) = 5,95 x 10 -4 x 1010 x 971 = 583,5 J
5)
Eficiência térmica para este ciclo Diesel:
Como foi derivado na seção anterior, a eficiência térmica do ciclo Diesel é uma função da taxa de compressão, da taxa de corte e κ:
- η Diesel é a eficiência térmica máxima de um ciclo Diesel
- α é a razão de corte V 3 / V 2 (ou seja, a razão de volumes no final e no início da fase de combustão)
- CR é a taxa de compressão
- κ = c p / c v = 1,4
Para este exemplo:
η Diesel = 0,6467 = 64,7%
6)
O MEP foi definido como:
Nesta equação, o volume de deslocamento é igual a V max – V min . O trabalho líquido para um ciclo pode ser calculado usando o calor adicionado e a eficiência térmica:
W net = Q add . η Otto = 583,5 x 0,6467 = 377,3 J
MEP = 377,3 / ( 500 × 10 -6 – 25 × 10 -6 ) = 794,3 kPa = 7,943 bar
……………………………………………………………………………………………………………………………….
Este artigo é baseado na tradução automática do artigo original em inglês. Para mais informações, consulte o artigo em inglês. Você pode nos ajudar. Se você deseja corrigir a tradução, envie-a para: translations@nuclear-power.com ou preencha o formulário de tradução on-line. Agradecemos sua ajuda, atualizaremos a tradução o mais rápido possível. Obrigado.